武汉市高二化学上册期末考试题免费试卷
| 1. 选择题 | 详细信息 |
|
下列说法不正确的是 A.用Na2S作沉淀剂,除去废水中的Cu2+和Hg2+ B.向ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀 C.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s) D.溶解度小的沉淀不能转化为溶解度大的沉淀 |
|
| 2. 选择题 | 详细信息 |
|
下列说法正确的是 A.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 B.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol·L-1盐酸、③0.1 mol·L-1氯化镁溶液、④0.1 mol·L-1硝酸银溶液中,Ag+浓度:①>④=②>③ C.除去NH4Cl溶液中的FeCl3杂质:可加入氨水调节溶液至适当pH D.在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动 |
|
| 3. 选择题 | 详细信息 |
已知:Ag++ SCN- = AgSCN↓(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。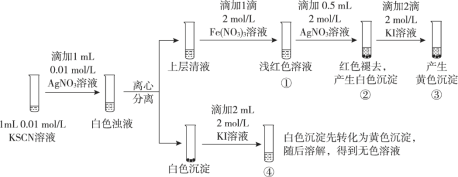 下列说法中,不正确的是 A. ①中现象能说明Ag+与SCN-生成AgSCN沉淀的反应有限度 B. ②中现象产生的原因是发生了反应Fe(SCN)3 + 3Ag+ = 3AgSCN↓+ Fe3+ C. ③中产生黄色沉淀的现象能证明AgI的溶解度比AgSCN的溶解度小 D. ④中黄色沉淀溶解的原因可能是AgI与KI溶液中的I-进一步发生了反应 |
|
| 4. 选择题 | 详细信息 |
|
在含有Ag+的酸性溶液中,以铁铵矾NH4Fe(SO4)2作指示剂,用KSCN的标准溶液滴定Ag+.已知:AgSCN(白色s) A. 边滴定,边摇动溶液,溶液中首先析出AgSCN白色沉淀 B. 当Ag+定量沉淀后,少许过量的SCN-与Fe3+生成红色配合物,即为终点 C. 上述实验可用KCl标准溶液代替KSCN的标准溶液滴定Ag+ D. 滴定时,必须控制溶液一定的酸性,防止Fe3+水解,影响终点的观察 |
|
| 5. 选择题 | 详细信息 |
|
已知25℃时,CaCO3饱和溶液中c(Ca2+)为5.3×10-5 mol·L-1 MgCO3的饱和溶液中c(Mg2+)为2.6×10-3 mol·L-1。若在5 mL浓度均为0.01 mol·L-1的CaCl2和MgCl2溶液中,逐滴加入5 mL 0.012 mol·L-1 Na2CO3溶液,充分反应后过滤得到溶液M和沉淀N(不考虑溶液体积的变化)。下列观点不正确的是 A.25℃时,Ksp(CaCO3)=2.8×10-9 B.加入Na2CO3溶液的过程中,先生成CaCO3沉淀 C.滤液M中:c(Cl-)>c(Na+)>c(Mg2+)>c(CO32-)>c(OH-) D.滤液M中: 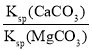 |
|
| 6. 计算题 | 详细信息 | ||||||||
酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物。该电池放电过程产生MnOOH。回收处理该废电池可得到多种化工原料。有关数据如表所示:
|
|||||||||
| 7. | 详细信息 | ||||||||||||||||
锰的用途非常广泛,以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴的碳酸盐及SiO2杂质)为原料生产金属锰的工艺流程如下: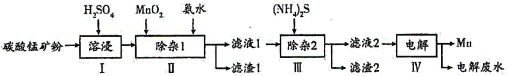 已知25℃时,部分物质的溶度积常数如下:
|
|||||||||||||||||
最近更新



