黑龙江高一化学期中考试(2019年前半期)在线免费考试
| 1. 选择题 | 详细信息 |
|
“物质的量”是指( ) A.物质的质量 B.物质的微观粒子数 C.物质的质量与微观粒子数 D.把物质的质量同微观粒子数联系起来的一个基本物理量 |
|
| 2. 选择题 | 详细信息 | ||||||||
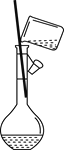
化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。下列实验装置与实验目的对应的是( )
|
|||||||||
| 3. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列对0.3 mol·L-1硫酸钾溶液的说法中正确的是( ) A. 1 L溶液中含0.3NA个K+ B. 1 L溶液中含0.9NA个离子 C. 2 L溶液中K+浓度是1.2 mol·L-1 D. 2 L溶液中含0.6NA个离子 |
|
| 4. 选择题 | 详细信息 |
|
下列叙述中正确的是( ) ①标准状况下,1LHCl和1LH2O的物质的量相同; ②常温常压下,1gH2和14gN2的体积相同; ③28gCO的体积为22.4L; ④两种物质的物质的量相同,则它们在标准状况下的体积也相同; ⑤同温同体积时,气体的物质的量越大,则压强越大; ⑥同温同压下,气体的密度与气体的相对分子质量成正比 A. ①③④⑥ B. ②⑤⑥ C. ⑤⑥ D. ①⑤⑥ |
|
| 5. 选择题 | 详细信息 |
|
下列电离子方程式错误的是 A.NaHCO3=Na++HCO3- B.NaHSO4=Na++H++SO42- C.KClO3=K++Cl-+3O2- D.H2SO4=2H++SO42- |
|
| 6. 选择题 | 详细信息 |
|
下列说法正确的是 A.碱性氧化物一定是金属氧化物,但酸性氧化物不一定都是非金属氧化物 B.胶体会产生电泳现象是因为胶体吸附带电离子而显电性 C.电解质与非电解质的本质区别是水溶液能否导电 D.离子反应是否能够发生要看离子之间能否发生复分解反应 |
|
| 7. 选择题 | 详细信息 |
|
下列叙述正确的是 A.含有最低价元素的化合物不一定具有很强的还原性 B.元素的单质一定是由氧化或还原该元素的化合物制得 C.阳离子只能得电子被还原,阴离子只能失电子被氧化 D.在化学反应中,得电子越多的氧化剂,其氧化性就越强 |
|
| 8. 选择题 | 详细信息 |
|
钠加热后能在空气中着火燃烧的现象是 A. 黄色火焰,生成白色固体Na2O B. 黄色火焰,生成淡黄色固体Na2O2 C. 紫色火焰,生成淡黄色固体Na2O2 D. 红色火焰,生成黄色固体Na2O |
|
| 9. 选择题 | 详细信息 | ||||||||||||||||||||
下列各组关于强电解质、弱电解质、非电解质的归类正确的( )
|
|||||||||||||||||||||
| 10. 选择题 | 详细信息 |
|
VL Fe2(SO4)3溶液中含有a g Fe3+,取此溶液0.5VL,用水稀释至2VL,则稀释后溶液中SO42-的物质的量的浓度为( ) A. |
|
| 11. 选择题 | 详细信息 |
|
根据下面两个化学方程式判断Fe2+、Cu2+、Fe3+氧化性由强到弱的顺序是①2FeCl3+Cu===2FeCl2+CuCl2 ②CuCl2+Fe===FeCl2+Cu A. Fe3+>Cu2+>Fe2+ B. Fe2+>Cu2+>Fe3+ C. Cu2+>Fe3+>Fe2+ D. Fe3+>Fe2+>Cu2+ |
|
| 12. 选择题 | 详细信息 |
|
固体A在一定温度下分解生成气体B、C和D:2A(s)==B(g)+2C(g)+3D(g)。若测得生成气体的质量是相同体积的H2的15倍,则A的摩尔质量是 ( ) A. 30g/mol B. 60g/mol C. 90g/mol D. 120g/mol |
|
| 13. 选择题 | 详细信息 |
|
下列各组离子在溶液中能大量共存的是( ) A.H+、SO42-、NO3-、Fe2+ B.Mg2+、Cl-、NO3-、OH- C.Ba2+、Na+、CO32-、NO3- D.Na+、Al3+、Cl-、SO42- |
|
| 14. 选择题 | 详细信息 |
|
2Mn2++ 5R2O8X—+8H2O=16H++10RO42—+2MnO4—在酸性溶液中(加热并有Ag催化)可发生如下反应根据上述反应,则R2O8x-中x的值是( ) A. 4 B. 3 C. 2 D. 1 |
|
| 15. 选择题 | 详细信息 |
|
金属铜的提炼多从黄铜矿开始,黄铜矿的熔烧过程主要反应之一为2CuFeS2+O2=_____+2FeS+SO2,若CuFeS2中Cu、Fe的化合价都为+2,S的化合价为﹣2,下列说法正确的是 A.横线中的物质是Cu2S B.CuFeS2仅作还原剂 C.SO2是还原产物,不是氧化产物 D.FeS是氧化产物 |
|
| 16. 选择题 | 详细信息 |
|
已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:Fe3+→Fe2+;MnO4-→Mn2+;Cl2→2Cl-;HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,则得到I2最多的是( ) A. Fe3+ B. MnO4- C. Cl2 D. HNO2 |
|
| 17. 选择题 | 详细信息 |
|
下列反应的离子方程式正确的是 A.石灰乳与Na2CO3溶液混合: Ca2++CO32-=CaCO3↓ B.向Ca(HCO3)2中加入少量NaOH溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O C.氯气通入氢氧化钠溶液中: 2Cl2+2OH-=3Cl-+ClO-+H2O D.钠与水的反应: Na+2H2O =Na++2OH-+H2↑ |
|
| 18. 选择题 | 详细信息 |
某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如下:(所加试剂均过量,气体全部逸出) 下列说法不正确的是 A. 原溶液一定存在CO32-和SO42-,一定不存在Fe3+ B. 若原溶液中不存在Na+,则c(Cl-)<0.1mol·L-1 C. 原溶液中c(Cl-)≥0.1mol·L-1 D. 原溶液一定存在Cl-,可能存在Na+ |
|
| 19. 选择题 | 详细信息 |
已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且 的值与温度高低有关。当n (KOH)=a mol时,下列有关说法错误的是 的值与温度高低有关。当n (KOH)=a mol时,下列有关说法错误的是A.若某温度下,反应后  =11,则溶液中 =11,则溶液中 = =B.参加反应的氯气的物质的量等于 C.改变温度,反应中转移电子的物质的量n的范围: D.改变温度,产物中KClO3的最大理论产量为 |
|
| 20. 填空题 | 详细信息 |
|
Ⅰ.(1)3.01×1022个OH-的物质的量为_____mol;这些OH-与_____molNH3的质量相等,与____g Na+含有的离子数相同。 (2)有四种正盐的混合溶液,含有0.2 mol·L-1 Na+、0.25 mol·L-1 Mg2+、0.4mol·L-1 Cl-,则SO42-的浓度为__ mol·L-1。 Ⅱ.现有以下物质: ①NaCl晶体 ②干冰 ③熔融的KNO3 ④石墨 ⑤BaSO4固体 ⑥蔗糖 ⑦酒精,请回答以下问题(填序号): (1)能导电的是_________; (2)属非电解质的是_________; (3)属于电解质的是________; |
|
| 21. 填空题 | 详细信息 |
|
已知:2Fe2++Cl2===2Cl﹣+2Fe3+,2Br﹣+Cl2===Br2+2Cl﹣,2Fe2++Br2===2Br﹣+2Fe3+。含有a mol FeBr2的溶液中,通入x mol Cl2,请按要求写出通Cl2过程中溶液内发生反应的离子方程式。 (1)当x=0.4a时: ____________________________ (2)当x=a 时: ____________________________ (3)当x=1.5a时: ___________________________ |
|
| 22. 填空题 | 详细信息 |
|
实验室可用KMnO4和浓盐酸反应制取氯气。KMnO4+HCl(浓)=KCl+MnCl2+Cl2↑+H2O(未配平)。 (1)将上述化学方程式配平并改写为离子方程式______。 (2)浓盐酸在反应中显示出来的性质是______。 ①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性 (3)若产生0.5 mol Cl2,则被氧化的HCl______mol,转移的电子的数目约为______。 (4)一定条件下,KMnO4还可以氧化其他还原性物质。 MnO4-+C2O42-+______=Mn2++CO2↑+________完成上述离子方程式,此反应中,发生氧化反应的物质是______;若转移1 mol电子,生成标准状况下CO2__________L。 |
|
| 23. 填空题 | 详细信息 |
|
某化学小组制备氢氧化铁胶体:洁净的小烧杯盛适量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1 mol·L-1氯化铁溶液,至液体呈透明的红褐色。回答下列问题: (1)氢氧化铁胶体中微粒直径的范围是________________。 (2)检验胶体制备成功的操作是__________________________________。 (3)实验中手不慎被玻璃割破,可用氯化铁溶液应急止血,主要原因是____________(填序号)。 ①氯化铁溶液具有杀菌消毒的作用 ②氯化铁溶液能使血液胶体凝固 ③氯化铁溶液能产生氢氧化铁沉淀堵住伤口 ④氯化铁溶液能使血液发生化学变化 (4)制备胶体的化学方程式为_______。如果将1molFeCl3全部制成胶体,胶粒数目______NA(选填“大于”“等于”“小于”)。 |
|
| 24. 综合题 | 详细信息 |
|
某课题研究小组的同学探究钠与水反应之后,又研究了与溶液反应和NaCl溶液的配制。 Ⅰ.将金属钠放入盛有下列溶液的小烧杯中:①Fe2(SO4)3溶液 ②NaCl溶液 ③Na2SO4溶液 ④饱和澄清石灰水 ⑤Ca(HCO3)2溶液。回答下列问题: (1)既有气体,又有白色沉淀产生的是___________________; (2)写出金属钠与①反应的离子方程式___________________; (3)若剩余的金属钠露置在空气中最终会变成___________________。 Ⅱ.配制480mL 0.2 mol·L-1 NaCl溶液。 (1)计算后,需称出NaCl质量为___________g。 (2)在配制过程中,下列操作对所配溶液浓度的影响是(填偏高、偏低或无影响) ①配制前,容量瓶内有水__________ ②溶液未冷却便定容__________ ③定容时仰视刻度线__________ |
|
最近更新