2019-2020年高一上半年12月份月考化学题开卷有益(山东省临沂市沂水县第一中学)
| 1. 选择题 | 详细信息 |
|
《本草图经》中关于绿矾的分解有如下描述:“绿矾形似朴消(Na2SO4·10H2O)而绿色,取此物置于铁板上,聚炭,封之囊袋,吹令火炽,其矾即沸,流出,色赤如融金汁者是真也。”对此段话的说明中肯定错误的是( ) A. 绿矾的化学式为FeSO4·7H2O B. 绿矾分解过程中没有发生电子的转移 C. “色赤”物质可能是Fe2O3 D. 流出的液体中可能含有硫酸 |
|
| 2. 选择题 | 详细信息 |
|
根据中学化学教材所附元素周期表判断,下列叙述不正确的是( ) A. K层电子数为奇数的所有元素所在族的序数与该元素原子的K层电子数相等 B. L层电子数为奇数的所有元素所在族的序数与该元素原子的L层电子数相等 C. L层电子数为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等 D. M层电子数为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等 |
|
| 3. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数,下列叙述中正确的是( ) A.标准状况下, B.1mol氯气与足量铁粉充分反应,转移的电子数为 C. D. |
|
| 4. 选择题 | 详细信息 |
|
等量的Al分别加入0.3 L 1 mol·L-1的盐酸和NaOH溶液中,生成氢气的体积比为1∶2,则加入Al的质量为( ) A.2.7 g B.5.4 g C.8.1 g D.10 g |
|
| 5. 选择题 | 详细信息 |
|
下列各组离子,在酸性溶液中能大量共存,且溶液为无色透明的是( ) A. C. |
|
| 6. 选择题 | 详细信息 |
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等。下列判断不正确的是( )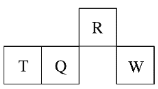 A. 最简单气态氢化物的热稳定性:R>Q B. 最高价氧化物对应水化物的酸性:Q<W C. 原子半径:T>Q>R D. 单质T与NaOH溶液不反应 |
|
| 7. 选择题 | 详细信息 |
|
标准状况下有①0.112 L水 ②3.01×1023个氯化氢分子 ③13.6 gH2S气体 ④0.2 mol氨气,下列对这四种物质的关系由小到大排列正确的是 A.体积:①④③② B.密度:④①②③ C.质量:①④③② D.氢原子数:①③④② |
|
| 8. 选择题 | 详细信息 |
|
下列有关离子(或物质)的检验、现象及结论,都正确的是( ) A. 向某溶液中滴加氯水,再滴加KSCN溶液,溶液变成红色,该溶液中一定含有Fe2+ B. 焰色反应实验中,透过蓝色钴玻璃,可观察到钠离子火焰呈黄色 C. 向FeCl2溶液中滴入用硫酸酸化的H2O2溶液,溶液变黄,说明发生氧化还原反应,且氧化性:H2O2>Fe3+ D. 向某无色溶液中加入BaCl2溶液有白色沉淀出现,再加入稀盐酸,沉淀不消失,则该溶液中一定含有SO42﹣ |
|
| 9. 选择题 | 详细信息 |
|
下列离子方程式书写正确的是( ) A. 钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ B. 向FeCl3溶液中加入几滴KSCN溶液:3SCN-+Fe3+ =Fe(SCN)3 ↓ C. 稀硫酸和氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ D. 碳酸钙与盐酸反应:CO32-+2H+=CO2↑+H2O |
|
| 10. 选择题 | 详细信息 |
|
向一定量的Fe、FeO、Fe2O3的混合物中,加入500 mL 1 mol/L的盐酸,恰好使混合物完全溶解,放出672 mL(标准状况)气体。向所得溶液中加入KSCN溶液无血红色出现,那么若用足量的CO在高温下还原相同质量的此混合物,能得到铁( ) A. 28 g B. 14 g C. 12.32 g D. 条件不足,无法计算 |
|
| 11. 选择题 | 详细信息 | ||||||||||
已知下列原子的半径:
|
|||||||||||
| 12. 选择题 | 详细信息 |
|
下列有关化学用语表示正确的是( ) A.氮气的电子式: B.用电子式表示氯化钠的形成过程: C.重水的化学式为 D.N2H4的结构式 |
|
| 13. 选择题 | 详细信息 |
|
亚硝酸钠(NaNO2)具有致癌作用,许多腌制食品中含NaNO2。酸性KMnO4溶液与亚硝酸钠反应的离子反应:MnO4- +NO2- +H+ → Mn2++NO3- +H2O(未配平),下列叙述错误的是 A.生成1mol Mn2+,转移电子为5mol B.该反应中氮元素被还原 C.配平后,水的化学计量数为3 D.反应中氧化产物与还原产物的物质的量之比为2:5 |
|
| 14. 选择题 | 详细信息 |
将2.32gNa2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况) 关系如图所示,下列说法中错误的是( )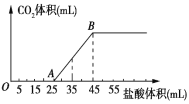 A.OA段发生反应的离子方程式为:H++OH-=H2O、CO32-+H+=HCO3- B.A点溶液中的溶质为NaCl、NaHCO3 C.混合物中NaOH的质量0.60g D.当加入35mL盐酸时,产生CO2的体积为224mL |
|
| 15. 选择题 | 详细信息 | |||||||||||||||||||||
如图所示是元素周期表的一部分,下列说法中正确的是 ( )
|
||||||||||||||||||||||
| 16. 实验题 | 详细信息 |
实验室有化学纯的浓硫酸,其试剂瓶标签上的部分内容如下图: 请回答下列问题: (1)配制溶液时,一般可以分为以下几个主要步骤: ①量取 ②计算 ③溶解 ④定容 ⑤转移 ⑥洗涤 ⑦装瓶,其正确的操作顺序为___________(填序号)。 (2)实验室只有100 mL、250 mL、500 mL三种规格的容量瓶,但要配制480 mL 0.50 mol/L的稀硫酸,需取该浓硫酸______mL。 (3)接下来完成此实验你将用到的仪器有20 mL量筒、烧杯、玻璃棒、____________。 (4)要从所配溶液中取出50 mL盛装于试剂瓶中,给它贴上标签,则标签的内容是________________;若再从中取出10 mL溶液稀释至20 mL,则稀释后溶液的物质的量浓度为__________。 (5)下列操作会使所配溶液浓度偏低的是__________。 A. 用量筒量取浓硫酸,读数时仰视刻度线 B. 转移溶液时未洗涤烧杯 C. 容量瓶用蒸馏水洗净后仍残留有蒸馏水 D. 定容时俯视容量瓶的刻度线 E. 定容摇匀后,发现液面低于刻度线,再加水至刻度线 |
|
| 17. 推断题 | 详细信息 |
如图是中学化学中常见物质的转化关系,部分物质和反应条件略去。 请回答下列问题: (1)物质A的化学式为_____。 (2)写出单质B与强碱溶液反应的离子方程式_____,氧化物D与NaOH溶液反应的化学方程式_____。 (3)溶液E中加入氨水时,先生成白色沉淀L,L最终变为红褐色沉淀G,写出L变为G的化学反应方程式_____。 (4)溶液E敞口放置容易变质,写出检验溶液E是否变质的实验操作、现象及结论_____。为了防止溶液E的变质,可往溶液中加入_____。用离子方程式说明______________ (5) 把3.06 g铝和镁的混合物粉末放入100 mL盐酸中,恰好完全反应,并得到标准状况下3.36 L H2。则该合金中铝的物质的量_____,反应后溶液中Cl-的物质的量浓度_____(假定反应体积仍为100 mL) |
|
| 18. 实验题 | 详细信息 |
|
过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易吸收空气中CO2而变质。 (1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入_______________溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。 (2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取ag样品,并设计用如图装置 来测定过氧化钠的质量分数。 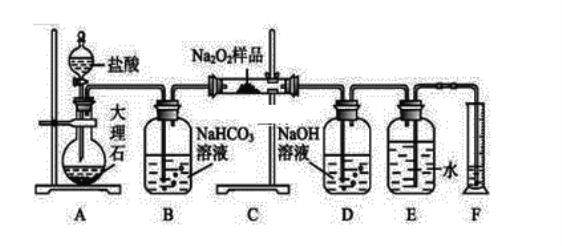 ①A中发生反应离子方程式为___________________ ②将仪器连接好以后,必须进行的第一步操作是__________ ③写出装置C中发生的所有反应的化学方程式______________________________,_______________________________________________________ ④D中NaOH溶液的作用__________________________ ⑤读出量筒内水的体积后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分 数为__________________ |
|
| 19. 填空题 | 详细信息 |
|
下面是同学们熟悉的物质: ①O2 ②H2O2 ③MgCl2 ④H2SO4 ⑤Na2CO3⑥NH4Cl ⑦CO2 ⑧Ne ⑨Na2O2 ⑩NaOH (1)这些物质中,只含有共价键的是__________________________________(填序号,下同);只含有离子键的是___________________________;既含有极性共价键又含有离子键的是_____________________________;既含有非极性共价键又含有离子键的是________________________不存在化学键的是_________________________________。 属于共价化合物的是_________________________________; (2)写出下列物质的结构式 ①O2 _______________②H2O2_______________⑦CO2_______________ (3)写出下列物质的电子式 ⑥NH4Cl ______________⑨Na2O2 _______________ ⑩NaOH_______________ (4)用电子式表示下列物质的形成 ①O2_______________________________________________________________ ③MgCl2____________________________________________________________ |
|
最近更新



