2018-2019年高二下册开学考试化学试卷带参考答案和解析(安徽省安庆市第二中学)
| 1. 选择题 | 详细信息 |
|
党的十九大报告中多次提到“生态文明”,下列做法不符合生态文明理念的是( ) A. 发展新能源汽车,实现低碳出行 B. 用氯乙烯生产快餐盒,降低白色污染 C. 用地沟油制生物柴油,回收利用资源 D. 科学开发利用自然资源,维护生态平衡 |
|
| 2. 选择题 | 详细信息 |
|
有关能量与能源的说法正确的是 A. 原电池是将电能转变为化学能的装置 B. 逆反应的活化能总是大于正反应的活化能 C. 新能源中的太阳能、风能、生物质能等,都是可再生能源 D. 同温同压下, |
|
| 3. 选择题 | 详细信息 |
|
在四个不同的容器中,在不同的条件下进行合成氨反应,根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是( ) A. v(NH3)=0.1 mol/(L•min) B. v(NH3)=0.2 mol/(L•min) C. v(H2)=0.3 mol/(L•min) D. v(H2)=0.4 mol/(L•min) |
|
| 4. 选择题 | 详细信息 |
|
某温度下,在固定容积的容器中,可逆反应: A. 平衡向逆反应方向转动 B. 平衡不移动 C. C的百分含量增大 D. C的百分含量减小 |
|
| 5. 选择题 | 详细信息 |
|
某浓度的氨水中存在下列平衡: A. ①② B. ②③ C. ③④ D. ②④ |
|
| 6. 选择题 | 详细信息 |
|
100mL 6mol•L﹣1 H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量 A.碳酸钠溶液 B.醋酸钾固体 C.硫酸钾固体 D.硝酸钠溶液 |
|
| 7. 选择题 | 详细信息 |
|
对于反应CO(g)+H2O(g) A. 加入催化剂,改变了反应的途径,反应的△H也随之改变 B. 改变压强,平衡不发生移动,反应放出的热量不变 C. 升高温度,反应速率加快,反应放出的热量不变 D. 若在原电池中进行,反应放出的热量不变 |
|
| 8. 选择题 | 详细信息 |
|
下列事实不能用电化学原理解释的是 A. 可将地下输油钢管与外加直流电源的负极相连以保护钢管不受腐蚀 B. 常温条件下,铝在空气中不易被腐蚀 C. 镀层破坏后,白铁(镀锌的铁)比马口铁(镀锡的铁)更耐腐蚀 D. 用锌和稀硫酸反应产生氢气时,往稀硫酸中滴少量硫酸铜溶液能加快反应速率 |
|
| 9. 选择题 | 详细信息 |
|
在平衡体系Ca(OH)2(s) A. 加入少量MgCl2固体 B. 加入少量Na2CO3固体 C. 加入少量KCl固体 D. 加入少量稀H2SO4 |
|
| 10. 选择题 | 详细信息 |
|
下列物质的水溶液经加热浓缩,蒸干灼烧仍能得到原物质的是 A.FeCl3 B.Cu(NO3)2 C.Na2SO3 D.NaAlO2 |
|
| 11. 选择题 | 详细信息 |
|
下列叙述正确的是 A. 某醋酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=b,则a>b B. 常温下,某溶液中由水电离的c(OH-) = 1.0×10-13mol/L,则此溶液一定呈酸性 C. 25℃时,将pH=4的盐酸稀释1000倍后,溶液的pH=7 D. 25℃时,pH=13的强碱溶液与pH=2的强酸溶液混合,若所得混合液的pH=7,则强碱与强酸的体积比是1:10 |
|
| 12. 选择题 | 详细信息 |
|
在容积不变的密闭容器中,一定条件下发生反应:2A(?)B(g)+C(s),达到化学平衡后,升高温度,容器内气体的密度增大,则下列叙述正确的是( ) A. 若正反应是吸热反应,则A为非气态 B. 若正反应是放热反应,则A为非气态 C. 在平衡体系中加入少量C,该平衡向逆反应方向移动 D. 改变压强对该平衡的移动一定无影响 |
|
| 13. 选择题 | 详细信息 |
t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t ℃时AgCl的Ksp=4×10-10,下列说法不正确的是 A. 在t ℃时,AgBr的Ksp为4.9×10-13 B. 通过蒸发,可使溶液由a点变到c点 C. 图中b点有AgBr沉淀析出 D. 在t ℃时,AgCl(s)+Br-(aq) |
|
| 14. 选择题 | 详细信息 |
利用如图装置可以模拟铁的电化学防护。下列叙述正确的是 ( ) A. 若X为锌片,开关K置于M处,可减缓铁的腐蚀 B. 当K置于N处时,可减缓铁的腐蚀 C. 若X为碳棒,开关K置于M处,可减缓铁的腐蚀 D. 铁被腐蚀过程实质是金属铁失电子发生了还原反应 |
|
| 15. 选择题 | 详细信息 |
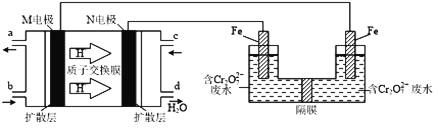
 A. 每消耗2.24 B. 离子交换膜应为阳离子交换膜, C. 该燃料电池的负极反应式为 D. 粗铜中的Ag、Au沉在阳极区,电解质溶液的浓度基本保持不变 |
|
| 16. 选择题 | 详细信息 | |||||||||||||||
常温下浓度均为0.1mol/L 的四种盐溶液,其pH 如表所示,下列说法正确的是( )
|
||||||||||||||||
| 17. 选择题 | 详细信息 |
H2X为二元弱酸,常温下,将NaOH溶液加入到H2X溶液中,在不同pH环境下,不同形态的粒子(酸、酸式酸根、酸根离子)的组成分数如图所示。下列说法正确的是 A. HX-的电离程度小于水解程度 B. 在pH=7的溶液中HX-和X2-能大量共存 C. 在pH=9时,H2X 与NaOH恰好完全中和 D. 1L.0.1 mol•L-1Na2X溶液中,n(HX-)+2n(X2-)+n(H2X)=0.1 mol |
|
| 18. 实验题 | 详细信息 | ||||||||||||
室温下,某一元弱酸HA的电离常数 (1)a、b、c、d四点中水的电离程度最大的是________点,滴定过程中宜选用__________作指示剂,滴定终点在________(填“c点以上”或“c点以下”)。 (2)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视______________________,滴定终点的现象为_____________________________________________________。 (3)若滴定结束时,滴定管中的液面如图所示,则其读数为___________mL。 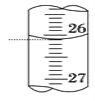 (4)滴定过程中部分操作如下,下列各操作使测量结果偏高的是____________(填字母序号)。 A.滴定前碱式滴定管未用标准NaOH溶液润洗 B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定 C.滴定过程中,溶液出现变色后,立即停止滴定 D.滴定结束后,仰视液面,读取NaOH溶液体积 (5)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为_____
|
|||||||||||||
| 19. 填空题 | 详细信息 |
|
(1)已知:① ②2 ③ 则 (2)汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致: ①某温度下,向2L的密闭容器中充入 ②将 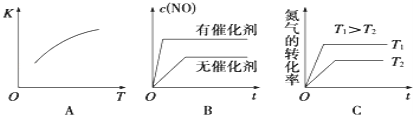 ③该温度下,某时刻测得容器内 |
|
| 20. 解答题 | 详细信息 | ||||||||
胆矾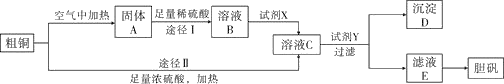
|
|||||||||
| 21. 综合题 | 详细信息 | ||||||||
|
甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料. (1)以下是工业上合成甲醇的反应: 下表所列数据是该反应在不同温度下的化学平衡常数(K).
|
|||||||||