湖南省邵东县第一中学2020届高三上学期第二次月考化学题开卷有益
| 1. 选择题 | 详细信息 |
|
中华文化源远流长、博大精深。从化学的视角看,下列理解不正确的是( ) A. “千淘万漉虽辛苦,吹尽黄沙始到金”中“淘”“漉”相当于分离提纯操作中的“过滤” B. 司母戊鼎属青铜制品,是我国古代科技光辉成就的代表之一 C. 瓷器(China)属硅酸盐产品,China一词又指“瓷器”,这反映了在西方人眼中中国作为“瓷器故乡”的形象 D. 侯德榜是我国化学工业的奠基人,主要成就: 侯氏制碱法,该碱指的是烧碱 |
|
| 2. 选择题 | 详细信息 |
|
既能用浓硫酸又能用碱石灰干燥的气体是 A. Cl2 B. SO2 C. NO D. NH3 |
|
| 3. 选择题 | 详细信息 |
|
只用一种试剂可将NH4Cl、(NH4)2SO4、NaCl、Na2SO4 四种溶液区分开,这种试剂是 A. Ba(OH)2溶液 B. AgNO3溶液 C. BaCl2溶液 D. NaOH 溶液 |
|
| 4. 选择题 | 详细信息 |
|
下列试剂的保存方法不正确的是 A.在盛液溴的试剂瓶中加水,形成“水封”,以减少溴挥发 B.金属钠通常密封保存在煤油中 C.浓硝酸通常保存在棕色细口瓶并置于阴凉处 D.NaOH溶液保存在配有玻璃塞的细口瓶中 |
|
| 5. 选择题 | 详细信息 |
|
常温下,将等质量的铝片、银片、铁片、铜片分别置于四个小烧杯中,然后分别加足量的浓硝酸,放出NO2气体最多的是 A.铝片 B.铜片 C.铁片 D.银片 |
|
| 6. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的值。下列有关叙述错误的是 A.80 g CuO和Cu2S的混合物中,所含铜原子数为NA B.1 mol NaBH4与足量水反应(NaBH4+2H2O=NaBO2+4H2↑)时转移的电子数为4NA C.标准状况下,2.24L Cl2溶于水,转移的电子数目为0.1 NA D.室温下1L pH=13的Ba(OH)2溶液中,含有OH-0.1NA个 |
|
| 7. 选择题 | 详细信息 |
|
向KOH溶液中通入11.2 L(标准状况)氯气恰好完全反应生成三种含氯盐: 0.7molKCl、0.2molKClO和X。则X是 A. 0.1molKClO4 B. 0.1molKClO3 C. 0.2molKClO2 D. 0.1molKClO2 |
|
| 8. 选择题 | 详细信息 |
|
下列解释实验过程或事实的反应方程式不正确的是 A. 熔融烧碱时,不能使用普通石英坩埚:SiO2+2NaOH B. 在海带灰的浸出液(含有I-)中滴加H2O2得到I2:2I-+ H2O2+2H+= I2+O2↑+2H2O C. 红热的铁丝与水接触,表面形成蓝黑色(或黑色)保护层:3Fe+ 4H2O(g) D. “84消毒液”(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用放出氯气:ClO-+ Cl-+ 2H+= Cl2↑+H2O |
|
| 9. 选择题 | 详细信息 | |||||||||||||||
下列离子组在给定条件下可能大量共存的是
|
||||||||||||||||
| 10. 选择题 | 详细信息 |
南海是一个巨大的资源宝库,开发利用这些资源是科学研究的重要课题。下图为海水资源利用的部分过程,有关说法正确的是( ) A. 海水淡化的方法主要有蒸馏法、电渗析法、冰冻法 B. 氯碱工业中采用阴离子交换膜可提高产品的纯度 C. 由MgCl2·6H2O得到无水MgCl2的关键是要低温小火烘干 D. 溴工业中③、④的目的是为了富集溴元素,溴元素在反应③、⑤中均被氧化,在反应④中被还原 |
|
| 11. 选择题 | 详细信息 |
某实验小组设计如下实验装置(图中夹持装置省略)测定制备的CaCO3粉末的纯度(样品中杂质不与酸反应,反应前装置中的CO2已全部排出)。下列说法错误的是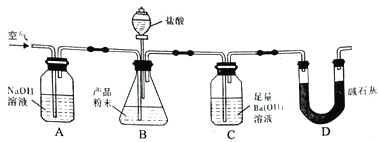 A. 缓入空气的作用是将反应结束后装置中残留的CO2全部鼓入到C装置中被吸收 B. A装置和D装置都是为了防止空气中的CO2气体进入C 装置而产生误差 C. 为了防止B 中盐酸挥发产生干扰,必须在B、C装置中间加一个装有饱和碳酸氢钠溶液的洗气瓶 D. 若CaCO3样品的质量为x,从C 中取出的沉淀洗净干燥后的质量为y,则CaCO3的纯度为 |
|
| 12. 选择题 | 详细信息 |
|
“化学实验→观察现象→分析推理→得出结论”是化学学习的方法之一。下列说法正确的是( ) A. 证明某红棕色气体是溴蒸气还是NO2,可用湿润的淀粉-KI 试纸检验,观察试纸颜色变化 B. 将SO2通入足量稀Fe(NO3)3溶液,溶液由棕黄色变为浅绿色,但立即又变成棕黄色,假设通入的SO2完全反应,则同温同压下,逸出气体和SO2的体积比为2∶3 C. 验证淀粉的水解产物是否具有还原性,取水解液于试管中并加入新制氢氧化铜悬浊液,加热煮沸,观察是否出现砖红色沉淀 D. 向铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色褪去,该过程中发生的反应为 2Al+3Ag2S=6Ag+Al2S3 |
|
| 13. 选择题 | 详细信息 |
|
中学常见的某反应化学方程式为X +Y→M+N +H2O(未配平,反应条件已略去),下列叙述错误的是 A. 若X、Y的物质的量之比为1:4,且N是黄绿色气体,则该反应的离子方程式为MnO2+4H++2Cl- B. 若M、N为气体,且都能使澄清石灰水变浑浊,则将此混合气体通入溴水中,橙色褪色,橙色褪色过程的离子方程式为SO2+Br2+2H2O=4H++SO42-+2Br- C. 若X是铁,Y是稀硝酸(过量),则X与Y反应的离子方程式为Fe+4H++NO3- = Fe3+ +NO↑+2H2O D. 当N为氯碱工业的主要原料,M是造成温室效应的主要气体,则上述反应的离子方程式一定为:CO32-+2H+=CO2↑+H2O |
|
| 14. 选择题 | 详细信息 |
下列有关各实验的叙述中正确的是 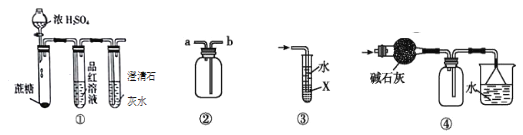 A. ①澄清石灰水变浑浊,证明蔗糖与浓硫酸反应生成了CO2 B. ②进行H2、NH3、CO2、Cl2、NO、NO2等气体的收集 C. ③当X选用苯时可进行NH3或HCl的吸收,并防止倒吸 D. ④可用于NH3的干燥,收集并吸收多余NH3 |
|
| 15. 选择题 | 详细信息 |
粉煤灰中的氮可通过如图所示方法处理生成对环境无影响的氮气,下列说法正确的是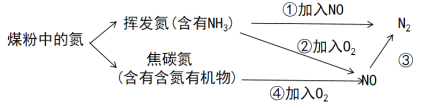 A.反应③中加入的物质可以是空气或氨气 B.反应①中,每生成22.4L(标况下)N2,转移电子2.4mol C.用湿润的蓝色石蕊试纸可判断挥发氮中含有NH3 D.焦碳氮在空气中充分燃烧产生的尾气可直接排放 |
|
| 16. 选择题 | 详细信息 | ||||||||||||||||||||
根据下列实验和现象,所得实验结论正确的是( )
|
|||||||||||||||||||||
| 17. 选择题 | 详细信息 |
美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示)。下列有关该工艺的说法错误的是( )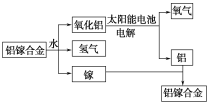 A.铝镓合金可以循环使用 B.该过程中,能量的转化形式只有两种 C.铝镓合金与水反应的化学方程式为:2Al+3H2O  Al2O3+3H2↑ Al2O3+3H2↑D.总反应式为2H2O  2H2↑+O2↑ 2H2↑+O2↑ |
|
| 18. 选择题 | 详细信息 |
某溶液由Na+、Cu2+、Ba2+、Fe3+、AlO A. 原溶液中一定只存在 B. 气体A的化学式是CO2,其电子式为O::C::O C. 原溶液中一定不存在的离子是Cu2+、Ba2+、Fe3+ D. 生成沉淀B的离子方程式为:Al3++3OH===Al(OH)3↓ |
|
| 19. 选择题 | 详细信息 |
某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。现进行如下图所示实验。下列有关说法正确的是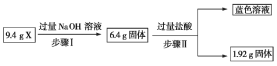 A. 步骤Ⅰ中减少的3 g固体一定是混合物 B. 步骤Ⅱ中质量减少的固体物质一定是Fe2O3 C. 根据上述步骤Ⅱ可以得出蓝色溶液中n(Cu2+)=0.02 mol D. 根据步骤Ⅰ、Ⅱ可以判断X中氧化铁的质量分数为50% |
|
| 20. 填空题 | 详细信息 |
|
(1) (2)实验室常用 (3)将 (4) |
|
| 21. 实验题 | 详细信息 |
叠氮化钠(NaN3)是一种白色剧毒晶体,是汽车安全气囊的主要成分。NaN3易溶于水,微溶于乙醇,水溶液呈弱碱性,能与酸发生反应产生具有爆炸性的有毒气体叠氮化氢。实验室可利用亚硝酸叔丁酯(t-BuNO2,以t-Bu表示叔丁基)与N2H4、氢氧化钠溶液混合反应制备叠氮化钠。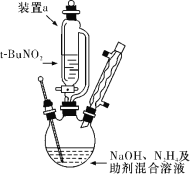 (1)按如图所示组装仪器(加热装置略)进行反应,反应方程式为:t-BuNO2+NaOH+N2H4=NaN3+2H2O+t-BuOH ①装置a的侧管的作用是________________; ②该反应需控制温度在65 ℃,采用的实验措施是_______________; ③反应后溶液在0 ℃下冷却至有大量晶体析出后过滤,所得晶体使用无水乙醇洗涤。试解释低温下过滤和使用无水乙醇洗涤晶体的原因是_________。 (2)产率计算 ①称取2.0 g叠氮化钠试样,配成100 mL溶液,并量取10.00 mL溶液于锥形瓶中。 ②用滴定管加入0.10 mol·L-1六硝酸铈铵[(NH4)2Ce(NO3)6]溶液40.00 mL发生的反应为[2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑](假设杂质均不参与反应)。 (3)充分反应后将溶液稀释并酸化,滴入2滴邻菲罗啉指示液,并用0.10 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]为标准液,滴定过量的Ce4+,终点时消耗标准溶液20.00 mL(滴定原理:Ce4++Fe2+=Ce3++Fe3+)。计算可知叠氮化钠的质量分数为_______(保留2位有效数字)。 (4)叠氮化钠有毒,可以使用次氯酸钠溶液对含有叠氮化钠的溶液进行销毁,反应后溶液碱性明显增强,且产生无色无味的无毒气体,试写出反应的离子方程式:____________________。 |
|
| 22. | 详细信息 |
粉煤灰是燃煤电厂的废渣,主要成分为SiO2、Al2O3、Fe2O3和C等。实验室模拟工业从粉煤灰提取活性Al2O3,其流程如图: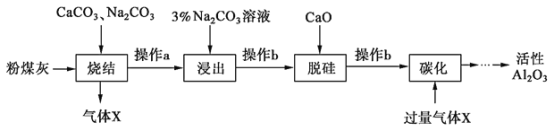 已知烧结过程的产物主要是:NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等。 (1)写出烧结过程中铝元素转化的化学方程式________________________________。 (2)操作b的名称是_______ ,所用的玻璃仪器有_________________________和烧杯。 (3)浸出过程中,NaFeO2可完全水解,水解反应的离子方程式为_______________。 (4)“碳化”时生成沉淀的化学式为______________。 |
|
| 23. | 详细信息 |
高锰酸钾常用作消毒杀菌、水质净化剂等。某小组用软锰矿(主要含MnO2,还含有少量SiO2、Al2O3、Fe2O3等杂质)模拟工业制高锰酸钾流程如下。试回答下列问题。 (1)焙烧过程中发生的主要反应为MnO2+KOH+O2 (2)滤渣Ⅱ是________,第一次通CO2不能用稀硫酸代替的原因是_____________。 (3)第二次通入过量的CO2生成MnO2的离子方程式为___________________。 (4)由图可知,从滤液Ⅲ得到KMnO4需经过__________________、洗涤等操作。 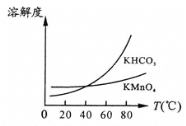 |
|
最近更新




