营口市2020年高二化学后半期期末考试网上在线做题
| 1. 选择题 | 详细信息 |
|
进行化学实验要注意实验安全,正确的实验操作是获得正确的实验结果和保障人身安全的前提。下图中的实验操作正确的是( ) A. 熄灭酒精灯  B. 稀释浓硫酸 B. 稀释浓硫酸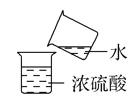 C. 检验钾离子 C. 检验钾离子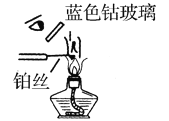 D. 称量氢氧化钠 D. 称量氢氧化钠 |
|
| 2. 选择题 | 详细信息 | |||||||||||||||||||||||||
下列除杂试剂或方法有错误的是
|
||||||||||||||||||||||||||
| 3. 选择题 | 详细信息 |
|
实验室需480 mL 1.0 mol/L的NaOH溶液,假如其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是 A.称取氢氧化钠20.0 g B.定容时俯视观察刻度线 C.移液时,对用于溶解氢氧化钠的烧杯没有进行冲洗 D.移液用玻璃棒引流时,玻璃棒下端靠在容量瓶刻度线上方 |
|
| 4. 选择题 | 详细信息 |
|
从海带中提取碘的实验过程中,涉及下列操作,其中正确的是( ) A. 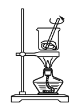 将海带灼烧成灰 B. 将海带灼烧成灰 B.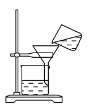 过滤得含I-的溶液 过滤得含I-的溶液C.  萃取后下面放出碘的苯溶液 D. 萃取后下面放出碘的苯溶液 D.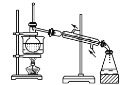 分离碘并回收苯 分离碘并回收苯 |
|
| 5. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数,则下列叙述正确的是 A.标准状况下,2.24LCCl4中含有0.4NA个碳氯单键 B.22.4LCl2通入水中充分反应,共转移NA个电子 C.1 L 1 mol/L的氯化铜溶液中Cu2+的数目小于NA D.5.6g铁在0.1 mol氯气中充分燃烧,转移的电子数为0.3NA |
|
| 6. 选择题 | 详细信息 |
|
下列化学式对应的结构式从成键情况看不合理的是( ) A.CH3N, 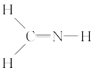 B.CH2SeO, B.CH2SeO, C.CH4S, 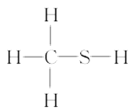 D.CH4Si, D.CH4Si,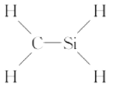 |
|
| 7. 选择题 | 详细信息 |
|
下列有关电子排布图的表述正确的是 A. B. C. D. |
|
| 8. 选择题 | 详细信息 |
|
长式周期表共有18个纵行,从左到右排为1﹣18列,即碱金属为第一列,稀有气体元素为第18列。按这种规定,下列说法正确的是 A. 第9列元素中没有非金属元素 B. 只有第二列的元素原子最外层电子排布为ns2 C. 第四周期第9列元素是铁元素 D. 第10、11列为ds区 |
|
| 9. 选择题 | 详细信息 |
|
现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p4 ,②1s22s22p63s23p3,③1s22s22p3,④1s22s22p5,则下列有关比较中正确的是 A. 原子半径:④>③>②>① B. 第一电离能:④>③>②>① C. 电负性:④>③>②>① D. 最高正化合价:④>③=②>① |
|
| 10. 选择题 | 详细信息 |
|
配位化合物的数量巨大,组成和结构形形色色,丰富多彩。请指出配合物[Cu(NH3)4](OH)2的中心离子、配体、中心离子的电荷数和配位数( ) A.Cu2+、NH3、2+、2 B.Cu+、NH3、1+、4 C.Cu2+、OH-、2+、2 D.Cu2+、NH3、2+、4 |
|
| 11. 选择题 | 详细信息 |
|
下列描述正确的是( ) A. CS2为V形极性分子 B. SiF4与SO C. C2H2分子中σ键与π键的数目比为1︰1 D. 水加热到很高温度都难分解是因水分子间存在氢键 |
|
| 12. 选择题 | 详细信息 |
|
如图是A,b两种不同物质的熔化曲线,下列说法中正确的是( ) ①a是晶体 ②a是非晶体 ③b是晶体 ④b是非晶体. 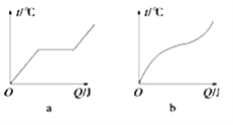 A. ①④ B. ②④ C. ①③ D. ②③ |
|
| 13. 选择题 | 详细信息 |
钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法不正确的是( )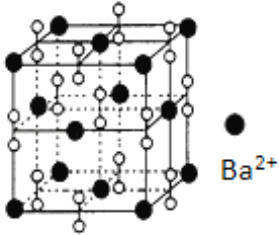 A. 该晶体属于离子晶体 B. 晶体的化学式为Ba2O2 C. 该晶体晶胞结构与NaCl相似 D. 与每个Ba2+距离相等且最近的Ba2+共有12个 |
|
| 14. 选择题 | 详细信息 |
|
在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是 A. sp,范德华力 B. sp2,范德华力 C. sp2,氢键 D. sp3,氢键 |
|
| 15. 选择题 | 详细信息 |
N2的结构可以表示为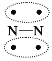 ,CO的结构可以表示为 ,CO的结构可以表示为 ,其中椭圆框表示 π键,下列说法不正确的是( ) ,其中椭圆框表示 π键,下列说法不正确的是( )A.N2 分子与 CO 分子中都含有三键 B.CO 分子中有一个 π 键是配位键 C.N2 与 CO 互为等电子体 D.N2 与 CO 的化学性质相同 |
|
| 16. 选择题 | 详细信息 |
|
下列各组原子中,彼此化学性质一定相似的是( ) A. 原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 B. 原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子 C. 2p轨道上只有2个电子的X原子与3p轨道上只有2个电子的Y原子 D. 最外层都只有一个电子的X、Y原子 |
|
| 17. 选择题 | 详细信息 |
|
X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结构,工业上通过分离液态空气获得其单质;Y元素原子最外电子层上s、p电子数相等;Z元素+2价阳离子的核外电子排布与氖原子相同;W元素原子的M层有1个未成对的p电子。下列有关这些元素性质的说法一定正确的是 A. X元素的氢化物的水溶液显碱性 B. Z元素的离子半径大于W元素的离子半径 C. Z元素的单质在一定条件下能与X元素的单质反应 D. Y元素最高价氧化物的晶体具有很高的熔点和沸点 |
|
| 18. 填空题 | 详细信息 |
I .以下是实验室常用的部分仪器,请回答下列问题: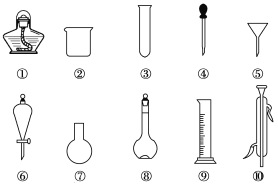 (1)序号为⑧和⑩的仪器的名称分别为______、______。 (2)在分液操作中,必须用到上述仪器中的____(填序号)。 (3)能作反应容器且可直接加热的仪器是上述中的___(填名称)。 (4)在配制溶液时,需要用到的仪器是________(填序号)。 (5)仪器上标有温度的是____(填序号)。 ‖.请选择下列实验方法分离混合物,并将分离方法的序号填在横线上。 A 萃取分液; B 升华; C 结晶 ;D 分液 ;E 蒸馏 ; F 过滤。 (1)___分离饱和食盐水与沙子的混合物。 (2)___从硝酸钾和氯化钠的混合液中获得硝酸钾。 (3)____分离水和汽油的混合物。 (4)___分离CCl4和苯(二者互溶)的混合物。 |
|
| 19. 推断题 | 详细信息 | ||||||||||||||||
已知X、Y、Z、W、Q、R、E七种元素中,原子序数X<Y<Z<W<Q<R<E,其结构或性质信息如下表。
|
|||||||||||||||||
| 20. 推断题 | 详细信息 |
|
A、B、C、D、E、F为元素周期表中前四周期元素,且原子序数依次增大,A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C的氧化物是导致酸雨的主要物质之一,D原子核外电子有8种不同的运动状态,E的基态原子在前四周期元素的基态原子中单电子数最多,F元素的基态原子最外能层只有一个电子,其他能层均已充满电子。 (1)写出基态E原子的价电子排布式_______。 (2)A与C可形成CA3分子,该分子中C原子的杂化类型为______,该分子的立体结构为_____;C的单质与BD化合物是等电子体,据等电子体的原理,写出BD化合物的电子式______;A2D由液态形成晶体时密度减小,其主要原因是__________(用文字叙述)。 (3)已知D、F能形成一种化合物,其晶胞的结构如图所示,则该化合物的化学式为___;若相邻D原子和F原子间的距离为a cm,阿伏加德罗常数的值为 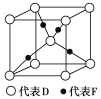 |
|
| 21. 综合题 | 详细信息 |
|
五种短周期元素X、Y、Z、W、Q的原子序数依次增。X、Y是非金属元素X、Y、Q元素的原子最高能级上电子数相等;Z元素原子的最外层电子数是次外层的两倍;W元素原子核外有三种不同的能级且原子中p亚层与s亚层电子总数相等;Q元素电离能分别是I1=496,I2=4562,I3=6912。回答下列问题: (1)基态Q原子的核外电子排布式是____________________。 (2)Q、W形成的化合物Q2W2中的化学键类型是______________。 (3)Y能与氟元素形成YF3,该分子的空间构型是_______,该分子属于______分子(填“极性”或“非极性”)。Y与X可形成具有立体结构的化合物Y2X6,该结构中Y采用______杂化。 (4)Y(OH)3是一元弱酸,其中Y原子因缺电子而易形成配位键,写出Y(OH)3在水溶液中的电离方程式_______________。 (5) Z的一种单质晶胞结构如下图所示。 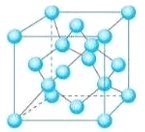 ①该单质的晶体类型为___________。 ②含1 mol Z原子的该晶体中共有_____mol化学键。 ③己知Z的相对原子质量为M,原子半径为r pm,阿伏伽德罗常数的值为NA,则该晶体的密度为____g·cm-3。 |
|
最近更新



