高一下学期期中考试化学试卷带参考答案和解析(2019-2020年浙江省诸暨中学)
| 1. 选择题 | 详细信息 |
|
氦气的分子式是 A.He B.He2 C.He3 D.He4 |
|
| 2. 选择题 | 详细信息 |
|
根据物质的组成与性质进行分类,纯碱属于 A.氧化物 B.酸 C.碱 D.盐 |
|
| 3. 选择题 | 详细信息 |
|
仪器名称为"蒸发皿”的是 A. |
|
| 4. 选择题 | 详细信息 |
|
下列分散系能产生“丁达尔效应”的是( ) A.稀盐酸 B.氢氧化铁胶体 C.泥浆 D.硫酸钾溶液 |
|
| 5. 选择题 | 详细信息 |
|
下列属于非电解质的是 A.SO3 B.KClO3 C.Ca(OH)2 D.Cl2 |
|
| 6. 选择题 | 详细信息 |
|
反应 MnO2+4HCl(浓) A.MnO2- B.HCl C.MnCl2 D.Cl2 |
|
| 7. 选择题 | 详细信息 |
|
下 列表示正确的是 A.铝离子的结构示意图:  B.乙烯的结构式:CH2=CH2 B.乙烯的结构式:CH2=CH2C.氯化氢的球棍模型为: |
|
| 8. 选择题 | 详细信息 |
|
下列说法不正确的是 A.12C和14C互为同位素 B.甲烷和丁烷互为同系物 C.乙醇和二甲醚互为同分异构体 D.Na2O 和Na2O2互为同素异形体 |
|
| 9. 选择题 | 详细信息 |
|
下列说法不正确的是 A.实验室应将钠保存在煤油中 B.分液漏斗和容量瓶在使用前都要检漏 C.可用酒精代替CCl4萃取碘水中的碘单质 D.蒸发至只留下少量液体时,应停止加热,用余热将液体蒸干 |
|
| 10. 选择题 | 详细信息 |
|
下 列说法不正确的是 A.工业上通常以氯气和烧碱为原料制造漂白粉 B.我国华为集团自主研发的“麒麟”芯片生产时需要用到硅 C.镁合金可用于制造火箭、导弹和飞机的部件 D.硫酸可用于金属矿石的处理、金属材料表面的清洗 |
|
| 11. 选择题 | 详细信息 |
|
下列方法(必要时可加热)不合理的是 A. 用澄清石灰水鉴别CO和CO2 B. 用水鉴别苯和四氯化碳 C. 用Ba(OH)2溶液鉴别NH4Cl、(NH4)2SO4和K2SO4 D. 用淀粉碘化钾试纸鉴别碘水和溴水 |
|
| 12. 选择题 | 详细信息 |
|
下列说法不正确的是 A. 石灰石、纯碱、石英可作为制备水泥的主要原料 B. 燃煤烟气的脱硫过程可以得到副产品石膏和硫酸铵 C. 硫酸钡可作高档油漆、油墨、塑料、橡胶的原料及填充剂 D. 在催化剂作用下,用玉米、高粱为原料经水解和细菌发酵可制得乙醇 |
|
| 13. 选择题 | 详细信息 |
|
下列说法不正确的是 A.钠着火不能用泡沫灭火器灭火 B.二氧化硅导电能力很强可用于制造光导纤维 C.干燥的氯气能使品红溶液褪色 D.工业上主要采用高温冶炼黄铜矿获得铜 |
|
| 14. 选择题 | 详细信息 |
|
下列方程式不正确的是 A.镁在二氧化碳中燃烧的化学方程式:2Mg+ CO2 B.一水合氨在水中的电离方程式: NH3+H2O= C.氯化铁水解的离子方程式:Fe3+ +3H2O D.乙醇在铜催化下被氧化的化学方程式:2CH3CH2OH+O2 |
|
| 15. 选择题 | 详细信息 |
|
下列实验操作对应的现象不符合事实的是( ) A.  向FeCl3溶液中滴入KSCN溶液,溶液颜色变红 向FeCl3溶液中滴入KSCN溶液,溶液颜色变红B.  将混有少量氯化钾的硝酸钾饱和溶液在冰水中冷却,氯化钾晶体先析出 将混有少量氯化钾的硝酸钾饱和溶液在冰水中冷却,氯化钾晶体先析出C. D.  将灼热的铜丝伸入盛有氯气的集气瓶中,铜丝剧烈燃烧,产生棕黄色的烟 将灼热的铜丝伸入盛有氯气的集气瓶中,铜丝剧烈燃烧,产生棕黄色的烟 |
|
| 16. 选择题 | 详细信息 | ||||||||
下列实验操作对应的现象不符合事实的是
|
|||||||||
| 17. | 详细信息 |
在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器的接触室(见右图)。下列说法错误的是 A. a、b两处的混合气体成分含量相同,温度不同 B. c、d两处的混合气体成分含量相同,温度不同 C. 热交换器的作用是预热待反应的气体,冷却反应后的气体 D. c处气体经热交换后再次催化氧化的目的是提高SO2的转化率 |
|
| 18. 选择题 | 详细信息 |
|
下列说法不正确的是 A.石油分馏是物理变化、煤的液化和气化均属于化学变化 B.葡萄糖、蔗糖、淀粉和纤维素均属于糖类 C.花生油的主要成分是高级脂肪酸甘油酯,属于高分子化合物 D.塑料、合成纤维、合成橡胶都是人工合成的有机高分子 |
|
| 19. 选择题 | 详细信息 |
|
下列说法正确的是 A.1mol乙烷在光照条件下最多能与6mol Cl2发生取代反应 B.乙烯和苯都能与H2发生加成反应,说明二者的分子中均含碳碳双键 C.乙醇与金属钠能反应,且在相同条件下比水与金属钠的反应更剧烈 D.乙醛能被还原成乙醇,但不能被氧化成乙酸 |
|
| 20. 选择题 | 详细信息 |
|
下列说法不正确的是 A.乙烷分子中的所有原子处于同一平面上 B.乙烯为不饱和烃,分子中6个原子处于同一平面 C.苯分子中存在六个碳原子和六个氢原子完全等价的特殊结构 D.相同质量的烷烃完全燃烧时,甲烷的耗氧量最高 |
|
| 21. 选择题 | 详细信息 |
|
下列说法正确的是 A. 向鸡蛋清的溶液中加入浓的硫酸钠溶液或福尔马林,蛋白质的性质发生改变并凝聚 B. 将牛油和烧碱溶液混合加热,充分反应后加入热的饱和食盐水,上层析出甘油 C. 氨基酸为高分子化合物,种类较多,分子中都含有—COOH和—NH3 D. 淀粉、纤维素、麦芽糖在一定条件下可和水作用转化为葡萄糖 |
|
| 22. 选择题 | 详细信息 |
实验室提纯含少量氯化钾杂质的硝酸钾的过程如图所示。下列分析正确的是 A.操作I是过滤,将固体分离除去 B.操作II是加热浓缩,除去杂质氯化钾 C.操作III是过滤、洗涤,将硝酸钾晶体从溶液中分离出来 D.操作I~ III总共需两次过滤 |
|
| 23. 选择题 | 详细信息 |
配制500mL 0.100 mol·Lˉ1的NaCl溶液,部分实验操作示意图如下: 下列说法正确的是 A. 实验中需用的仪器有:天平、250mL容量瓶、烧杯、玻璃棒、胶头滴管等 B. 上述实验操作步骤的正确顺序为①②④③ C. 容量瓶需要用自来水、蒸馏水洗涤,干燥后才可用 D. 定容时,仰视容量瓶的刻度线,使配得的NaCl溶液浓度偏低 |
|
| 24. 选择题 | 详细信息 |
向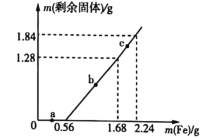 A. B. C. D.原溶液中 |
|
| 25. 选择题 | 详细信息 |
白色固体混合物A,含有KCl、CaCO3、Na2CO3、Na2SiO3、CuSO4中的几种,常温常压下进行如下实验。 下列推断不正确的是 A. 无色溶液B的pH≥7 B. 白色固体F的主要成分是H2SiO3 C. 混合物A中有Na2SiO3、CuSO4和CaCO3 D. 在无色溶液B中加HNO3酸化,无沉淀;再滴加AgNO3,若有白色沉淀生成,说明混合物A中有KCl |
|
| 26. 填空题 | 详细信息 |
|
(1)①写出绿矾的化学式:_________;②写出葡萄糖的分子式:______________。 (2)写出工业上用焦炭在高温下还原二氧化硅制备粗硅的化学方程式:____________________。 |
|
| 27. | 详细信息 |
通过对煤的综合利用,可以获得多种有机物。化合物A含有碳、氢、氧3种元素,其质量比是12:3:8。 液态烃B是一种重要的化工原料,其摩尔质量为78 g/mo1。E是有芳香气味的酯。它们之间的转化关系如下(含有相同官能团的有机物通常具有相似的化学性质): 请回答: (1)化合物A所含的官能团名称是_________________。 (2) B和CH2=CH2反应生成C的反应类型是_____________。 (3) E在氢氧化钠溶液中水解的化学方程式是_______________。 (4)下列说法正确的是_______________。 A.将铜丝在空气中灼烧后迅速插入A中,反应多次,可得到能发生银镜反应的物质 B.确定A中有D或除去A中含有的D都可以用碳酸钠溶液 C.苯甲酸钠(常用作防腐剂)可通过D和氢氧化钠反应得到 D.共a mol的B和D混合物在氧气中完全燃烧,消耗氧气大于7.5a mol |
|
| 28. 推断题 | 详细信息 |
固体化合物X由3种元素组成。某学习小组进行了如下实验: 请回答: (1) 由现象1得出化合物X含有________元素(填元素符号)。 (2) 固体混合物Y的成分________(填化学式)。 (3) X的化学式________。X与浓盐酸反应产生黄绿色气体,固体完全溶解,得到蓝色溶液,该反应的化学方程式是________。 |
|
| 29. 综合题 | 详细信息 |
某学习小组欲从含有[Cu(NH3)4]SO4、乙醇和氨水的实验室废液中分离乙醇并制备硫酸铜铵[CuSO4·(NH4)2SO4]固体,完成了如下实验: 已知:[Cu(NH3)4]2++4H+==Cu2++4NH4+ 请回答: (1)步骤①中,试剂X应采用_____________________________________________。 (2)甲、乙两同学取相同量的溶液Y分别进行蒸馏,收集到的馏出液体积相近,经检测,甲同学的馏出液中乙醇含量明显偏低,可能的原因是_______________________________________________。 (3)设计实验方案验证硫酸铜铵固体中的NH4+___________________________________________ |
|
| 30. 计算题 | 详细信息 |
|
称取Na2CO3和NaOH固体混合物5.32 g,溶于水后加入60 mL 1.0 mol/L的Ba(OH)2溶液充分反应,经过滤、洗涤、干燥,称得沉淀3.94 g。为将滤液处理至中性后达标排放,需加入50 mL稀硫酸。请计算: (1)混合物中NaOH的质量________________。 (2)稀硫酸物质的量浓度__________________。 |
|
最近更新







