夯基提能高三化学上册专题练习在线测验完整版
| 1. 选择题 | 详细信息 |
常温下,用0.1mol/LNaOH溶液滴定10 mL 0.1 mol/LH2A溶液,溶液的pH与NaOH溶液的体积关系如图所示。下列说法不正确的是( )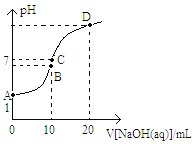 A.A点溶液中加入少量水: B.B点:c( HA -)>c(H+)>c(A2一)>c(H2A) C.C点:c(Na+) =c(HA-)+2c( A2-) D.水电离出来的c(OH -):B点>D点 |
|
| 2. 选择题 | 详细信息 |
|
设 A.lmol B.1mol C.23g乙醇完全氧化生成乙醛时转移的电子总数为 D.2L |
|
| 3. 选择题 | 详细信息 |
|
下列说法正确的是 A. 实验室用Zn和稀硫酸制H2,为加快反应速率,可向稀硫酸中加入少量Cu粉 B. CH3Cl(g)+Cl2(g) C. 在一体积可变的恒温密闭容器中发生反应PCl3(g)+Cl2(g) D. 25℃时Ka(HClO)=3.0×10-8,Ka(HCN)=4.9×10-10,若该温度下NaClO溶液与NaCN溶液pH相同,则c(NaClO)<c(NaCN) |
|
| 4. 选择题 | 详细信息 |
|
下列顺序不正确的是 A.热稳定性:HF>HCl>HBr>HI B.微粒的半径:Cl->Na+>Mg2+>Al3+ C.电离程度(同温度同浓度溶液中):HCl>CH3COOH>NaHCO3 D.分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
|
| 5. 选择题 | 详细信息 |
|
下列指定溶液中一定能大量共存的离子组是( ) A. B.含有大量 C.中性溶液中: D. |
|
| 6. 选择题 | 详细信息 |
|
下列说法中不正确的是( ) ①将硫酸钡放入水中不能导电,所以硫酸钡是非电解质②氨溶于水得到的溶液氨水能导电,所以氨水是电解质③固态共价化合物不导电,熔融态的共价化合物可以导电④固态的离子化合物不导电,熔融态的离子化合物也不导电⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 A.①④ B.①④⑤ C.①②③④ D.①②③④⑤ |
|
| 7. 选择题 | 详细信息 | |||||||||||||||
下列实验操作及现象能够达到对应实验目的是( )
|
||||||||||||||||
| 8. 选择题 | 详细信息 |
|
下列化学用语不正确的是( ) A. B.醛基的电子式:  C.溴乙烷的比例模型是:  D.乙酸乙酯的实验式: |
|
| 9. 选择题 | 详细信息 | ||||||||||||||||||
常温下,几种难溶电解质的溶度积和弱酸的电离常数如下表所示:则下列说法不正确的是( )
|
|||||||||||||||||||
| 10. 选择题 | 详细信息 |
亚氯酸钠是一种高效氧化剂漂白剂,主要用于棉纺、亚麻、纸浆等漂白。亚氯酸钠 A.亚氯酸钠在酸性条件下较稳定 B. C.pH越大,该漂白剂的漂白性能越好 D. |
|
| 11. 选择题 | 详细信息 |
|
下列图示与对应的叙述不相符的是( ) A.  表示1 B.  表示不同温度下水溶液中 C. 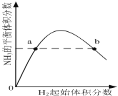 表示一定条件下的合成氨反应中, D.  表示同一温度下,在不同容积的容器中进行反应 |
|
| 12. 选择题 | 详细信息 |
|
下列有关物质应用的说法正确的是( )。 A. 碳酸钠溶液呈碱性,可用热的纯碱溶液除去金属表面的煤油 B. 为加快漂白精的漂白速率,使用时可滴加几滴醋酸 C. 向饱和硼酸溶液中滴加Na2CO3溶液,有CO2气体生成 D. 铝表面易形成致密的氧化膜,铝制器皿可长时间盛放咸菜等腌制食品 |
|
| 13. 选择题 | 详细信息 |
|
下列说法正确的是( ) A.PM2.5是指大气中直径≤2.5×10-6 m的颗粒物,则受PM2.5污染的大气定能产生丁达尔效应 B.根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质 C.黑火药的配方为“一硫二硝三木炭”,其中“硝”是指硝酸 D. |
|
| 14. 选择题 | 详细信息 |
常温下,向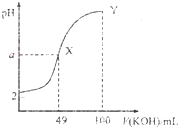 A.当加入 B.HA为弱酸,常温下,Ka的数量级为 C.Y点对应的溶液中: D.若用KOH溶液滴定HA溶液,可选用甲基橙作指示剂 |
|
| 15. 选择题 | 详细信息 |
|
将0.1 mol·L-1的氨水加水稀释至0.01 mol·L-1,稀释过程中温度不变,下列叙述正确的是( ) A.稀释后溶液中c(H+)和c(OH-)均减小 B.稀释后溶液中c(OH-)变为稀释前的1/10 C.稀释过程中氨水的电离平衡向左移动 D.稀释过程中溶液中 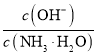 增大 增大 |
|
| 16. 选择题 | 详细信息 |
|
某化学兴趣小组同学对有关物质的分类进行讨论辨析,下列说法正确的是 A. BaSO4、CH3COONH4都属于强电解质 B. SiO2、NO2都属于酸性氧化物 C. NaCl溶液、牛奶都属于溶液 D. CuSO4·5H2O、水玻璃都属于纯净物 |
|
| 17. 选择题 | 详细信息 |
|
下列过程或现象与盐类水解无关的是 A.将FeCl3溶于盐酸配制FeCl3溶液 B.加热稀醋酸溶液其pH降低 C.用低浓度铁盐溶液获得纳米氧化铁 D.小苏打溶液与AlCl3溶液混合产生气体和沉淀 |
|
| 18. 选择题 | 详细信息 |
|
下列各溶液中,微粒的物质的量浓度关系正确的是( ) A. B.在 C. D.10mL |
|
| 19. 选择题 | 详细信息 |
|
下列有关电解质的说法正确的是 A.强电解质一定是离子化合物 B.强电解质、弱电解质的电离都是吸热过程 C.强电解质的饱和溶液一定是浓溶液 D.强电解质在水中一定能全部溶解 |
|
| 20. 选择题 | 详细信息 |
|
现有常温下 A.两溶液中水电离出的 B.加水稀释100倍后两溶液的pH仍相同 C.醋酸中的 D.等体积的两溶液中分别加入足量锌片时放出 |
|
| 21. 选择题 | 详细信息 | ||||||||||||
下表是
|
|||||||||||||
| 22. 选择题 | 详细信息 |
|
中和相同体积、相同pH的 A. |
|
| 23. 选择题 | 详细信息 |
|
下列有关平衡常数K的说法中正确的是( ) A.平衡常数与反应物或生成物的浓度变化无关,温度越高,平衡常数越大 B. C. D. |
|



