河北省衡水市第十四中学2020-2021年高二上学期三调考试化学无纸试卷完整版
| 1. 选择题 | 详细信息 |
|
甲醚(CH3—O—CH3)和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是( ) A.利用金属钠或者金属钾 B.利用质谱法 C.利用红外光谱法 D.利用核磁共振氢谱法 |
|
| 2. 选择题 | 详细信息 |
|
在一定条件下,将A2和B2两种气体通入1L密闭容器中,发生反应:xA2(g)+yB2(g) A.2和3 B.3和2 C.3和1 D.1和3 |
|
| 3. 选择题 | 详细信息 |
|
已知在101KPa,298K条件下,2mol氢气完全燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( ) A.H2O(g)=H2(g)+1/2O2(g);△H=-242kJ·mol-1 B.H2(g)+ C.2H2O(g)=2H2(g)+O2(g);△H=+484kJ·mol-1 D.H2(g)+ |
|
| 4. 选择题 | 详细信息 |
|
下列说法中不正确的是( ) ①高分子化合物不溶于任何溶剂 ②高分子化合物对环境都会产生污染 ③天然高分子材料主要成分都是纤维素 ④塑料均有热塑性 ⑤许多合成高分子材料在性能上优于天然高分子材料. A. ①③④⑤ B. ②③⑤ C. ①②③⑤ D. ①②③④ |
|
| 5. 选择题 | 详细信息 |
|
下列反应在较高温度下才能自发进行的是( ) A.ΔH<0 ΔS<0 B.ΔH<0 ΔS>0 C.ΔH>0 ΔS<0 D.ΔH>0 ΔS>0 |
|
| 6. 选择题 | 详细信息 |
|
下列关于合成材料的说法中,不正确的是( ) A.结构为…—CH=CH—CH=CH—CH=CH—CH=CH—…的高分子的单体是乙炔 B.聚氯乙烯可制成薄膜、软管等,其单体是CH2==CHCl C.合成酚醛树脂( 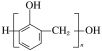 )的单体是苯酚和甲醇 )的单体是苯酚和甲醇D.合成顺丁橡胶( 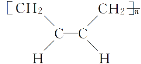 )的单体是CH2=CH—CH=CH2 )的单体是CH2=CH—CH=CH2 |
|
| 7. 选择题 | 详细信息 |
|
下列说法不正确的是 A.淀粉水解液加过量氢氧化钠溶液后,加新制氢氧化铜悬浊液可检验是否水解完全 B.用重铬酸钾的酸性溶液不能鉴别乙醇、乙醛 C.饱和(NH4)2SO4 溶液或硫酸铜溶液均可使蛋白质溶液产生沉淀,但原理不同 D.在苯与液溴制备溴苯的实验中,溴苯提纯步骤:水洗、用10%的氢氧化钠溶液洗涤、水洗、用干燥剂干燥、蒸馏 |
|
| 8. 选择题 | 详细信息 |
|
反应A(g)+3B(g)=2C(g)+2D(g)在四种不同情况下的反应速率分别为 ①v(A)=0.45 mol·L-1·min-1 ②v(B)=0.6 mol·L-1·s-1 ③v(C)=0.4 mol·L-1·s-1 ④v(D)=0.5 mol·L-1·s-1 下列有关反应速率的比较中正确的是 A.④>③=②>① B.①>④>③=② C.①>②>③>④ D.④>③>②>① |
|
| 9. 选择题 | 详细信息 |
|
对于可逆反应:aA(气)+bB(气) A.平衡移动,反应的平衡常数必改变 B.增大压强平衡必移动 C.升高温度平衡必移动 D.加入催化剂平衡必移动 |
|
| 10. 选择题 | 详细信息 |
合成氨反应: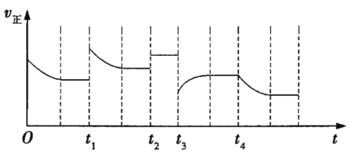 A. C. |
|
| 11. 选择题 | 详细信息 |
参照反应Br+H2→HBr+H的能量对反应历程的示意图,下列叙述中不正确的是( )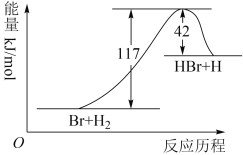 A.该反应的正向活化能为117 kJ/mol B.升高温度使该反应的反应速率降低 C.加入催化剂,不改变该化学反应的反应热 D.从图中可看出,该反应的△H=+75 kJ/mol |
|
| 12. 选择题 | 详细信息 |
|
可逆反应2NO2 ①单位时间内生成nmo1O2的同时生成2nmolNO2②混合气体的颜色不再改变③混合气体的密度不再改变的状态④混合气体的平均相对分子质量不再改变的状态 A.①②③ B.①②④ C.①③④ D.②③④ |
|
| 13. 选择题 | 详细信息 |
NO氧化反应:2NO(g)+O2(g)⇌2NO2(g) ΔH,该反应分两步进行,其反应过程能量变化示意图如图,下列说法不正确的是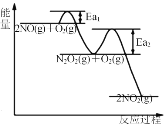 Ⅰ 2NO(g)⇌N2O2(g) ΔH1 Ⅱ N2O2(g)+O2(g)⇌2NO2(g) ΔH2 A.因Ea1<Ea2,所以决定NO氧化反应速率快慢的是反应Ⅱ B.由图可知,0>ΔH1>ΔH2,ΔH1+ΔH2=ΔH C.反应过程中,c(N2O2)先增大后减小 D.2NO(g)+O2(g)⇌2NO2(g) 两步反应过程中都是反应物断键吸收能量大于生成物成键释放的能量 |
|
| 14. 选择题 | 详细信息 | ||||||||
在
|
|||||||||
| 15. 选择题 | 详细信息 |
|
对于可逆反应:2A(g)+B(g) A. 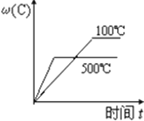 B. B.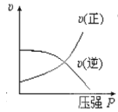 C. 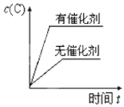 D. D.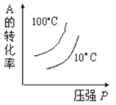 |
|
| 16. 选择题 | 详细信息 |
|
将1mol N2O5置于2L密闭容器中,在一定温度下发生下列反应:①2N2O5(g) A.3.2 B.0.2 C.1/180 D.4/45 |
|
| 17. 选择题 | 详细信息 | ||||
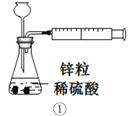
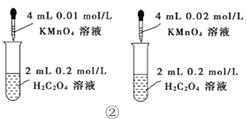
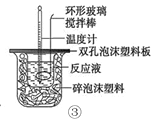
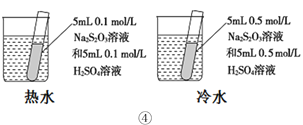
下列装置或操作能达到目的的是
|
|||||
| 18. 选择题 | 详细信息 |
合成导电高分子材料PPV的反应:n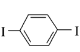 +n +n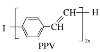 +(2n-1)HI,下列说法正确的是( ) +(2n-1)HI,下列说法正确的是( )A.合成PPV的反应为缩聚反应 B.PPV与聚苯乙烯具有相同的重复结构单元 C.  和苯乙烯互为同系物 和苯乙烯互为同系物D.通过质谱法测定PPV的平均相对分子质量,可得其聚合度 |
|
| 19. 选择题 | 详细信息 |
从中草药中提取的一种有机物A(结构简式如下图)可用于治疗多种疾病。下列关于有机物A的说法正确的是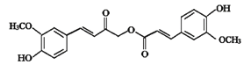 A.有机物A分子中共有四种含氧官能团 B.其碱性水解的产物均可与Na2CO3溶液反应 C.1mol该分子最多与9molH2发生加成反应 D.苯环上氢原子发生氯代时,一氯代物有3种 |
|
| 20. 选择题 | 详细信息 |
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)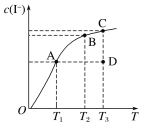 A.该反应ΔH<0 B.若在T1、T2温度下,反应的平衡常数分别为K1、K2,则K1<K2 C.若反应进行到状态D时,一定有v正>v逆 D.状态A与状态B相比,状态A的c( |
|
| 21. 选择题 | 详细信息 |
如图所示,三个烧瓶中分别充满NO2气体并分别装在盛有水的三个烧杯中,在①烧杯中加入CaO,在②烧杯中不加其他任何物质,在③烧杯中加入NH4Cl晶体,发现①中红棕色变深,③中红棕色变浅。已知:2NO2(红棕色)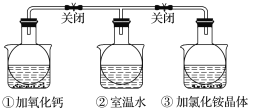 A.2NO2 B.NH4Cl溶于水时吸收热量 C.①烧瓶中平衡混合气的平均相对分子质量增大 D.③烧瓶中气体的压强增大 |
|
| 22. 选择题 | 详细信息 |
|
5mL0.01mol·L−1KI溶液与1mL0.01mol·L−1CuCl2溶液发生反应:2Cu2+(aq)+4I−(aq) A.加入苯,振荡,平衡正向移动 B.过滤,滤液经苯2次萃取分离后,在水溶液中加入适量浓氨水出现蓝色沉淀,表明该化学反应存在限度 C.该反应的平衡常数 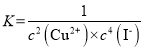 D.往平衡体系中加水稀释,平衡正向移动 |
|
| 23. 综合题 | 详细信息 |
酯类物质H是一种疗效明显的血管扩张剂,以烃A、E为原料合成H的流程如下: 已知:RCHCl2 (1)C的名称是____,①的反应类型是___。D中含有官能团的名称是____。 (2)E的结构简式可能为___,H的分子式为____。 (3)写出反应④的化学方程式:__________。 (4)写出符合下列条件的D的同分异构体的结构简式(同一碳原子上不能连2个—OH):______(写一种即可)。 ①能发生银镜反应但不能发生水解 ②核磁共振氢谱峰面积比为2 :2 :2 :1 :1 ③遇FeCl3溶液显紫色 (5)以1—丙醇为原料合成2—丁烯酸,写出合成路线图:_______(无机试剂任选)。 |
|
| 24. | 详细信息 | ||||||||||||||||||||||||||
|
氢气还原NO的反应为 (1) (2)已知几种共价键的键能如下:
根据上述数据计算,NO的键能a=___________。
① |
|||||||||||||||||||||||||||
| 25. 填空题 | 详细信息 |
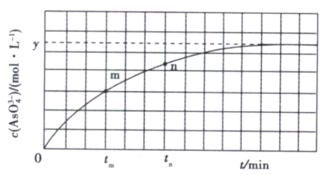 (1)下列可判断反应达到平衡的是_________(填标号)。 a.溶液的pH不再变化 b. c. d. (2) (3) (4)若平衡时 |
|
| 26. 实验题 | 详细信息 |
|
工业上乙醚可用于制造无烟火药。实验室合成乙醚的原理如下: 主反应:2CH3CH2OH 副反应:CH3CH2OH (乙醚的制备)实验装置如图所示(夹持装置和加热装置略) 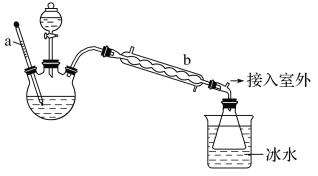  (1)仪器a是___________(写名称);仪器b应更换为下列的___________(填字母)。 A.干燥器 B.直形冷凝管 C.玻璃管 D.安全瓶 (2)实验操作的正确排序为___________(填字母),取出乙醚后立即密闭保存。 a.组装实验仪器b.加入12mL浓硫酸和少量乙醇的混合物c.检查装置气密性d.熄灭酒精灯e.先通冷却水后加热烧瓶f.拆除装置g.控制滴加乙醇的速率与产物馏出的速率相等 (3)加热后发现烧瓶中没有添加碎瓷片,处理方法是___________。反应温度不超过140℃,其目的是___________。若滴入乙醇的速率显著超过产物馏出的速率,则反应速率会降低,可能的原因是___________。 |
|