遵义市2019年高二上册化学月考测验完整试卷
| 1. 选择题 | 详细信息 |
|
关于离子化合物NH5(H有正价和负价)下列说法正确的是( ) A.N为+5价 B.阴阳离子个数比是1:1 C.阴离子为8电子稳定结构 D.阳离子的电子数为11 |
|
| 2. 选择题 | 详细信息 |
|
已知反应式:mX(g)+nY(?) A.反应向逆方向移动 B.Y可能是固体或液体 C.系数n>m D.Z的体积分数减小 |
|
| 3. 选择题 | 详细信息 |
|
用标准盐酸溶液滴定未知浓度的氢氧化钠溶液,用甲基橙作指示剂,下列说法正确的是( ) A.可以用石蕊代替指示剂 B.滴定前用待测液润洗锥形瓶 C.若氢氧化钠吸收少量CO2,不影响滴定结果 D.当锥形瓶内溶液由橙色变为红色,且半分钟内不褪色,即达到滴定终点 |
|
| 4. 选择题 | 详细信息 |
将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是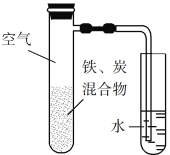 A. 铁被氧化的电极反应式为Fe−3e− B. 铁腐蚀过程中化学能全部转化为电能 C. 活性炭的存在会加速铁的腐蚀 D. 以水代替NaCl溶液,铁不能发生吸氧腐蚀 |
|
| 5. 选择题 | 详细信息 |
绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是 A. 图中a和b分别为T1、T2温度下CdS在水中的溶解度 B. 图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q) C. 向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动 D. 温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动 |
|
| 6. 选择题 | 详细信息 |
|
室温下,取20 mL 0.1 mol·L−1某二元酸H2A,滴加0.1 mol·L−1 NaOH溶液。已知:H2AH++HA−,HA−⇌H++A2−。下列说法不正确的是 A. 0.1 mol·L−1 H2A溶液中有c(H+)-c(OH−)-c(A2−)=0.1 mol·L−1 B. 当滴加至中性时,溶液中c(Na+)=c(HA−)+2c(A2−),用去NaOH溶液的体积小于10 mL C. 当用去NaOH溶液体积10 mL时,溶液的pH<7,此时溶液中有c(A2−)=c(H+)-c(OH−) D. 当用去NaOH溶液体积20 mL时,此时溶液中有c(Na+)=2c(HA−)+2c(A2−) |
|
| 7. | 详细信息 |
多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。 回答下列问题: Ⅰ.硅粉与 Ⅱ.将 ① ② ③ (1)氢化过程中所需的高纯度 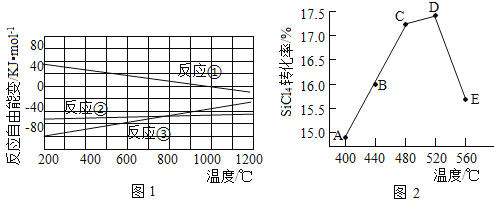 (2)已知体系自由能变 (3)不同温度下反应②中 a.B点: (4)反应③的 (5)由粗硅制备多晶硅过程中循环使用的物质除 |
|
| 8. 解答题 | 详细信息 |
|
偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:(CH3)2NNH2(l)+2N2O4(l)= 2CO2(g)+3N2(g)+4H2O(g) (Ⅰ) (1)反应(Ⅰ)中氧化剂是___________。 (2)火箭残骸中常现红棕色气体,原因为:N2O4(g)⇌2NO2(g) (Ⅱ)当温度升高时,气体颜色变深,则反应(Ⅱ)为______(填“吸热”或“放热”)反应。 (3)一定温度下,反应(Ⅱ)的焓变为△H。现将1mol N2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是_________。若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数______(填“增大”“不变”或“减小”)。 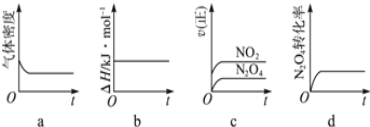 (4)NO2可用氨水吸收生成NH4NO3 。25℃时,将a mol NH4NO3溶于水,溶液显酸性,原因是______________(用离子方程式表示)。向该溶液滴加b L 氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将________(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为_______mol•L﹣1 。(NH3•H2O的电离平衡常数取Kb=2×10﹣5mol•L﹣1) |
|
| 9. 综合题 | 详细信息 |
|
无水三氯化铁易升华,有强烈的吸水性,是一种用途比较广泛的盐。 (1)实验室中可将FeCl3溶液_____________________、_______________________、过滤、洗涤干燥得FeCl3·6H2O;再______________________________,得到无水FeCl3。 (2)室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH为2.7时,Fe3+开始沉淀;当溶液pH为4时,c(Fe3+)=______mol·L-1(已知:Ksp[Fe(OH)3]= 1.1×10-36)。 (3)利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3·5H2O]的实验流程如下图所示:  ①为抑制FeCl3水解,溶液X为______________。 ②所得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是____________________________。 ③为测定所得草酸铁晶体的纯度,实验室称取ag样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于下图所示仪器_________(填“甲”或“乙”)中;下列情况会造成实验测得Fe2(C2O4)3·5H2O含量偏低的是___________。  a.盛放KMnO4的滴定管水洗后未用标准液润洗 b.滴定管滴定前尖嘴部分有气泡,滴定后消失 c.滴定前仰视读数,滴定后俯视读数 |
|
| 10. 综合题 | 详细信息 |
|
水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题: (1)Shibata曾做过下列实验:①使纯H2缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴(Co),平衡后气体中H2的物质的量分数为0.0250。 ②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO_________H2(填“大于”或“小于”)。 (2)721 ℃时,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H2的物质的量分数为_________(填标号)。 A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50 (3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用  可知水煤气变换的ΔH________0(填“大于”“等于”或“小于”),该历程中最大能垒(活化能)E正=_________eV,写出该步骤的化学方程式_______________________。 |
|
最近更新



