2019届高三下半期4月第二次模拟考试理科综合化学考试(湖南省怀化市)
| 1. | 详细信息 |
|
化学与生产生活密切相关,下列说法不正确的是 A. “卤水点豆腐”运用了胶体电泳的性质 B. C. NaCl既可以做调味品,也可以做食品防腐剂 D. 清乾隆“瓷母”是指各种釉彩大瓶,它们的主要成分是硅酸盐 |
|
| 2. | 详细信息 |
|
下列说法正确的是 A. 0.1molFe溶于硝酸,电子转移数目一定为0.3 B. 标准状况下,14.4g正戊烷( C. 18g重水( D. 12g熔融 |
|
| 3. | 详细信息 |
根据下图(其他产物未写出)分析,下列说法正确的是 A. A和B生成C的反应为加成反应 B. C中所有原子可能在同一平面 C. B的分子式为 D. C苯环上的二氯代物只有两种 |
|
| 4. | 详细信息 |
短周期元素T、X、Y、Z、W在元素周期表中的相对位置如下表所示,其中T的单质在一定条件下能与W的最高价氧化物对应水化物的浓溶液反应并生成两种酸性气体,则下列相关说法正确的是 A. 离子半径:X<Y<W B. 最简单气态氢化物的热稳定性:W<Z C. D. 最高价氧化物对应水化物的碱性:X<Y |
|
| 5. | 详细信息 |
|
下列实验能达到预期目的的 A. 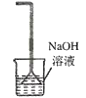 吸收HCl尾气 吸收HCl尾气B.  进行喷泉实验 进行喷泉实验C. 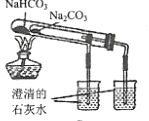 比较 比较D. 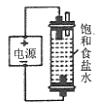 制少量NaClO为主要成分的消毒液 制少量NaClO为主要成分的消毒液 |
|
| 6. | 详细信息 |
锂锰电池结构如图所示,其中电解质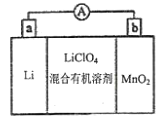 A. 外电路电流方向:a→b B. 电池正极反应式为: C. 可以用水代替电池中的混合有机溶剂 D. 用该电池给铅蓄电池充电,a极与Pb电极相连 |
|
| 7. | 详细信息 |
常温下,将 A. B. 在0≤pH≤5时, C. 分别往M、N两点对应溶液中滴加1 mo/L NaOH溶液至恰好完全反应,消耗NaOH溶液的体积相等 D. 常温下,浓度均为0.1 mo/L的 |
|
| 8. | 详细信息 |
某研究性学习小组利用下图装置探究草酸钙晶体(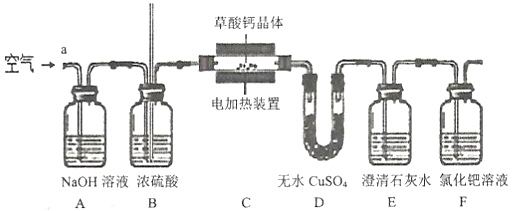 (1)A的作用是____________________;D中可观察到的现象是_________________。 (2)B中长玻璃管的作用是______________________________________________。 (3)E、F位置___________(填“能”或“不能”)互换,理由是________________________________。 (4)写出 (5)为探究草酸钙晶体加热分解产物的成份并测x,进行如下实验: ①按上图连接好仪器,______________________________(填实验操作名称)。 ②将29.2g草酸钙晶体放入C中,从a处通入一段时间空气。 ③加热草酸钙晶体直到质量不再减少,从a处一直通空气直至冷却。 ④测得C中残留固体质量11.2g,D增重3.6g,E增重8.8g(澄清石灰水足量)。 ⑤数据处理:计算可得x=_______________;写出上述实验中草酸钙晶体受热分解的化学方程式________________________________________________。 |
|
| 9. | 详细信息 | ||||||||||
镓是制作高性能半导体的重要原料。工业上常从锌矿冶炼的废渣中回收镓。已知某锌矿渣主要含Zn、Si、Pb、Fe、Ga的氧化物,利用该矿渣制镓的工艺流程如下: 已知:①镓在元素周期表中位于第四周期第ⅢA,化学性质与铝相似。 ②lg2=0.3,lg3=0.48。 ③部分物质的Ksp如F表所示
|
|||||||||||
| 10. | 详细信息 | ||||||
|
氨气是一种重要化工原料。 (1)德国化学家哈伯从1902年开始研究由氮气和氢气直接合成氨。 已知:① ②每破坏lmol有关化学键需要的能量如下表:
|
|||||||
| 11. | 详细信息 |
|
铁和铜都是日常生活中常见的金属,有着广泛的用途。请回答下列问题: (1)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于__________(填晶体类型);Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=_____________; (2) (3)某M原子的外围电子排布式为 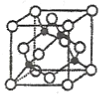 ①该晶体的化学式为__________________。 ②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于___________(填“离子”或“共价”)化合物。 ③已知该晶体的密度为 |
|
| 12. | 详细信息 |
|
口服抗菌药利君沙的制备原料E和某种广泛应用于电子电器领域的高分子化合物H的合成路线如下: 已知:  I、核磁共振氢谱显示E分子中有两组峰,且峰面积比为2:1 Ⅱ、 Ⅲ、 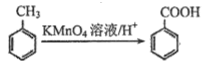 回答下列问题: (1)丙烯的结构简式为_______________;E的分子式为_____________________; (2)B分子中官能团的名称为__________________;G的名称为_______________________。 (3)由甲苯生成F的反应类型为_________________。 (4)写出C→D的化学方程式________________________________________________。 (5)满足下列条件的G的同分异构体有_________种。 ①苯环上有三个取代基。②遇 ③能和 (6)写出1,3-丁二烯( 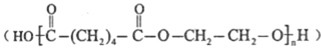 的合成路线________________(无机试剂任选)。 的合成路线________________(无机试剂任选)。 |
|