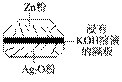2016——2017高一年级第二学期期中考试
| 1. | 详细信息 |
|
下列叙述错误的是 ( ) A.13C和14C属于同一种元素,它们互为同位素 B.1H和2H是不同的核素,它们的质子数相等 C.14 D.6Li和7Li的电子数相等,中子数也相等
|
|
| 2. | 详细信息 |
|
关于化学键的各种叙述中正确的是 A.离子化合物里一定不存在共价键 B.共价化合物里一定不存在离子键 C.非极性键只存在于双原子的单质分子里 D.由不同元素组成的多原子分子里,一定只存在极性键
|
|
| 3. | 详细信息 |
|
1 mg锎(25298Cf)每秒种能释放2.34×109个中子,其在医学上常被用作治疗恶性肿 瘤的中子源。下列有关说法错误的是 ( ) A.锎 B.1 mg锎(25298Cf)中含有2.34×109个中子 C.25298Cf原子中,质子数和核外电子数均为98 D.25298Cf的中子数与质子数之差为56
|
|
| 4. | 详细信息 | |||||||||||||||
|
下列各组材料中,能组成原电池的是( )
|
||||||||||||||||
| 5. | 详细信息 |
|
已知反应:2H2O2==2H2O+O2↑,下列条件下,反应速率最大的是( ) A.10 ℃,5 mL 3 % H2O2溶液 B.10 ℃,5 mL 5 % H2O2溶液 C.30 ℃,5 mL 5% H2O2溶液 D.30 ℃,5 mL 5 % H2O2溶液且加入少量MnO2
|
|
| 6. | 详细信息 |
|
下列措施对增大反应速率明显有效的是( ) A.Na与水反应时增大水的用量 B.Fe与稀硫酸反应制取氢气时,改用浓硫酸 C.在K2SO4与BaCl2两溶液反应时,增大压强 D.将铝片改为铝粉,做铝与氧气反应的实验
|
|
| 7. | 详细信息 |
|
下列描述的化学反应状态,不一定是平衡状态的是( ) A.H2(g)+Br2(g) 恒温、恒容下,反应体系中气体的颜色保持不变 B.2NO2(g) 恒温、恒容下,反应体系中气体的压强保持不变 C.CaCO3(s) 恒温、恒容下,反应体系中气体的密度保持不变 D.3H2(g)+N2(g) 反应体系中H2与N2的物质的量之比保持3∶1
|
|
| 8. | 详细信息 |
|
在密闭容器中进 A.c(Z)=0.5 mol·L-1 B.c(Y2)=0.5 mol·L-1 C.c(X2)=0.2 mol·L-1 D.c(Y2)=0.6 mol·L-1
|
|
| 9. | 详细信息 |
|
“在3支大小相同的试管中各加入2 mL 5%的H2O2溶液,再向其中2支试管中分别加入少量MnO2粉末、2滴1 mol/L FeCl3溶液。对比观察现象。”该实验的目的是( ) A.探究浓度对反应速率的影响 B.探究温度对反应速率的影响 C.探究固体表面积对反应速率的影响 D.探究催化剂对反应速率的影响
|
|
| 10. | 详细信息 |
|
反应C(s)+H2O(g) ①增加C的量 ②将容器的体积减小一半 ③保持体积不变,充入氮气使体系的压强增大 ④保持压强不变,充入氮气使体系的体积增大 A.①② B.②③ C.①③ D.③④
|
|
| 11. | 详细信息 |
|
对于可逆反应M + 3N A.M、N、Q三种物质的浓度一定相等 B.M、N全部变成了Q C.反应混合物各组分的浓度不再变化 D.反应已经停止
|
|
| 12. | 详细信息 |
|
氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1 mol氢气中的化学键消耗的能量为Q1 kJ,破坏1 mol氯气中的化学键消耗的能量为Q2 kJ,形成1 mol氯化氢中的化学键释放的能量为Q3 kJ。下列关系式中,正确的是( ) A.Q1+Q2>Q3 B.Q1+Q2>2Q3 C.Q1+Q2<Q3 D.Q1+Q2<2Q3
|
|
| 13. | 详细信息 |
|
下列有关性质的比较,不能用元素周期律解释的是( ) A.酸性:H2SO4>H3PO4 B.非金属性:Cl>Br C.碱性:NaOH>Mg(OH)2 D.热稳定性:Na2CO3>NaHCO3
|
|
| 14. | 详细信息 |
|
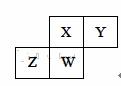
短周期元素X、Y、Z、W在元索周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )
A.原子半径:W>Z>Y>X B.最高价氧化物对应水化物的酸性:X>W>Z C.最简单气态氢化物的热稳定性:Y>X>W>Z
|
|
| 15. | 详细信息 |
|
下列说法正确的是( ) A.热稳定性:H2O>H2S>HF B.微粒X2﹣和Y2+的核外电子排布相同,离子半径:X2﹣<Y2+ C.第3周期金属都能与氯气发生化合反应 D.第IVA族元素的氧化物都能与NaOH溶液反应生成盐和水
|
|
| 16. | 详细信息 |
|
依据下列说法来判断相应元素的金属性、非金属性强弱,不合理的是( ) A.卤素单质Cl2、B B.气态氢化物NH3 C.碱金属单质Li、Na、K与水反应的剧烈程度 D.1mol Na、Mg、Al分别与足量盐酸反应时失电子数的多少
|
|
| 17. | 详细信息 |
|
A、B、C、D为四种短周期元素,已知A、C同主族,B、C、D同周期:A的气态氢化物比C的气态氢化物稳定; B的阳离子比D的阳离子氧化性强;B的阳离子比C的阴离子少一个电子层.下列叙述正确的是( ) A.原子序数:A>C>B>D B.单质熔点:D>B,A>C C.原子半径:D>B>C>A D.简单离子半径:D>B>C>A
|
|
| 18. | 详细信息 |
|
对于反应Zn(s)+H2SO4(aq)===ZnSO4(aq)+H2(g),下列叙述不正确的是( )
A.其反应物或生成物都能用来表示该反应的速率 B.反应过程中能量关系可用上图表示 C.若将该反应设计成原电池,锌为负极 D.若设计为原电池,当有32.5 g锌溶解时,正极放出标准状况下11.2 L气体
|
|
| 19. | 详细信息 |
|
最新报道:科学家首次用X射线激光技术观察到CO与O
下列说法正确的是( ) A.CO和O生成CO2是吸热反应 B.在该过程中,CO断键形成C和O C.CO和O形成了具有极性共价键的CO2 D.状态 Ⅰ→状态 Ⅲ 表示CO与O2反应的过程
|
|
| 20. | 详细信息 |
|
下列说法正确的是( ) A.化学反应速率是对可逆反应而言的,非可逆反应不谈化学反应速率 B.在可逆反应中,正反应的化学反应速率是正值,逆反应的化学反应速率是负值 C.同一化学反应中,化学反应速率可用反应物浓度的改变表示,也可用生成物浓度的改变表示,其值可能相同,也可能不同 D.化学反应速率的单位通常是g·L-1·s-
|
|
| 21. | 详细信息 |
|
微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电
根据上述反应式,完成下列题目。 (1)判断下列叙述中正确的是________。 A.在使用过程中,电解质KOH不断被消耗 B.使用过程中,电子由Ag2O极经外电路流向Zn极 C.Zn是负极,Ag2O是正极 D.Zn电极发生还原反应,Ag2O电极发生氧化反应 (2)写出电池的总反 (3)使用时,负极区的c(OH-)_____
|
|
| 22. | 详细信息 |
|
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) (1)用物质A表示反应的平均速率为________。 (2)用物质B表示反应的平均速率为________。 (3)2 s时物质A的转化率为________。 (4)2 s时物质B的体积分数为________。
|
|
| 23. | 详细信息 |
|
现有A、B、C、D、E五种元素,它们的质子数依次增多。①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;③C+比B3+多8个电子;④C与D元素可以形成化合物CD;⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;⑥在周期表中E处于C的下两个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为2∶1。试回答: (1)B是________(写元素符号,下同),E是________。 (2)B的离子结构示意图________,D的单质分子的电子式________,C元素最高价氧化物对应的水化物的电子式________。 (3)用电子式表示H2A形成过程:___________________。 (4)写出CD的溶液中通入氯气反应的离子方程式: ______________________________________。 (5)比较B、C、E三种元素形成的简单离子氧化性的强弱:______________(B、C、E离子用实际离子符号表示)。
|
|
- 2017-2018年高二上学期第三次月考化学考卷带参考答案和解析(江西省南昌市第二中学)
- 高中化学人教版 必修1 第三章 金属及其化合物 2.几种重要的金属化合物 铁的重要化合物
- 黄金30题系列 高二化学 小题好拿分
- 2016-2017年高一下半期理综化学开学考试(安徽师大附中)
- 高中化学人教版 必修2 第四章 化学与自然资源的开发利用 第一节 开发利用金属矿物和海水资源 海水资源的开发利用
- 2017-2018年高二12月联考化学考试题(河南省豫北重点中学)
- 2016-2017年高一下半年化学开学考试专题训练(广西省桂林市第十八中学)
- 高中化学人教版 选修四 第三章 水溶液中的离子反应 第二节 水的电离和溶液的酸碱性 水的电离和溶液的酸碱性第二课时