2018高三上学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
下列物质中属于含有极性共价键的离子化合物的是 ( ) A.过氧化钠 B.碘化氢 C.苛性钠 D.氯化钾
|
|
| 2. | 详细信息 |
|
下列有关生活中化学的叙述,错误的是 ( ) A.向燃料煤中加入生石灰,可以减少对大气的污染B.用双氧水清洗伤口,可以杀菌消毒 C.只用淀粉溶液就能检验出食盐中是否加碘D.随意丢弃废旧电池,会对环境造成污染
|
|
| 3. | 详细信息 |
|
下列有关性质的比较中,正确的是 ( ) A.热稳定性:H2S>HCl>HBr>HI B.熔点:Na2O >MgO>CaO C.微粒半径:F-<Na+<Mg2+ D.还原性:H2S>HCl >HF
|
|
| 4. | 详细信息 |
|
在50 mL FeCl3和CuCl2的混合溶液中,FeCl3和CuCl2的浓度均为1 mol/L,在混合溶液中加入100 mL NaOH溶液,恰好完全反应,则该NaOH溶液的浓度为 ( ) A.0.5mol/L B.1mol/L C.1.25mol/L D.2.5mol/L
|
|
| 5. | 详细信息 |
|
在化学实验室进行下列实验操作时,其操作或记录的数据正确的是 ( ) A.用托盘天平称取8.84g食 B.用250mL的容量瓶配制所需的280mL、0.10mol/L的NaOH溶液 C.用量筒量取12.12mL的盐酸 D.用0.12mol/L盐酸滴定未知浓度的NaOH溶液,消耗盐酸21.40mL
|
|
| 6. | 详细信息 |
|
用NA代表阿伏加德罗常数,下列说法正确的是: ( ) A.0.5mol Al与足量盐酸反应转移电子数为1NA B.标准状况下,11.2L SO3所含的分子数为0.5NA C.0.1molCH4所含的电子数为1NA D.46g NO2和N2O4的混合物所含的分子数为1NA
|
|
| 7. | 详细信息 |
|
同温同压下,对于等体积的一氧化氮(14N18O)和一氧化碳(13C18O)气体,下列说法正确的是: ( ) A.含相同的分子数和原子数 B.含相同的分子数和电子数 C.含相同的质子数和中子数 D.所含分子数和质量均不相同
|
|
| 8. | 详细信息 |
|
在一定温度下,已知有关某饱和溶液的一些数据:①溶液的质量,②溶剂的质量,③溶液的体积,④溶质的摩尔质量,⑤溶质的溶解度,⑥溶液的密度.利用下列各组数据计算该饱和溶液的物质的量浓度,不能算出的一组 ( ) A.④⑤⑥ B.①②③④ C.①④⑥ D.①③④⑤
|
|
| 9. | 详细信息 |
|
下列离子方程式书写正确的是: ( ) A.用铂电极电解氯化镁溶液:Cl-+2H2O B.NaHSO4溶液中滴入Ba(OH)2溶液至中性:H++SO42-+Ba2+十OH-===BaSO4↓+H2O C.在H2O2中加入酸性KMnO4溶液:2MnO4-+5H2O2+6H+====2Mn2+ +5O2↑+8H2O D.溴乙烷与6mol/L氢氧化钠水溶液共热:C2H5Br +OH-
|
|
| 10. | 详细信息 |
|
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是 A.电解饱和食盐水时,阳极的电极反应式为:2Cl - -2e -==Cl2 ↑ B.氢氧燃料电池的负极反应式:O2 + 2H2O + 4e- == 4OH - C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e- == Cu2+ D.钢铁发生电化学腐蚀的正极反应式:Fe-2e - == Fe2+
|
|
| 11. | 详细信息 |
|
用惰性电极实现电解,下列说法正确的是: A、电解稀硫酸溶液,实质上是电解水,故溶液pH不变; B、电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小; C、电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1:2; D、电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1;
|
|
| 12. | 详细信息 |
|
下列有机物是按照碳的骨架进行分类的是 A.烷烃 B.烯烃 C.芳香烃 D.卤代烃
|
|
| 13. | 详细信息 |
|
下列关于官能团的判断中说法错误的是 A.醇的官能团是羟基(-OH) B.羧酸的官能团是羟基(-OH) C.酚的官能团是羟基(-OH) D.烯烃的官能团是双键
|
|
| 14. | 详细信息 |
|
下列烷烃中可能存在同分异构体的是 A.甲烷 B.乙烷 C.丙烷 D.丁
|
|
| 15. | 详细信息 |
|
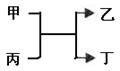
甲、乙为短周期同一主族元素组成的单质,丙、丁为含氧化合物,它们存在如下转化关系:满足条件的甲和乙分别为 ( ) A.铝和铁 B.氯气和溴 C.铝和氢气 D.钠和氢气
|
|
| 16. | 详细信息 |
|
常温下,下列各组离子在给定条件下一定能大量共存的是 ( ) A.在pH=0的溶液中:I-、Ca2+、NO3-、NH4+ B.存在大量Fe2+的溶液:SCN-、Na+、NO3-、SO42- C.在由水电离出的c(OH-)=10-13mol·L-1的溶液中:ClO-、Na+、SO32-、Cl- D.在c(OH-)=1.0ⅹ10-13 mol·L-1的溶液中:Na+、S2-、AlO2-、SO32-
|
|
| 17. | 详细信息 | ||
|
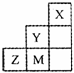
图为短周期的一部分,推断关于Y、Z、M的说法正确的是 ( ) B.原子半径:M>Z>Y C.气态氢化物的稳定性:Y<M<Z D.ZM2分子中各原子的最外层电子均满足8e—稳定结构
|
|||
| 18. | 详细信息 |
|
将磁性氧化铁放入稀HNO3中可发生如下反应:3Fe3O4+ 28HNO3=9Fe (NO3)x+ NO↑+14H2O 。下列判断合理的是 ( ) A.Fe (NO3)x中的x为2 B.反应中每生成0.2 mol 还原产物,就有0.6 mol 电子转移 C.稀HNO3 在反应中只作氧化剂 D.磁性氧化铁中的铁元素全部被氧化
|
|
| 19. | 详细信息 |
|
下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。
下列说法中不正确的是( ) A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4 B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3 C.B和Cl2的反应是氧化还原反应 D.当X是强酸时,C在常温下是气态单质
|
|
| 20. | 详细信息 |
|
铅笔是常用的学习用品,铅笔芯的主要成分是石墨和黏土。某型号的铅笔芯质量的一半成分是石墨,用该铅笔写一个化学方程式消耗铅笔芯的质量约1mg,那么铅笔芯中减少的碳原子数约为 ( ) A.2.5×1019个 B.2.5×1022个 C.5×1019个 D.5×1022个
|
|
| 21. | 详细信息 |
|
某一反应体系中的物质有:HCl、SnCl2、H2SnCl6、As、H3AsO3、H2O, 已知:As是产物之一。 (1)写出并配平该反应的化学方程式 ; (2)在该反应中,得电子的物质是 ,被氧化的元素是 ; (3)在反应中,每转移1 mol电子,消耗(或生成)HCl mol; (4)下列叙述正确的是 (填写序号)。 a.在相同条件下,第VIIA族元素的阴离子的还原性从上到下逐渐增强 b.Sn和Pb位于同一主族,其+4价的化合物均很稳定 c.在相同条件下,还原性顺序:S2->I->Fe2+>Br->Cl-
|
|
| 22. | 详细信息 |
|
某无色透明溶液可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-,取该溶液进行如下实验: ① 用蓝色石蕊试纸检测该溶液,试纸显红色; ② 取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色; ③ 取溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失; ④ 取溶液少许,滴入氯化钡溶液产生白色沉淀; ⑤ 取实验 ④ 后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。 请回答下列问题: ⑴用简要语言描述在实验 ① 中的操作 ⑵根据上述实验判断原溶液中肯定存在的离子是______,肯定不存在的离子是_____。 ⑶写出与②③两个实验有关的离子方程式: ②___________________________ ③_________________________
|
|
| 23. | 详细信息 |
|
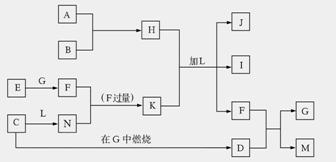
下图每一方框中的字母代表一种反应物或生成物,它们都是中学化学中常见的物质。产物J是含A金属元素的胶状白色沉淀,I为NaCl溶液,L是水,D是淡黄色固体,E为单质。
试填写下列空白: (1)写出F的化学式: _______________。 (2)写出M发生水解的化学反应方程式__________________。 (3)反应C+G→D的化学方程式是_______________。 (4)写出H 、K加L生成J、I、F反应的离子方程式_______________。
|
|
| 24. | 详细信息 |
|
某种含有少量FeCl2杂质的FeCl3样品,现要测定其中铁元素的含量。实验采用以下步骤进行: ① 准确称量m g样品(2~3g); ② 向样品中加入10mL 5mol/L的盐酸,再加入蒸馏水,配制成250mL溶液; ③ 量取25mL操作②中配得的溶液,加入3mL溴水,加热使之完全反应; ④ 趁热迅速加入浓度为10%的氨水至过量,充分搅拌,使之完全沉淀; ⑤ 过滤,将沉淀洗涤、灼烧、冷却称量,反复操作至恒重。 请根据上面的叙述回答: (1)若称量前,托盘天平的指针偏向标尺左方;称量读数时,指针刚好在标尺的中间,则所得样品的质量 。 A、比mg多 B、比mg少 C、恰好为mg (2)溶解样品时要加入盐酸,原因是 。 (3)配制250mL溶液时,除需250mL的容量瓶、烧杯外,还需用到的玻璃仪器 是 。 (4)加入溴水时发生反应的离子方程式是 。 (5)若坩埚质量为W1 g,坩埚与灼烧后固体的总质量是W2 g,则样品中铁元素的质量分数是 。 (6)若在配制250mL溶液时,所用的容量瓶没有洗干净。当含有下列物质时,最终会使铁元素的测定含量(填“偏高”、“偏低”或“不变”)。 ①NaCl ②Fe2(SO4)3
|
|