2020吉林人教版初中化学中考真题
| 1. | 详细信息 |
|
人类每时每刻都离不开空气,其中能供给呼吸的是 A. 氮气 B. 氧气 C. 稀有气体 D. 二氧化碳
|
|
| 2. | 详细信息 |
|
我国古代科技发展成果卓著,下列成果的应用中只发生物理变化的是() A. 司南指示方向 B. 高温烧制陶瓷 C. 古代湿法炼铜 D. 谷物酿造美酒
|
|
| 3. | 详细信息 |
|
物质是由微观粒子构成的,下列物质由原子直接构成的是() A. 金刚石 B. 水蒸气 C. 氯化钠 D. 碳酸钠
|
|
| 4. | 详细信息 |
|
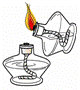
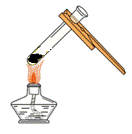
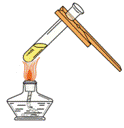
下列酒精灯的使用正确的是 A. 点燃酒精灯 B. 给固体加热 C. 给液体加热 D. 熄灭酒精灯
|
|
| 5. | 详细信息 |
|
黑火药是中国四大发明之一,其主要反应为 A. X的化学式为2N B. 该反应属于复分解反应 C. 该反应前后各元素的化合价均未改变 D. 参加反应的碳、硫质量比为9:8
|
|
| 6. | 详细信息 |
|
材料、能源、环境、健康等方面问题的解决离不开化学的发展,下列说法错误的是() A. 塑料、合成纤维、合成橡胶都属于合成材料 B. 煤、石油、天然气都是不可再生能源 C. CO、CO2、SO2都是污染环境的有毒气体 D. 钙、铁、锌都是人体必不可少的金属元素
|
|
| 7. | 详细信息 |
|
下列因果关系错误的是 A. 因为分子构成不同,所以水和过氧化氢的化学性质不同 B. 因为质子数不同,所以碳原子和氮原子所属的元素种类不同 C. 因为碳原子排列方式不同,所以金刚石和石墨的性质完全不同 D. 因为电子层数及最外层电子数不同,所以钠原子
|
|
| 8. | 详细信息 |
|
下列有关金属材料的说法错误的是() A. 在潮湿的空气中铁易生锈 B. 金属的回收利用是保护金属资源的有效途径之一 C. 铝和金都有很好的抗腐蚀性,是因为二者的化学性质都很稳定 D. 高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来
|
|
| 9. | 详细信息 |
|
下列探究实验能达到目的的是() A. 探究温度对分子运动速率的影响,只将少量品红加入到热水中 B. 探究三种金属的活动性强弱,只将Fe、Cu、Ag分别加入到稀盐酸中 C. 探究MnO2是否是H2O2分解的催化剂,比较MnO2加到H2O2溶液前后产生气泡快慢 D. 探究吸入空气和呼出气体中O2含量不同,将燃着的木条分别伸入等体积两种气体中
|
|
| 10. | 详细信息 | |||||||||||||||
|
下列实验方案合理的是()
A. A B. B C. C D. D
|
||||||||||||||||
| 11. | 详细信息 |
|
用化学用语回答下列问题: (1)碳原子:________________________。 (2)两个钾离子________________________。 (3)氧气________________________。
|
|
| 12. | 详细信息 |
|
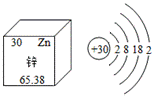
锌相对原子质量的国际新标准由张青莲教授主持测定。根据下图,回答下列问题:
(2)锌元素属于____________(选填“金属”或“非金属”)元素; (3)锌原子在化学反应中容易__________(选填“得到”或“失去”)电子。
|
|
| 13. | 详细信息 |
|
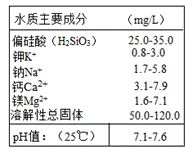
如图是某矿泉水标签的部分内容,根据标签回答下列问题:
(2)H2SiO3中Si的化合价为___________; (3)标签上共列举了__________种金属阳离子; (4)该矿泉水呈___________(选填“酸性”、“碱性”或“中性”)。
|
|
| 14. | 详细信息 |
|
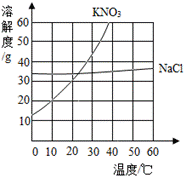
根据KNO3和NaCl的溶解度曲线,回答下列问题:
(2)根据溶解度曲线分析,从海水中获得粗盐不采用降温结晶方法的原因是__________________。 (3)下列说法正确的是______________。 A 将不饱和的KNO3溶液变为饱和,可采用加KNO3的方法 B 20℃时,KNO3和NaC1两种饱和溶液中,所含溶质质量NaCl大于KNO3 C 30℃时,溶质质量分数为20%的KNO3溶液甲,降温至20℃得到溶液乙,再降温至10℃得到溶液丙,三种溶液中溶质的质量分数大小关系:甲=乙>丙
|
|
| 15. | 详细信息 |
|
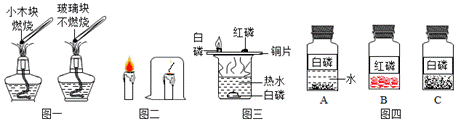
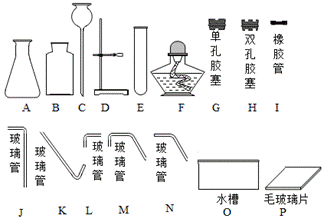
火的利用推动了人类文明的进程,观察下图:
选择序号回答(1)~(3):①与氧气接触②温度达到着火点③有可燃物 (1)图一所示实验现象,说明燃烧应具备的条件是__________________。 (2)图二烧杯中蜡烛渐渐熄灭,说明燃烧应具备的条件是__________________。 (3)图三铜片上白磷燃烧红磷不燃烧,说眀燃烧应具备的条件是__________________。 (4)图三实验中所用药品的保存方法正确的是_________________(选填图四中的字母编号)。
|
|
| 16. | 详细信息 |
|
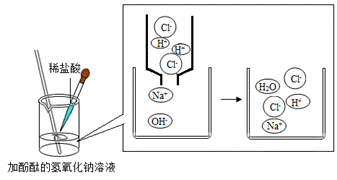
根据下图回答问题:
(2)反应中,数目减少的离子是_____________(填离子符号); (3)验证反应后溶液中稀盐酸有剩余,下列操作可行的是______________。 A 取样,加入CuO粉末 B 取样,滴加NaOH溶液 C 取样,加入CaCO3粉末 D 取样,滴加AgNO3溶液
|
|
| 17. | 详细信息 |
|
某实验小组用6%的氯化钠溶液(密度约为1.04g/cm3)配制50g质量分数为3%的氯化钠溶液,步骤如下:①计算;②量取;③混匀;④装瓶贴标签。冋答下列问题: (1)计算需要6%的氯化钠溶液的体积是___________mL(结果取整数); (2)实验中用到的仪器有25mL的量筒、细口瓶、烧杯、____________; (3)下列实验操作会导致所配溶液中溶质的质量分数一定偏大的是________________。 A 量取6%的氯化钠溶液时仰视读数 B 向烧杯内加入液体时有液体溅出 C 混匀过程中没有使用玻璃棒搅拌 D 配制好的溶液装入未干燥的细口瓶
|
|
| 18. | 详细信息 |
|
下列实验用常用于实验室制取气体,回答下列问题:
(2)用 (3)按上述反应加热31.6g的KMnO4完全反应后,理论上剩余固体质量为______________g。
|
|
| 19. | 详细信息 |
|
小明想探究家中厨房用某种洗涤剂的成分,他将洗涤剂的粉末带到学校寻求老师的帮助。在老师指导下,小明进行了大胆的猜想与实验: 【提出问题】洗涤剂中主要含有哪些物质?
猜想一:可能含有CO 猜想二:可能含有_________, 猜想三:可能含有CO 【进行实验】实验一:取少量粉末,加水溶解得到无色溶液,滴加紫色石蕊溶液后,溶液变为_________色,说明洗涤剂的溶液显碱性。 实验二:取少量粉末,滴加足量的稀盐酸,有无色无味气体产生。将生成气体通入澄清石灰水,观察到__________,证实洗涤剂中含有CO 【查阅资料】小明查阅资料得知(1)该洗涤剂中含有Na2CO3、NaOH等; (2)Na2CO3溶液显碱性。 【小结反思】实验二中产生气体的化学方程式为____________________。 【实验验证】该洗涤剂中还含有NaOH 实验三中可选试剂:A BaCl2溶液 B Ba(OH)2溶液 C NaCl溶液 D 稀盐酸 E 石蕊溶液 F 酚酞溶液 实验三:取少量粉末,加水配成溶液,加入稍过量的___________(选填字母编号,下同),产生了白色沉淀,再加几滴____________,溶液变为红色,证实洗涤剂中还含有NaOH。 【实验结论】该洗涤剂中含有Na2CO3和NaOH。
|
|
| 20. | 详细信息 |
|
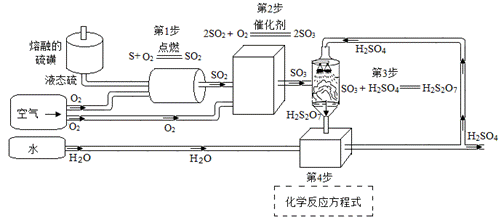
接触法生产硫酸的工艺流程如下:
回答下列问题: (1)第1步反应中将液态硫喷入反应器的目的是_____________________。 (2)写出第4步化学反应方程式_____________________。 (3)第1步至第4步流程中涉及到的物质,属于氧化物的有____________(用化学式表示); (4)若用3.2吨硫为原料,则理论上能产出98%的浓硫酸__________吨。
|
|
| 21. | 详细信息 |
|
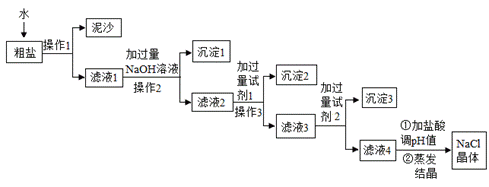
粗盐中除了含有NaCl外,还含有少量Na2SO4、CaCl2、MgCl2及泥沙等杂质。下图是常用的粗盐精制操作流程:
回答下列问题: (1)操作1相当于实验室中的____________操作; (2)沉淀1的化学式为__________________; (3)加入过量试剂1的目的是________________________; (4)滤液4中含有的阴离子是___________(填离子符号)。
|
|

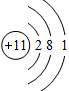 和钠离子
和钠离子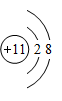 的化学性质不同
的化学性质不同