2017广东高二上学期人教版高中化学期末考试
| 1. | 详细信息 |
|
下列物质属于碱的是 A.苛性钠 B.生石灰 C.纯碱 D.胆矾
|
|
| 2. | 详细信息 |
|
在高空中有一层臭氧层,它吸收太阳光中绝大部分紫外线,使地球上的生物免受紫外线伤害。臭氧的化学式是O3,它是一种 A.混合物 B.氧化物 C.单质 D.化合物
|
|
| 3. | 详细信息 |
|
体操运动员比赛时为了防滑常在手掌上涂抹碳酸镁。碳酸镁属于 A.酸 B.碱 C.盐 D.氧化物
|
|
| 4. | 详细信息 |
|
下列物质属于纯净物的是 A.碘酒 B.漂白粉 C.氯水 D.液氯
|
|
| 5. | 详细信息 |
|
下列物质的俗称与化学式对应一致的是 A.纯碱NaOH B.硫黄SO3 C.铁红Fe2O3 D.苏打NaHCO3
|
|
| 6. | 详细信息 |
|
下列物质中,属于酸性氧化物但不溶于水的是 A. 二氧化硫 B. 二氧化氮 C.二氧化硅 D.二氧化碳
|
|
| 7. | 详细信息 |
|
2015年10月,中国中医研究员屠呦呦因发现并提取出青蒿素而获得了诺贝尔医学奖。她发现的青蒿素用以治疗疟疾,挽救了数百万患者的生命。青蒿素的分子式为C5H22O5,它属于 A.单质 B.混合物 C.无机物 D.有机物
|
|
| 8. | 详细信息 |
|
下列反应属于氧化还原反应的是 A.HCl+NaOH═NaCl+H2O B.SO3+H2O═H2SO4 C.2Na+Cl2
|
|
| 9. | 详细信息 |
|
“纳米材料”是指研究、开发出的直径从几纳米至几十纳米的材料。下列分散系中,分散质的微粒直径与“纳米材料”粒子直径大致相当的是 A.胶体 B.悬浊液 C
|
|
| 10. | 详细信息 |
|
小明体检的血液化验单中,葡萄糖为5.9mmol/L.该体检指标的物理量是 A.物质的量浓度 B.溶解度 C.质量分数 D.摩尔质量
|
|
| 11. | 详细信息 |
|
下列各选项中,二者互为同位素的是 A.40Ca和40Ar B. 16O和18O C. H2O和H2O2 D. O2和O3
|
|
| 12. | 详细信息 |
|
当光束通过下列分散系时,能观察到丁达尔效应的是 A.泥浆 B.CuSO4溶液 C.酒精溶液 D.Fe (O
|
|
| 13. | 详细信息 |
|
胶体的最本质的特征是 A.丁达尔效应 B.可以通过滤纸 C.布朗运动 D.分散质颗粒的直径在1nm~100nm之间
|
|
| 14. | 详细信息 |
|
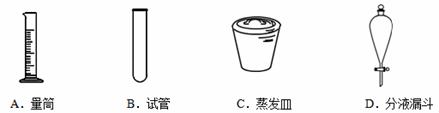
实验室中配制250mL 0.10mol•L﹣1NaOH溶液时,必须使用到的玻璃仪器是 A.锥形瓶 B.试管 C.分液漏斗 D.容量瓶
|
|
| 15. | 详细信息 |
|
下列物质中含氢原子数最多的是 A.2mol CH4 B.3mol NH3 C.4mol H2O D.6mol HCl
|
|
| 16. | 详细信息 |
|
在标准状况下,22g气体X所占体积和16g氧气所占体积相同,则X的相对分子质量是 A.22 B.44 C.28 D.88
|
|
| 17. | 详细信息 |
|
将4g NaOH 完全溶解于水配成1L的溶液,从中取出10mL,所量取的10mL溶液中NaOH的物质的量浓度为 A.1mol/L B.0.1 mol/L C.0.01 mol/L
|
|
| 18. | 详细信息 |
|
方志敏烈士生前在狱中曾用米汤(内含淀粉)给鲁迅先生写信,鲁迅先生收到信后,为了看清信中内容,可使用的化学试剂是 A.碘化钾 B.溴水 C.碘水 D.碘化钾淀粉溶液
|
|
| 19. | 详细信息 |
|
某物质经 A.可能是纯净物也可能是混合物 B.可能是单质也可能是化合物 C.一定是纯净物
|
|
| 20. | 详细信息 |
|
下列说法中正确的是 A.1mol任何气体的体积约是22.4L B.标准状况下,1mol H2O 所占的体积约为22.4L C.常温常压下,1mol O2 所占的体积约为22.4L D.标准状况下, N2 和N2O 的混合气体体积为22.4L,其中N 原子约含有2mol
|
|
| 21. | 详细信息 |
|
C60自被发现以来,已逐步应用到超导、材料等各个领域。下列有关说法正确的是 A.C60就是金刚石 B.C60属于有机化合物 C.C60的摩尔质量是720g/mol D.1mol C60完全燃烧生成22.4L CO2
|
|
| 22. | 详细信息 |
|
提出元素周期律并根据周期律编制第一个元素周期表的科学家是 A.道尔顿 B.拉瓦锡 C.门捷列夫 D.阿伏加德罗
|
|
| 23. | 详细信息 |
|
下列变化中,不存在化学键断裂的是 A.氯化氢气体溶于水 B.干冰气化 C.氯化钠固体溶于水 D.氢气在氯气中燃烧
|
|
| 24. | 详细信息 |
|
同周期的X.Y.Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是: HZO4 ①阴离子的还原性按X、Y、Z顺序减弱 ②单质的氧化性按X、Y、Z顺序增强 ③元素的原子半径按X、Y、Z顺序减小 ④气态氢化物的稳定性按X、Y、Z顺序减弱 A.①② B.②③ C.①②③ D.①②③④
|
|
| 25. | 详细信息 |
|
14C可用于考古,“14”是指 A.质量数 B.核外电子数 C.中子数 D.质子数
|
|
| 26. | 详细信息 |
|
35Cl和 35Cl- 两种微粒中,不同的是 A.核内质子数 B.核外电子层数 C.核内中子数 D.核外电子数
|
|
| 27. | 详细信息 |
|
据报道1994年12月科学家发现了一种新元素,其原子的原子核内有161个中子,质量数是272,该元素原子的质子数为 A.272 B.161 C.111 D.433
|
|
| 28. | 详细信息 |
|
20℃时,饱和KCl溶液的密度为1.174g·cm-3,物质的量浓度为4.0mol·L-1。下列说法不正确的是 A.25℃时,饱和KCl溶液的 B.此溶液中KCl的质量分数为 C.20℃时,密度小于1.174g·cm-3的KCl溶液是不饱和溶 D.将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174g·cm-3
|
|
| 29. | 详细信息 |
|
下列氧化还原反应中水既不作氧化剂又不作还原剂的是 A.H2O+CaO===Ca(OH) C.3NO2+H2O===2HNO3+NO D.2H2O
|
|
| 30. | 详细信息 |
|
下列反应中,属于吸热反应的是 A.木炭在空气中燃烧 B.氢气在氯气中燃烧 C.盐酸和氢氧化钠溶液反应 D.Ba(OH)2·8H2O与NH4C1反应
|
|
| 31. | 详细信息 |
|
下列关于 A.1L溶液中含有Na+、SO42-总数为0.3NA B.1L溶液中含有Na+数目是0.15NA C.1 L溶液中Na+的浓度是0.3 mol/L D.2 L溶液中含有SO42—的浓度是0.3mol / L
|
|
| 32. | 详细信息 |
|
实验室需要使AlCl3溶液中的Al3+离子全部 A.NaOH溶液 B.Ba(OH)2溶液 C.盐酸 D.氨水
|
|
| 33. | 详细信息 |
|
关于元素周期表的说法正确的是 A.元素周期表有8个主族 B.ⅠA族的元素全部是金属元素 C.元素周期表有7个周期
|
|
| 34. | 详细信息 |
|
已知某离子的结构示意图为 A.该元素位于第二周期第ⅡA C.该元素位于第三周期第ⅡA族 D.该元素位于第三周期0族
|
|
| 35. | 详细信息 |
|
食品的主要成分大都是有机化合物。以下食品中的有机成分属于高分子化合物的是 A.食醋中含有的醋酸 B.酒中含有的酒精 C.谷类中含有的淀粉 D.植物油、动物脂肪中含有的油脂
|
|
| 36. | 详细信息 |
|
下列物质属于离子化合物是 A.SO2 B.H2O C.NaCl D.HCl
|
|
| 37. | 详细信息 |
|
下列有关元素周期律的叙述中,正确的是 A.氧化性强弱:F2<Cl2 B.金属性强弱:K<Na C.酸性强弱:H3PO4<H2SO4 D.碱性强弱:NaOH<Mg(OH)2
|
|
| 38. | 详细信息 |
|
下列递变规律不正确的是 A.Na、Mg、Al还原性依次减弱 B.I2、Br2、Cl2氧化性依次增强 C.C、N、O原子半径依次增大 D.P、S、Cl最高正价依次升高
|
|
| 39. | 详细信息 |
|
下列化学用语表示正确的是 A.氯化钙的化学式 CaCl B.HCl分子的电子式 C.氯化钠的电子式
|
|
| 40. | 详细信息 |
|
某元素的原子核外有三个电子层,其最外层电子数是次外层电子数的一半,此元素是 A.S
|
|
| 41. | 详细信息 |
|
配制一 A.称量时,将Na2CO3固体直接放在托盘天平的右盘上 B.将Na2CO3固体在烧杯中溶解,所得溶液冷却到室温,再转移至容量瓶中 C.定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分 D.定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
|
|
| 42. | 详细信息 |
|
对于反应中的能量变化,表述正确的是 A.放热反应中,反应物的总能量大于生成物的总能量 B.氧化反应均为吸热反应 C.断开化学键的过程会放出能量 D.加热才能发生的反应一定是吸热反应
|
|
| 43. | 详细信息 |
|
|
|
| 44. | 详细信息 |
|
.某元素最高价氧化物对应水化物的化学式为HXO4,该元素的气态氢化物的化学式是 A.HX B.H2X C.XH3 D.XH4
|
|
| 45. | 详细信息 |
|
在某一化学 A.0.3 B.0.3 mol/(L·s) C.0.4 mol(L·s)-1 D.0.04 mol/L
|
|
| 46. | 详细信息 |
|
.苹果汁是人们喜爱饮料,由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色,若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有 A.氧化性 B.还原性 C.碱性 D.酸性
|
|
| 47. | 详细信息 |
|
化学与人类生活密切相关。关于下列物质的使用不合理的是 A.二氧化硫常用于食品增白 B.碳酸氢钠常用于焙制糕点 C.醋酸常用于除去水壶内的水垢 D.氢氧化铝常用于治疗胃酸过多
|
|
| 48. | 详细信息 |
|
居室空气污染的主要来源之一是人们使用的装饰材料、胶合板、内墙涂料会释放出一种刺激性气味气体。该气体是 A.甲烷 B.甲醛 C.氨气 D.二氧化硫
|
|
| 49. | 详细信息 |
|
化学与生活、社会密切相关。下列说法不正确的是 A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 B.凡含有食品添加剂的食物对人体健康均有害,不可食用 C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 D.提倡人们购物时不用塑料袋,是为了节约资源,为了防止白色污染
|
|
| 50. | 详细信息 |
|
某广告称某种品牌的八宝粥(含桂圆、红豆、糯米等)不加糖,比加糖还甜,最适合糖尿病人食用。你认为下列关于糖尿病人能否食用此八宝粥的判断不正确的是 A.这个广告有误导喜爱甜食消费者的嫌疑,不加糖不等于没有糖 B.不加糖不等于没有糖,糖尿病人食用需慎重 C.不能听从厂商或广告商的宣传,应咨询医生 D.糖
|
|
| 51. | 详细信息 |
|
下列物质是常见的氧化剂的是 A.O2 B. HNO3 C.KMnO4 D.CO
|
|
| 52. | 详细信息 |
|
下列措施是为了加快化学反应速率的是 A.食品放在冰箱中贮藏 B.双氧水制氧气时加入少量二氧化锰 C.试管中进行镁和水反应时,
|
|
| 53. | 详细信息 |
|
据报道,碳纳米管是碳原子形成的大分子,其导电性是铜的1万倍;N5可以做烈性炸药。下列叙述不正确的是 A.14C的质子数为14 B.N5和N2互为同素异形体 C.金刚石和纳米管互为同分异构体 D.C原子半径比N原子半径小
|
|
| 54. | 详细信息 |
|
糖类是人体主要的能量来源。下列物质中,属于糖类的是 A.葡萄糖 B.蔗糖 C.淀粉 D.酶
|
|
| 55. | 详细信息 |
|
下列过程属于化学变化的是 A.煤的干馏 B.石油的分馏 C.石油的裂解 D.蔗糖的水解
|
|
| 56. | 详细信息 |
|
随着卤素原子序数递增,下列说法不正确的是 A.单质的熔、沸点逐渐降低 B.单质的氧化性逐渐增强 C.阴离子的还原性逐渐增强 D.气态氢化物稳定性逐渐增强
|
|
| 57. | 详细信息 |
|
雷雨天闪电时空气中有臭氧生成,下列说法正确的是 A.O2和O3的相互转化是物理变化 B.O2和O3互为同素异形体 C.等物质的量的O2和O3含有的质子数不相同 D.在相同的温度与压强下,等体积的O2和O3含有相同的分子数
|
|
| 58. | 详细信息 |
|
下列物质中,含有共价键的是 A.NaOH B.NaCl C.H2S D.H2
|
|
| 59. | 详细信息 |
|
下列叙述正确的是 A.氧化还原反应一定是有氧参加的反应 B.有单质生成的反应不一定是氧化还原反应 C.置换反应一定属于氧化还原反应 D.发生氧化反应的是所含元素化合价升高的反应物
|
|
| 60. | 详细信息 |
|
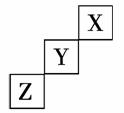
短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法中正确的是
B.X的 C.Y元素原子的最外层电子数为7 D.Z的最高价氧化物对应水化物的化学式为H2ZO4
|
|