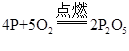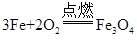2020江西九年级上学期人教版初中化学单元测试
| 1. | 详细信息 |
|
下列说法正确的是( ) A.根据质量守恒定律,1 L氢气和1 L氧气反应生成2 L水 B.蜡烛完全燃烧后消失不见了,不遵循质量守恒定律 C.只有固体或液体间的反应才遵循质量守恒定律 D.铁丝在氧气中燃烧,生成四氧化三铁的质量等于参加反应的铁丝与氧气的质量之和
|
|
| 2. | 详细信息 |
|
下列实验操作正确的是( ) A. C.
|
|
| 3. | 详细信息 |
|
下列关于化学方程式“ A.磷跟氧气在点燃的条件下反应生成五氧化二磷 B.每4个磷原子和5个氧分子在点燃的条件下反应生成2个五氧化二磷分子 C.参加反应的磷的质量的4倍加上参加反应的氧气的质量的5倍等于生成的五氧化二磷的质量的2倍 D.每31份质量的磷跟40份质量的氧气在点燃的条件下反应生成71份质量的五氧化二磷
|
|
| 4. | 详细信息 |
|
2.3 g某化合物在氧气中完全燃烧生成4.4 g二氧化碳和2.7 g水,则该化合物可能是( ) A.CH4 B.C2H4 C.C2H6 D.C2H5OH
|
|
| 5. | 详细信息 |
|
过氧化钠(Na2O2)可作呼吸面具中氧气的来源,它与二氧化碳反应后的生成物为( ) A.Na2CO3和H2 B.Na2O和O2 C.NaOH和O2 D.Na2CO3和O2
|
|
| 6. | 详细信息 |
|
ClO2是一种高效的水处理剂,制备ClO2的化学方程式为 A.Na2 SO4 B.Na2SO3 C.NaHSO4 D.NaHSO3
|
|
| 7. | 详细信息 |
|
老师板书的下列四个反应的生成物都是C,如果C的化学式为A2B5,则该反应的化学方程式为( ) A. B. C. D.
|
|
| 8. | 详细信息 |
|
在一个密闭容器中,有甲、乙、丙、丁、戊五种物质,在一定条件下发生反应,测得反应前后各物质的质量变化量如图所示(图中正数表示物质质量的增加量,负数表示物质质量的减少量,0表示物质质量不变),下列说法正确的是( )
B.戊一定是该反应的催化剂 C.参加反应的乙、丙的质量比一定为48∶23 D.该反应中甲、丁的相对分子质量之比一定为44∶27
|
|
| 9. | 详细信息 |
|
在化学反应 A.9 B.12 C.18 D.36
|
|
| 10. | 详细信息 |
|
在密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时刻各物质质量变化情况如图所示,下列说法正确的是( )
A.丁是反应物 B.丙一定是催化剂 C.生成丁的质量为8 g D.参加反应的甲、乙的质量比为5∶2
|
|
| 11. | 详细信息 |
|
化学反应前后一定发生变化的是(______) A 原子数目 B 分子数目 C 物质种类 D ____
|
|
| 12. | 详细信息 |
|
下列化学方程式书写正确的是(____) A 氧化汞受热分解: B 铁在氧气中燃烧: C 氢氧化钠溶液与硫酸铜溶液混合: D 电解水:_____________
|
|
| 13. | 详细信息 |
|
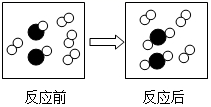
下图是某反应过程的微观示意图,“
A 参加反应的“ B 反应前后分子种类没有改变 C 反应后该密闭体系中没有单质存在 D 该反应属于____(填基本反应类型)反应
|
|
| 14. | 详细信息 |
|
在一密闭的容器内装有氢气和氧气的混合物共10 g,点火充分反应后得到9 g水,则原混合气体中氢气的质量可能是(____) A 1 g B 8 g C 11.1 g D ____
|
|
| 15. | 详细信息 | |||||||||||||||
|
下列实验方案正确的是(____)
|
||||||||||||||||
| 16. | 详细信息 |
|
高锰酸钾在医药领域可用作防腐剂、消毒剂、除臭剂及解毒剂;在水质净化及废水处理方面可作水处理剂,以氧化硫化氢、酚、铁、锰和有机、无机等多种污染物,控制臭味和脱色。请用化学用语填空: (1)钾元素:_____; (2)铁离子:_____; (3)两个水分子:_____; (4)标出高锰酸钾中锰元素的化合价:_____。
|
|
| 17. | 详细信息 |
|
据下图完成下列内容。
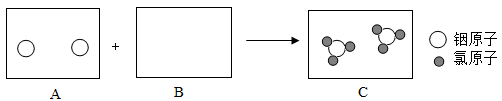
(1)铟属于____(填“金属”或“非金属”)元素,其相对原子质量为____。 (2)铟原子核外有_个电子层,铟元素的化学性质与铝元素的化学性质相似,原因是____。 (3)铟与氯气反应生成氯化铟的微观过程可表示为:
请将B框中的信息补充完整____。你这样补充的理由是____。
|
|
| 18. | 详细信息 |
|
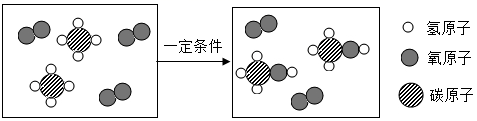
科学家成功研发出一种合成甲醇的新工艺,其反应过程的微观示意图如图。请回答下列问题。
(1)图中共有__种分子,属于单质的物质的化学式是__。 (2)写出图中反应的化学方程式:________,参加该反应的反应物的质量比是_。
|
|
| 19. | 详细信息 |
|
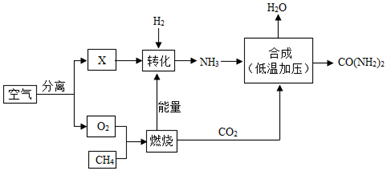
空气是宝贵的自然资源,下图是以空气等为原料生产尿素
(2)图中分离空气的过程属于__(填“物理”或“化学”)变化。 (3)甲烷(CH4)燃烧会生成水和二氧化碳,写出该反应的化学方程式:__。 (4)合成尿素的反应____(填“属于”或“不属于”)化合反应。
|
|
| 20. | 详细信息 |
|
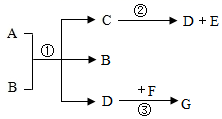
已知A~G都是初中化学常见的物质,通常状况下,A、C为无色液体,且组成元素相同,D、E为气体,F为黑色固体,G能使澄清石灰水变浑浊,它们之间的转化关系如图所示。回答下列问题。
(1)物质E的化学式是______。 (2)物质B在反应①中的作用是______。 (3)检验气体D的方法是________________。 (4)写出反应③的化学方程式:____________。
|
|
| 21. | 详细信息 |
|
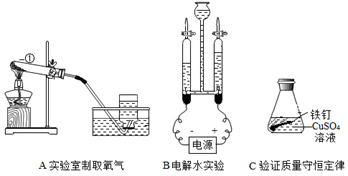
实验是学习化学的重要途径,下列是教材中的三个基本实验,请回答下列问题。
(1)实验A中标号①仪器的名称是____,利用该装置用高锰酸钾制取氧气,未能收集到两瓶氧气,可能的原因是____。 A 没有塞紧橡胶塞 B 试管口没有放棉花 C 收集时没有及时更换到第二瓶 D 加热前已将集气瓶灌满水倒立于水槽中 (2)实验B是通过证明生成物的___推断水的组成的。将燃着的木条靠近打开活塞后的两个玻璃管的尖嘴口,观察现象,得出关于水的组成的结论是_______。 (3)实验C中观察到的现象是__,反应的化学方程式为__。
|
|
| 22. | 详细信息 |
|
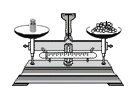
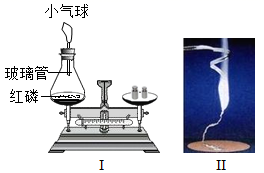
化学社团的同学用图所示实验验证质量守恒定律。图Ⅰ中将锥形瓶和玻璃管放在托盘天平上,调节砝码和游码使天平平衡,记录所称得的质量为M1,待反应后锥形瓶冷却,重新放到托盘天平上,记录所称得的质量为M2。图Ⅱ取一根用砂纸打磨干净的镁条和一块石棉网,称量其质量为M3,在石棉网上方点燃镁条,冷却后将燃烧后的产物和石棉网一起称量,称得其质量为M4。
【知识回顾】 质量守恒定律:__的各物质的质量总和,等于反应后生成的各物质的质量总和,这个规律叫作质量守恒定律。 【实验分析】 (1)锥形瓶的底部铺有一层细沙,其作用是_________。 (2)红磷燃烧过程中观察到气球的变化是____________。 (3)M1=95.9 g,M2=95.9 g,则红磷燃烧__(填“遵循”或“不遵循”)质量守恒定律。 (4)M4_(填“>”“=”或“<”)M3,理由是________________。 【实验结论】 图Ⅰ和图Ⅱ两个实验都遵循质量守恒定律的微观原因是____________。
|
|
| 23. | 详细信息 | ||||||
|
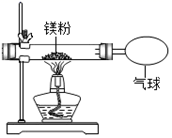
小红用如图装置验证了质量守恒定律,还发现产物中有少量黄色固体。
【查阅资料】 ①氧化镁为白色固体; ②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体; ③氮化镁可与水剧烈反应生成氨气,该气体能使湿润的红色石蕊试纸变蓝。 【作出猜想】 黄色固体是氮化镁。 【实验探究】 设计实验,验证猜想:
【反思与交流】 空气中氮气的含量远大于氧气的含量,可是镁条在空气中的燃烧产物氧化镁却远多于氮化镁,合理的解释是_。镁在氮气中燃烧的化学方程式为______。 【拓展延伸】 同学们再次查阅资料得知,镁还能在二氧化碳中燃烧,生成一种白色固体氧化物和一种单质,试写出该反应的化学方程式:__。
|
|||||||
| 24. | 详细信息 | ||||||||||
|
某兴趣小组用氯酸钾与二氧化锰的混合物制取氧气,试管中固体的质量随时间变化的数据见下表。
(1)共制得氧气 g。 (2)计算原混合物中二氧化锰的质量(写出计算过程)。 (3)t1时刻试管中的固体物质包含 。
|
|||||||||||
 B
B
 D
D