2020广东人教版(2019)高中化学月考试卷
| 1. | 详细信息 |
|
下列设备工作时,将化学能转化为电能的是( ) A.硅太阳能电池 B.铅蓄电池 C.燃气灶 D.电烤箱
|
|
| 2. | 详细信息 |
|
可逆反应N2+3H2 列关系中能说明反应已达到平衡状态的是 ( ) A.v正(N2)= v逆(NH3) B. 3v正(N2)= v正(H2) C.2v正(H2)=3 v逆(NH3) D.v正(N2)=3 v逆(H2)
|
|
| 3. | 详细信息 |
|
用铁片与稀硫酸反应制氢气时,下列措施不能使反应速率加快的是( ) A. 加热 B. 不用稀硫酸,改用98%的浓硫酸 C. 滴加少量CuSO4溶液 D.不用铁片,改用铁粉
|
|
| 4. | 详细信息 |
|
下物质分类组合正确的是( ) A B C D 强电解质:HBr FeCl3 H3PO4 Ca(OH)2 弱电解质:HF CH3COOH BaSO4 HI 非电解质:CCl4 Cu H2O C2H5OH
|
|
| 5. | 详细信息 |
|
关于化学平衡常数K的叙述正确的是( ) A. K值越大,表示化学反应速率越大 B. 对任一可逆反应,温度升高,则K值增大 C.加入催化剂或增大反应物的浓度时,K值均增大 D.一般情况下K值越大,可逆反应进行的越彻底
|
|
| 6. | 详细信息 |
|
用蒸馏水稀释0.1mol/L的CH3COOH时,始终保持增大趋势的是( )
|
|
| 7. | 详细信息 |
|
pH值相同的下列溶液,其物质的量浓度最大的是( )
|
|
| 8. | 详细信息 |
|
将pH=3的盐酸溶液和pH=11的氨水等体积混合后,溶液中离子浓度关系正确的是: A、c(NH4+)>c(Cl–)>c(H+)>c(OH–) B、c(NH4+)>c(Cl–)>c(OH–)>c(H+) C、c(Cl–)>c(NH4+)>c(H+)>c(OH–) D、c(Cl–)>c(NH4+)>c(OH–)>c(H+)
|
|
| 9. | 详细信息 |
|
A.②③ B.①② C.③④ D.④⑤
|
|
| 10. | 详细信息 |
|
下列化学用语中正确的是( ) A. 乙烯的结构简式为CH2CH2 B. 羟基的电子式 C. 2-丁烯的键线式为 D. 乙醇的分子式为CH3CH2OH
|
|
| 11. | 详细信息 |
|
1999年,在欧洲一些国家发现饲料被污染,导致畜禽类制品及乳制品不能食用,经测定饲料中含有剧毒物质二恶英,其结构为 A. 15种 B. 11种 C. 10种 D. 5种
|
|
| 12. | 详细信息 |
|
下列物质属于醇类的是 A.
|
|
| 13. | 详细信息 |
|
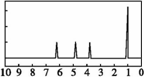
下列化合物分子中,在核磁共振氢谱图中能给出三种信号的是( ) A.CH3CH2CH3 B.CH3CH2CH2CH3 C. CH3OCH3 D. CH3CH2OH
|
|
| 14. | 详细信息 |
|
现有三组混合液:①汽油和水混合液 ②乙醇和己醇 ③溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是 A.分液、萃取、蒸馏 B. 萃取、蒸馏、分液 C.分液、蒸馏、萃取 D. 蒸馏、萃取、分液
|
|
| 15. | 详细信息 |
|
对已达平衡的下列反应 2X(g)+Y(g) A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 C. 正、逆反应速率都增大,平衡向正反应方向移动 D.正、逆反应速率都减小,平衡向逆反应方向移动
|
|
| 16. | 详细信息 | ||||||||||||
|
Ⅰ.在一定体积的密闭容器中,进行如下化学反应: CO2(g)+H2(g) 其化学平衡常数K和温度t的关系如下表:
回答下列问题: (1)该反应的化学平衡常数表达式为K = (2)该反应为 反应(选填“吸热”或“放热”)。 (3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。 Ⅱ.(1)FeCl3的水溶液呈 (填“酸”、“中”、“碱”)性, 原因是(用离子方程式表示): ; (2)实验室在配制FeCl3的溶液时,常将 FeCl3固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。 (3)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
|
|||||||||||||
| 17. | 详细信息 | ||||||
|
Ⅰ.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)上图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:_______________________________________________________ 。 (2)若已知下列数据:
试根据表中及图中数据计算N—H的键能:________ kJ·mol-1。 (3) 捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应: 反应 Ⅰ:2NH3(l)+H2O(l)+CO2(g) 反应 Ⅱ:NH3(l)+H2O(l)+CO2(g) 反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g) 则ΔH3与ΔH1、ΔH2之间的关系是ΔH3=________ 。
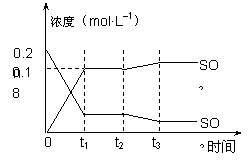
时达到平衡。如右图所示: (1) 用O2表示2分钟内该反应的平均反应速 率为 mol·L-1·min-1 计算500℃时该反应的平衡常数K= (2)上图表示该反应在时刻t1达到平衡后,求平衡时O2的转化率 ,时刻t2因改变某个条件而发生变化的情况:图中时刻t2发生改变的条件可能是 (写一个即可)。
|
|||||||
| 18. | 详细信息 | |
|
(1). (2分)按系统命名法命名有机物 (2). (4分)写出下列有机物的结构简式 2,3-二甲基-4-乙基已烷 _____________________________________ 1 mol该烃完全燃烧需消耗氧气 mol。 (3)(8分) 写出C4H9Cl的各种同分异构体的结构简式
|
||
| 19. | 详细信息 | ||||||||||
|
Ⅰ.有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
Ⅱ. (3分) 1MCP广泛应用于果蔬的保鲜,其结构简式如图所示
其分子式为
|
|||||||||||

 B
B C
C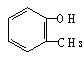 D
D