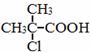2018广东高三下学期人教版高中化学高考模拟
| 1. | 详细信息 |
|
A.“地沟油”禁止食用,但可以用来制肥皂或燃油 B.BaCO3在医学上可用作“钡餐” C.光导纤维的主要成分是SiO2,太阳能电池使用的材料是单质硅 D.臭氧、醋酸、双氧水都能杀菌消毒
|
|
| 2. | 详细信息 |
|
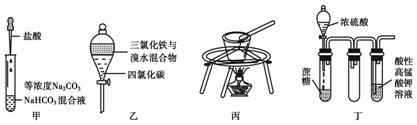
对于下图所示实验,下列实验现象预测或操作正确的是
A.实验甲:匀速逐滴滴加盐酸时,试管中没气泡产生和有气泡产生的时间段相同 B.实验乙:充分振荡后静置,下层溶液为橙红色,上层为无色 C.实验丙:由MgCl2•6H2O制备无水MgCl2 D.装置丁:酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅乃至褪去
|
|
| 3. | 详细信息 |
|
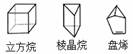
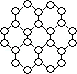
都属于多环烃类,下列有关它们的说法错误的是
A.这三种有机物的二氯代物同分异构体数目相同 B.盘烯能使酸性高锰酸钾溶液褪色 C.棱晶烷和盘烯互为同分异构体 D.等质量的这三种有机物完全燃烧,耗氧量相同
|
|
| 4. | 详细信息 |
|
锂空气电池放电时的工作原理如图所示。下列叙述正确的是
B.电池放电时总反应方程式为4Li+O2 +2H2O===4LiOH C.电解液a、b之间可采用阴离子交换膜 D.电解液a可能为LiCl水溶液
|
|
| 5. | 详细信息 |
|
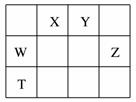
A.X、Y能形成不止一种氢化物,而Z只能形成一种 B.W和Z形成的共价化合物中,所有原子最外层均满足8电子稳定结构 C.W和T都具有良好的半导体性能 D.X和Y最多可以形成5种化合物
|
|
| 6. | 详细信息 | |||||||||||||||
|
下列陈述I、Ⅱ均正确且有因果关系的是
|
||||||||||||||||
| 7. | 详细信息 |
|
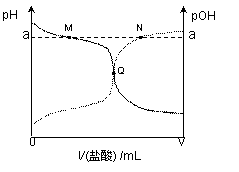
A.N点所在曲线为pH变化曲线 B.M、N两点的溶液中NH4+的物质的量:M>N C.Q点消耗盐酸的体积大于氨水的体积 D.随着盐酸滴入,溶液导电性持续增强
|
|
| 8. | 详细信息 |
|
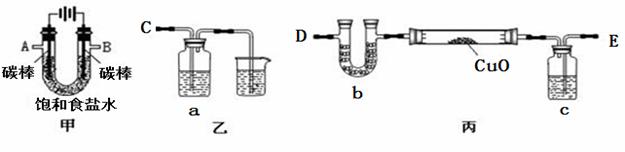
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。
(1)写出装置甲的电解总反应方程式 。 (2)为完成上述实验,正确的连接顺序为E→ (填写连接的字母)。 (3)对硬质玻璃管里的氧化铜粉末进行加热前,需要先通一段时间某气体并检验该气体的纯度,检验该气体已经纯的具体的操作和现象为 。 (4)乙装置的a瓶溶液可选用 。 A.淀粉碘化钾溶液 B.酸性高锰酸钾溶液 C.硫化钠溶液 D.Fe(NO3)2溶液 (5)若a瓶中盛放过量的NaHSO3溶液,写出发生的离子反应方程式 。 (6)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案。精确测量硬质玻璃管的质量为a g,加入CuO后,精确测量硬质玻璃管和CuO的总质量为b g , 实验完毕后: 甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。 乙方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。 乙方案不足之处是 。 按甲方案进行计算,Cu的相对原子质量为 。(用含a、b、c的式子来表示)
|
|
| 9. | 详细信息 |
|
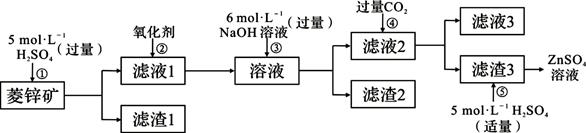
锌钡白是一种白色颜料。工业上是由ZnSO4与BaS溶液混合而成: BaS+ZnSO4=ZnS↓+BaSO4↓。请根据以下工业生产流程回答有关问题。
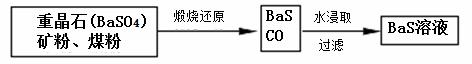
Ⅰ.ZnSO4溶液的制备与提纯: 有关资料:a.菱锌矿的主要成分是ZnCO3,含少量SiO2、FeCO3、Cu2(OH)2CO3等; b.Zn(OH)2与Al(OH)3相似,能溶于过量的NaOH溶液生成Na2ZnO2。 (1)若②中加入氧化剂为H2O2,写出离子反应方程式 。 (2)为了达到综合利用、节能减排的目的,上述流程步骤④中的CO2可以来自于步骤 (选填①、②、③、⑤)。 (3)滤渣2的主要成分为 。 (4)写出步骤④后产生滤渣3的离子反应方程式 。 (5)滤液3中含碳粒子浓度大小的顺序为 。 Ⅱ.BaS溶液的制备:
(6)写出煅烧还原的化学反应方程式 。 BaSO4和BaCO3的KSP相当,解释为什么BaCO3可溶于盐酸中而BaSO4难溶 。 Ⅲ.制取锌钡白: (7)如果生产流程步骤⑤硫酸过量,则ZnSO4与BaS溶液混合制取锌钡白产生的后果是 。
|
|
| 10. | 详细信息 |
|
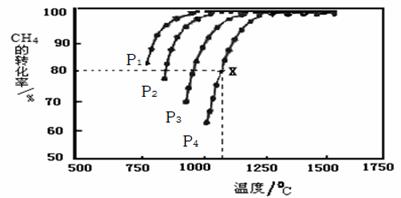
研究CO2与CH4的反应使之转化为CO和H2,对减缓燃料危机,减少温室效应具有重要的意义。 (1)已知CH4(g)+CO2(g) (2)在密闭恒容容器中通入物质的量浓度均为0.1 mol·L-1的CH4与CO2,在一定条件下发生反应 CH4(g)+CO2(g)
①工业生产时一般会选用P4和1250℃进行合成,请解释其原因 。 ②在压强为P4、1100℃的条件下,该反应5min时达到平衡点X,则用CO表示该反应的速率为 ,该温度下,反应的平衡常数为 (保留3位有效数字)。 (3)CO和H2在工业上还可以通过反应C(s)+H2O(g) ①在恒温恒容下,如果从反应物出发建立平衡,可认定已达平衡状态的是 。 A.体系压强不再变化 B.H2、CO和H2O的物质的量之比为1:1:1 C.混合气体的密度保持不变 D.气体平均相对分子质量保持不变 ②在某体积可变的密闭容器中同时投入四种物质,2min时达到平衡,测得容器中有1mol H2O(g)、1mol CO(g)、2.2molH2(g)和足量的C(s),如果此时对体系加压,平衡向 (填“正”或“逆”)反应方向移动,达到新的平衡后,气体的平均摩尔质量为 。
|
|
| 11. | 详细信息 |
|
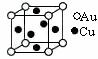
(1)下列有关石墨烯说法正确的是 。 A.键长:石墨烯>金刚石 B.石墨烯分子中所有原子可以处于同一平面 C.12g石墨烯含 D.从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用力 (2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,含碳源可以是甲烷、乙炔、苯、乙醇或酞菁等中的一种或任意组合。 ①铜原子在基态时,在有电子填充的能级中,能量最高的能级符号为 ;第四周期元素中,最外层电子数与铜相同的元素还有 。 ②乙醇的沸点要高于相对分子质量比它还高的丁烷,请解释原因 。 ③下列分子属于非极性分子的是 。 a.甲烷 b.二氯甲烷 c.苯 d.乙醇 ④酞菁与酞菁铜染料分子结构如右图,酞菁分子中碳原子采用的杂化方式是 ;酞菁铜分子中心原子的配位数为 。 ⑤金与铜可形成的金属互化物合金(如图,该晶胞中,Au占据立方体的8个顶点)
|
|
| 12. | 详细信息 |
|
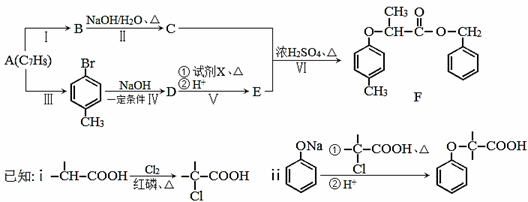
有机物F是一种香料,其合成路线如图所示:
(1)D的名称为 ,试剂X的结构简式为 ,步骤Ⅵ的反应类型为 。 (2)步骤Ⅰ的反应试剂和条件分别为 、 。 (3)步骤Ⅱ反应的化学方程式为 。 (4)满足括号中条件(①苯环上只有两个取代基,②能与FeCl3溶液发生显色反应,③能发生水解反应和银镜反应)的E的同分异构体有 种,其中核磁共振氢谱峰面积比为6︰2︰2︰1︰1的分子的结构简式为 。 (5)依据题中信息,完成以 (无机试剂一定要选银氨溶液,其它无机试剂任选) 合成路线图示例如下:
|
|