高一上学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
在物质分类中,前者包括后者的是 A.化合物、电解质 B.氧化物、化合物 C.钠的化合物、单质钠 D.溶液、分散系
|
|
| 2. | 详细信息 |
|
下列关于硅和硅的化合物叙述不正确的是 ①硅晶体的结构和金刚石相似 ②硅是地壳中含量最多的元素 ③单晶硅是良好的半导体材料 ④二氧化硅是制造光导纤维的重要原料 ⑤二氧化硅分子由两个氧原子和一个硅原子组成 ⑥二氧化硅是酸性氧化物,它不溶于任何酸。 A.①②③ B.①⑤⑥ C.③④⑤ D.②⑤⑥
|
|
| 3. | 详细信息 |
|
.溴(Br)与氯同属“卤族”元素,其单质在性质上具有很大的相似性,但Cl2比Br2的活泼性强,下面是根据氯的性质对溴的性质进行预测,其中不正确的是 A.溴单质常温下为液态,但极容易挥发为溴蒸气 B.溴也可与NaOH溶液反应生成NaBr、NaBrO、H2O C.溴原子外层有7个电子,在化学反应中容易得1个电子,表现氧化性 D.溴单质只具有氧化性
|
|
| 4. | 详细信息 |
|
将两份质量相同的铁、铝合金分别放入足量的盐酸和氢氧化钠溶液中充分反应,放出的氢气质量相等,则合金中铝、铁的质量之比为 A. 28∶9 B. 56∶27 C.3∶2 D. 1∶1
|
|
| 5. | 详细信息 |
|
向含有NaBr、NaI的溶液中通入足量的氯气后,将所得溶液蒸干灼烧,所的固体产物是 A. NaCl、NaBr B. NaCl、Br2、I2 C. NaCl D. NaCl、I2
|
|
| 6. | 详细信息 |
|
下列叙述中正确的是 A.1 mol任何气体的体积都约为22.4 L B.在标准状况下某气体的体积约为22.4 L,则可认为该气体的物质的量约是1 mol C.在0 ℃,1.01×1023时,1 mol水的体积为22.4 L D.标准状况下,22.4 L CO2和O2混合气体中含有6.02×1023个氧原子
|
|
| 7. | 详细信息 |
|
只用一种化学试剂一次即可将Na2CO3、MgSO4和AlCl3三种溶液鉴别开来,则该试剂是 A.NaOH溶液 B.盐酸 C.氨水 D.AgNO3溶液
|
|
| 8. | 详细信息 |
|
下列有关氢氧化铁悬浊液与氢氧化铁胶体的说法正确的是 A.都可以发生丁达尔现象 B.分别滴加稀硫酸至过量,现象不同,最终产物相同 C.能透过半透膜 D.分散质颗粒直径都在1~100 nm之间
|
|
| 9. | 详细信息 |
|
下列说法不正确的是 A.相同物质的量的任何物质具有相同数目的微粒 B.氧化还原反应过程中一定存在电子的得失或共用电子对的偏移 C.无论什么状况下,质量一定的某种气体含有的分子数是一定的 D.相同状况下,气体的相对分子质量越大则气体密度越大
|
|
| 10. | 详细信息 |
|
.下列各组的两种溶液中,分别加入足量氨水,观察到的现象相同的是 A.FeCl3 AlCl3 B.FeCl2 FeCl3 C.MgCl2 CuCl2 D.AlCl3 Ca(HCO3)2
|
|
| 11. | 详细信息 |
|
下列实验操作中错误的是 A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 B.蒸馏时应使温度计水银球靠近蒸馏烧瓶支管口 C.蒸发时,待蒸发皿中没有水了再停止加热 D.称量氢氧化钠时,应先将小烧杯放在左盘称量,再将样品加入到小烧杯中称量
|
|
| 12. | 详细信息 |
|
在烧杯中加水和煤油(密度:0.8g/cm3)各50mL。将一小粒金属钠(密度:0.97g/cm3)投入烧杯中。其现象可能是 A.钠在水层中反应并四处游动 B.钠停留在煤油层中不发生反应 C.钠在煤油的液面上反应并四处游动 D.钠在煤油与水的界面处反应并可能作上、下跳动
|
|
| 13. | 详细信息 |
|
下列离子方程式的书写正确的是 A.实验室用石灰石和稀盐酸反应制取CO2:CO32- + 2H+ = CO2↑ + H2O B.硫酸铝溶液与足量烧碱溶液反应:Al3+ + 4OH- = AlO2- + 2H2O C.氢氧化钠钠溶液通入足量的CO2气体:2OH-+CO2 =CO32- D.金属钠投入水中:Na + H2O = Na+ + OH- + H2↑
|
|
| 14. | 详细信息 |
|
等物质的量的Na2O和Na2O2分别与质量相等的足量的水反应,所得溶液质量分数的关系是 A.前者大 B.后者大 C.相等 D.无法确定
|
|
| 15. | 详细信息 |
|
.⑴(4分)在反应NaClO +SO2+H2O =NaCl+H2SO4中,氧化剂是 ,氧化产物是 ; 在反应3NO2+H2O=2HNO3+NO中,还原产物是 ,氧化剂与还原剂的物质的量之比为 。 ⑵(6分)请按要求写出下列反应的离子方程式 (1)氯气与氢氧化钙溶液反应: ; (2)硫酸铝溶液与氨水反应: ; (3)写出Ba(OH)2+NaHSO4=BaSO4↓+NaOH+H2O: ;
|
|
| 16. | 详细信息 |
|
⑴(4分)现有标准状况下8.96LSO2和24gO3,则相同状况下SO2与O3的体积之比为 ,所含氧原子数之比为 。 ⑵(4分)向100mL2mol/L的NaOH溶液中缓慢通入一定量的CO2。 ①当n(CO2)≤0.1mol 时,反应的离子方程式为: ; ②当0.1mol<n(CO2) <0.2mol时,所得溶液的溶质有 ;
|
|
| 17. | 详细信息 |
|
(每问2分,共8分)欲用质量分数为98%、密度为1.84g/cm3的浓硫酸,配制0.2mol/L的硫酸溶液480mL。试回答下列问题: (1)你所需要量取的浓硫酸的体积为 mL; (2)本实验必需用到的玻璃仪器有:胶头滴管、玻璃棒、烧杯和 、 ; (3)将量取好的浓硫酸 ,用玻璃棒搅拌,待充分冷却后,将烧杯中的溶液转移到容量瓶中; (4)配制过程中,造成浓度偏高的操作有 (填序号); A.容量瓶用蒸馏水洗后未干燥 B.量筒用蒸馏水洗后未干燥 C.未用水洗涤溶解过浓硫酸的烧杯 D.用量筒量取浓硫酸时,仰视读数 E.定容时,俯视液面加水至刻度线 F.转移浓溶液时不慎有液滴掉在容量瓶外面
|
|
| 18. | 详细信息 |
|
A、B、C、D四种化合物,其中A、C、D焰色反应均为黄色,而B的焰色反应为紫色。灼烧固体D可以得到A,若在A的溶液中通入一种无色无味气体又可制得D;C中逐滴滴加盐酸时现有白色沉淀生成,而后沉淀又逐渐溶解;在含有酚酞的水中加入固体B,有无色无味的气体产生,且溶液先变红后褪色。试推断: A ; B ; C ; D ;
|
|
| 19. | 详细信息 |
|
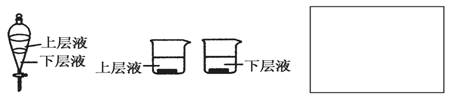
③实验过程 实验Ⅰ:把红色干布放入充满干燥氯气的集气瓶中,布条不褪色 实验Ⅱ:________________________________________________;(1分) 实验Ⅲ:把红色布条放在水里,布条不褪色。 ④得出结论:_______________________________________________(1分) (3)用量筒量取20 mL氯水,倒入已检查完好的分液漏斗中,然后再注入10 mL CCl4,盖好玻璃塞,充分振荡,静置于铁架台上(如下图),等分层后取上层液和下层液,呈黄绿色的是 (填“上层液”或“下层液”下同),再装入如图所示的烧杯中,能使有色布条褪色的是 (每空1分)
(4)这套制取氯水装置的缺点是 ,(1分) 请在上面的方框中画出改进部分的实验装置图。(2分)
|
|
| 20. | 详细信息 | |||
|
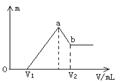
将镁和铝的混合物0.1mol溶于100mL 2 mol/L的H2SO4溶液中,然后滴加 1 mol/L的NaOH溶液。在滴加NaOH溶液的过程中, 沉淀质量m随加入 NaOH溶液的体积V变化如右图所示。请回答: (1)写出铝与氢氧化钠溶液反应的离子方程式: (2分) (2)若当V1=160mL时,则金属粉末中n(Mg)=_________mol,V2=__________m L。(共4分) (3)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积应为__________mL。(2分)
|
||||