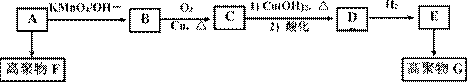2019江西高三上学期人教版(2019)高中化学期中考试
| 1. | 详细信息 | |||||||||||||||
|
有些古文或谚语包含了丰富的化学知识,下列解释不正确的是
A. A B. B C. C D. D
|
||||||||||||||||
| 2. | 详细信息 |
|
.下列排列顺序正确的是( ) A. 电离出氢离子的能力:CH3COOH>C2H5OH>H2O B. 微粒半径:Fe(OH)3胶粒>K+>C1->Na+ C. 固体的热稳定性:Na2CO3>CaCO3>NaHCO3 D. 氢化物的沸点:H2Se>H2S>H2O
|
|
| 3. | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列叙述正确的是( ) A. 常温常压下33.6L氯气与27g铝充分反应,转移的电子数为3NA B. 标准状况下,28g乙烯和丙烯的混合气体中所含原子个数为4NA C. 一定条件下,将1molN2与3molH2混合反应后,生成NH3分子的数目为2NA D. 在电解CuSO4溶液的实验中,测得电解后溶液pH=0,又知电解后溶液体积为1L,在阳极析出的气体分子数约为0.25NA
|
|
| 4. | 详细信息 |
|
室温下,下列各组微粒在指定溶液中能大量共存的是( ) A. pH=1的溶液中:CH3CH2OH、Cr2O72-、K+、SO42- B. c(Ca2+)=0.1 mol·L-1的溶液中:NH4+、SiO32-、C2O42-、Br- C. 加入铝粉放出大量H2的溶液中:Fe2+、Na+、Cl-、NO3- D. NaHCO3溶液中: C6H5O-、CO32-、Br-、K+
|
|
| 5. | 详细信息 |
|
分子式为C4H8O2且能与NaOH溶液发生水解反应的有机物有(不考虑空间异构) A. 6种 B. 5种 C. 4种 D. 3种
|
|
| 6. | 详细信息 |
|
已知NH4CuSO3与足量的3 mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。据此判断下列说法正确的是( ) A. 构反应中硫酸作氧化剂 B. NH4CuSO3中硫元素被氧化 C. 刺激性气味的气体是氨气 D. 1 mol NH4CuSO3完全反应转移0.5 mol电子
|
|
| 7. | 详细信息 | |||||||||||||||
|
下列离子方程式的书写及评价均合理的是( )
A. A B. B C. C D. D
|
||||||||||||||||
| 8. | 详细信息 | |||||||||||||||
|
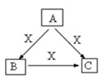
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是( )
A. A B. B C. C D. D
|
||||||||||||||||
| 9. | 详细信息 | ||||||||||||
|
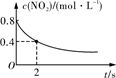
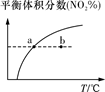
臭氧在烟气脱硝中的反应为2NO2(g)+O3(g)
A. A B. B C. C D. D
|
|||||||||||||
| 10. | 详细信息 |
|
下列有关滴定的说法正确的是( ) A. 用25mL滴定管进行中和滴定时,用去标准液的体积为21.7mL B. 用标准的KOH溶液滴定未知浓度的盐酸,配制标准溶液的固体KOH中有NaOH杂质,则结果偏低 C. 用C1mol/L酸性高锰酸钾溶液滴定V2mL未知浓度的H2C2O4溶液,至滴定终点用去酸性高猛酸钾溶液体积为V1mL,则H2C2O4溶液的浓度为 D. 用未知浓度的盐酸滴定已知浓度的NaOH溶液时,若读取读数时,滴定前仰视,滴定到终点后俯视,会导致测定结果偏低
|
|
| 11. | 详细信息 |
|
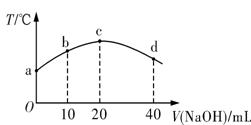
若往20 mL 0.01 mol·L-1 HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示。下列有关说法不正确的是
A. HNO2的电离平衡常数:c点>b点 B. b点混合溶液显酸性:c(Na+)>c(NO2-)>c(H+)>c(OH-) C. c点混合溶液中:c(OH-)>c(HNO2) D. d点混合溶液中:c(Na+)>c(OH-)>c(NO2-)>c(H+)
|
|
| 12. | 详细信息 |
|
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色呈黄色。5种元素核电荷数之和为54,最外层电子数之和为20。W、Z最外层电子数相同,Z的核电荷数是W的2倍。工业上一般通过电解氧化物的方法获得Y的单质。则下列说法不正确的是( ) A. 原子半径:X>Y>Q>W B. Q的单质都具有良好的导电性 C. Q和Z所形成的分子的空间构型为直线形 D. 化合物Y2Z3不能在水中稳定存在
|
|
| 13. | 详细信息 |
|
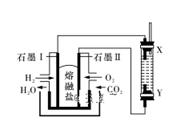
以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备Fe(OH)2,装置如图所示,其中电解池两极材料分别为铁和石墨,通电一段时间后,右侧玻璃管中产生大量的白色沉淀。则下列说法正确的是
A. 石墨电极Ⅱ处的电极反应式为O2+4e-===2O2- B. X是铁电极 C. 电解池中的电解液为蒸馏水 D. 若将电池两极所通气体互换,X、Y两极材料也互换,实验方案更合理
|
|
| 14. | 详细信息 | ||||||||||||||
|
.已知在常温下测得浓度均为0.1 mol/L的下列6种溶液的pH值如表所示:
下列反应不能成立的是( ) A. CO2+H2O+2NaClO===Na2CO3+2HClO B. CO2+H2O+NaClO===NaHCO3+HClO C. CO2+H2O+C6H5ONa===NaHCO3+C6H5OH D. CH3COOH+NaCN===CH3COONa+HCN
|
|||||||||||||||
| 15. | 详细信息 |
|
在100mL HNO3和H2SO4的混合溶液中,两种酸的物质的量浓度之和为0.6 mol • L-1。向该溶液中加入足量的铜粉,加热,充分反应后,所得溶液中Cu2+的物质的量浓度最大值为( )(反应前后溶液体积变化忽略不计) A. 0.225 mol • L-1 B. 0.30 mol • L-1 C. 0.36 mol • L-1 D. 0.45 mol • L-1
|
|
| 16. | 详细信息 |
|
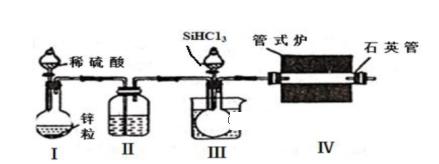
实验室用H2还原SiHCl3(沸点:31.85 ℃)制备纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法正确的是( )
A. 装置Ⅱ、Ⅲ中依次盛装的是浓H2SO4、冰水 B. 实验时,应先加热管式炉,再打开盛装稀硫酸的分液漏斗 C. 为鉴定制得的硅中是否含微量铁单质,用到的试剂可以为:盐酸、双氧水、硫氰化钾溶液 D. 该实验中制备氢气的装置也可用于氢氧化钠稀溶液与氯化铵固体反应制备氨气
|
|
| 17. | 详细信息 |
|
.A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示。请针对以下三种不同情况回答:
(1)若A、B、C均为化合物且焰色反应均为黄色,水溶液均为碱性。则C物质的化学式是_____________。 (2)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。 ①A中含有的金属元素为___________。(写元素符号) ②该金属元素的单质与某红棕色粉末在高温下反应,可用于焊接铁轨,反应的化学反应方程式为__________。 若A为固态非金属单质,A与X同周期,常温常压下C为白色固体,B分子中各原子最外层均为8e-结构。C与水剧烈反应,生成两种常见酸,反应的化学方程式为_______________________。
|
|
| 18. | 详细信息 |
|
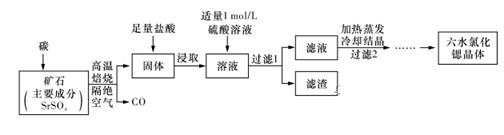
一种工业制备SrCl2·6H2O的生产流程如下图所示:
已知:①M(SrCl2·6H2O)=267 g/mol; ②Ksp(SrSO4)=3.3×10-7、Ksp(BaSO4)=1.1×10-10; ③经盐酸浸取后,溶液中有Sr2+和Cl-及少量Ba2+。 (1)隔绝空气高温焙烧,若2 mol SrSO4中只有S被还原,转移了16 mol电子。写出该反应的化学方程式:______________________________ 。 (2)过滤2后还需进行的两步操作是_____、_____。 (3)加入硫酸溶液的目的是_____;为了提高原料的利用率,滤液中Sr2+的浓度应不高于_____ mol/L(注:此时滤液中Ba2+浓度为1×10-5 mol/L)。 (4)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×10-2 mol的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应的离子),待Cl-完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+ 以AgSCN白色沉淀的形式析出。 ①滴定反应达到终点的现象是_____。 ②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为_____。
|
|
| 19. | 详细信息 |
|
.(1)某一反应体系中的物质有:HCl、SnCl2、H2SnCl6、As、H3AsO3、H2O,已知:HCl是反应物之一。 ①写出配平的该反应的化学方程式:_______________ ②被氧化的元素是___________ (2)氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它.CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+==Cu2++Cu. 根据以上信息,结合自己所掌握的化学知识,回答下列问题: ①写出CuH在氯气中燃烧的化学反应方程式:___________________________________. ②如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:__________________________________________________. (3)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_________
|
|
| 20. | 详细信息 |
|
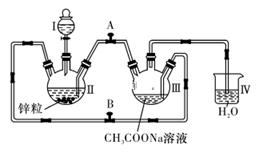
已知Cr2+不稳定,极易被氧气氧化,不与锌反应。醋酸亚铬水合物[Cr(CH3COO)2]2·2H2O是一种深红色晶体,不溶于冷水,是常用的氧气吸收剂。实验室中以锌粒、CrCl3溶液、CH3COONa溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如下图所示。制备过程中发生的相关反应如下所示: Zn+2HCl===ZnCl2+H2↑ Zn+2CrCl3===2CrCl2+ZnCl2 2Cr2++4CH3COO-+2H2O===[Cr(CH3COO)2]2·2H2O(晶体)
试回答下列问题: (1)本实验中配制溶液所用的蒸馏水需事先煮沸,原因是__________。 (2)往仪器Ⅱ中加盐酸和CrCl3溶液的顺序最好是__________________________,理由是____________。 (3)为使生成的CrCl2溶液与CH3COONa溶液混合,应关闭阀门____(填“A”或“B”,下同),打开阀门_____。 (4)本实验中锌粒要过量,其原因除了使锌与CrCl3充分反应得到CrCl2外,另一个作用是________。仪器Ⅳ的主要作用是___________。 (5)已知实验时取用的CrCl3溶液中含溶质9.51 g,取用的CH3COONa溶液为1.5 L 0.1 mol/L,其他反应物足量。实验后得干燥的[Cr(CH3COO)2]2·2H2O 9.4 g,则该实验所得产品的产率为________(用百分数表示,保留3位有效数字)(不考虑溶解的醋酸亚铬水合物)。
|
|
| 21. | 详细信息 |
|
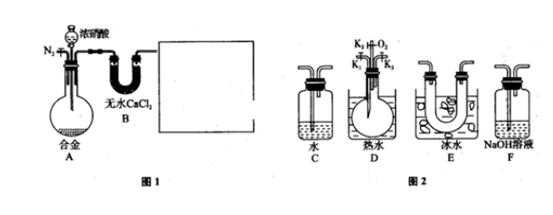
.某研究性学习小组,用下列仪器、药品验证足量合金(由Cu、Fe、Zn三种物质组成)和适量浓硝酸反应产生的气体中含NO(N2和O2的用量可自由控制,气体液化温度:NO2:21℃,NO:-152℃)
(1)在图2中选择恰当的仪器将图1补充完整,所选择仪器的连接顺序(按左→右连接,填各仪器编号)为_________. (2)反应前先通入N2目的是_______________________________________. (3)确认气体中含NO的现象是_____________________________________. (4)本题中,浓硝酸(含溶质a mol)完全反应,还原产物只有NO和NO2,被还原硝酸的物质的量n的取值范围为_________________________________________。
|
|
| 22. | 详细信息 |
|
烃A的质谱图中,质荷比最大的数值为42。碳氢两元素的质量比为6:1,其核磁共振氢谱有三个峰,峰的面积比为1:2:3。A与其他有机物之间的关系如下图所示:
已知:CH2=CH2 (1)F的结构简式为__________________。 (2)有机物C中的官能团名称_______________________。 (3)指出下列转化的化学反应类型:A→B__________ E→G____________。 (4)写出C与新制的氢氧化铜反应的化学方程式___________________________。 (5)E在一定条件下可以相互反应生成一种六元环有机物,则此反应的化学方程式为__________ 。 (6)与E互为同分异构体,且属于酯类的有机物,除CH3OCOOCH3、CH3CH2OCOOH外还有 __________种(分子中无O—O键)。
|
|