宜春市2019年高二化学上册月考测验在线免费考试
| 1. 选择题 | 详细信息 |
|
下列有关实验的叙述正确的是 A.过滤时,可用玻璃棒搅拌漏斗中的液体以加快过滤速率 B.用湿润的pH试纸测溶液的pH,因溶液被稀释而使测量值变大 C.酸碱滴定管、容量瓶、分液漏斗使用前必须检查是否漏水 D.酸碱滴定实验中,需用待滴定溶液润洗锥形瓶以减小实验误差 |
|
| 2. 选择题 | 详细信息 |
|
下列设计的实验方案能达到实验目的的是 A. 制取无水AlCl3:将AlCl3溶液加热蒸干并灼烧 B. 除去锅炉水垢中含有的CaSO4:先用Na2CO3溶液处理,然后再加酸去除 C. 证明氨水中存在电离平衡:向滴有酚酞的氨水中加入少量NH4Cl固体,溶液红色变深 D. 配制FeCl3溶液时为防止溶液浑浊常加入少量稀硫酸 |
|
| 3. 选择题 | 详细信息 |
|
物质的量浓度相同的下列溶液中,NH4+浓度最大的是( ) A.(NH4)2Fe(SO4)2 B.NH3·H2O C.(NH4)2CO3 D.NH4Cl |
|
| 4. 选择题 | 详细信息 |
|
常温下,0.1 mol·L-1的三种盐溶液NaX、NaY、NaZ的pH分别为7、8、9,则下列判断中正确的是 A. HX、HY、HZ的酸性依次增强 B. 离子浓度:c(Z-)>c(Y-)>c(X-) C. 电离常数:K(HZ)>K(HY) D. c(X-)=c(Y-)+c(HY)=c(Z-)+c(HZ) |
|
| 5. 选择题 | 详细信息 |
|
下列事实能说明醋酸是弱电解质的是( ) ①醋酸与水能以任意比互溶;②醋酸溶液能导电;③醋酸稀溶液中存在醋酸分子;④常温下,0.1mol/L醋酸的pH比0.1 mol/L盐酸的pH大;⑤醋酸能和碳酸钙反应放出CO2;⑥0.1 mol/L醋酸钠溶液pH=8.9;⑦大小相同的铁片与同物质的量浓度的盐酸和醋酸反应,醋酸产生H2速率慢 A. ②⑥⑦ B. ③④⑥⑦ C. ③④⑤⑥ D. ①② |
|
| 6. 选择题 | 详细信息 |
|
下列关于反应能量的说法正确的是( ) A.已知Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s) △H=-216kJ/mol,则反应物总能量<生成物总能量 B.已知101 kPa时,2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol,则H2的燃烧热△H=-241.8kJ/mol C.相同的条件下,如果1 mol氢原子所具有的能量为E1,1 mol 氢分子的能量为E2,则2E1>E2 D.H+(aq)+OH-(aq)=H2O(l),含1 mol NaOH的氢氧化钠溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ 的热量 |
|
| 7. 选择题 | 详细信息 |
|
常温下0.1mol•L﹣1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是 A. 将溶液稀释到原体积的2倍 B. 加入适量的醋酸钠固体 C. 加入等体积0.2 mol•L﹣1盐酸 D. 加少量冰醋酸 |
|
| 8. 选择题 | 详细信息 |
|
一定温度下,反应N2(g)+3H2(g) A. 2△H和2K B. -2△H和 K2 C. -2△H和 K-2 D. 2△H和-2K |
|
| 9. 选择题 | 详细信息 |
|
下列对化学平衡移动的分析中,不正确的是 ①已达平衡的反应C(s)+H2O(g) ②已达平衡的反应N2(g)+3H2(g) ③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动 ④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动 A. ①④ B. ①②③ C. ②③④ D. ①②③④ |
|
| 10. 选择题 | 详细信息 |
|
下列反应在常温下均为非自发反应,在高温下仍为非自发的是 A. 2Ag2O(s)=4Ag(s)+O2(g) B. 2Fe2O3(s)+3C(s)=Fe(s)+3CO2(g) C. N2O4(g)=2NO2(g) D. 6C(s)+6H2O(l)=C6H12O6(s) |
|
| 11. 选择题 | 详细信息 |
|
将4molA和2molB放入2L密闭容器中发生反应2A(g)+B(g) ,4s后反应达到平衡状态,此时测得C的浓度为0.6mol/L.下列说法正确的是( ) A.若不断增加A的质量,可使反应放出热量的数值达到2︱ΔH︱ B.4 s内,υ(B)=0.075 mol/(L ·s) C.达到平衡状态后,若只升高温度,则C的物质的量浓度增大 D.达到平衡状态后,若温度不变,缩小容器的体积,则A的转化率降低 |
|
| 12. 选择题 | 详细信息 |
|
已知甲、乙、丙、丁四种溶液分别为CH3COONa、NH3•H2O、CH3COOH、Na2SO4中的一种,相同温度下,甲与乙两种溶液的pH相同,甲与丙两种溶液中的水的电离程度相同,则丙为( ) A. NH3•H2O B. CH3COONa C. CH3COOH D. Na2SO4 |
|
| 13. 选择题 | 详细信息 |
|
25℃时,下列各组离子在指定溶液中一定能大量共存的是( ) A.能使甲基橙变红的溶液中:K+、Mg2+、NO3-、I- B.c(HCO3-)=1 mol·L-1溶液中:Na+、Al3+、SO42-、Cl- C.无色透明的溶液中:Fe3+、Al3+、NO3-、SO42- D.常温下,  =10-10的溶液中:K+、Na+、I-、SO42- =10-10的溶液中:K+、Na+、I-、SO42- |
|
| 14. 选择题 | 详细信息 |
室温下,用 A.该滴定过程应该选择甲基橙作为指示剂 B.从 C. D. |
|
| 15. 实验题 | 详细信息 | ||||||||||||
某学生为了探究锌与盐酸反应过程中速率变化,在100 mL稀盐酸中加入足量的锌粉,标准状况下测得数据累计值如下:
|
|||||||||||||
| 16. 填空题 | 详细信息 |
|
可逆反应3A(g) (1)升高温度,用“变大”、“变小”、“不变”或“无法确定”填空。 a.若B、C都是气体,气体的平均相对分子质量①___; b.若B、C都不是气体,气体的平均相对分子质量②____; c.若B是气体,C不是气体,气体的平均相对分子质量③___; (2)如果平衡后保持温度不变,将容器体积增加一倍,新平衡时A的浓度是原来的60%,则B是④___态,C是⑤___态。 |
|
| 17. 综合题 | 详细信息 | ||||||||||||||||
|
甲醇是一种新型燃料,工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g) (1)已知:CO(g)+ H2(g) + 则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式:________________ (2)在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律。如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。 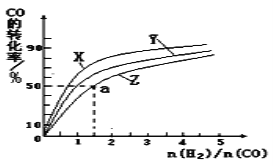 请回答: ①在上述三种温度中,曲线Z对应的温度是_________ ②利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)=CH3OH(g)的平衡常数 K=_________。 ③下列既能提高上述反应中 CO 的平衡转化率,又能增大反应速率的是____(填标号)。 a.增大压强 b.降低温度 c.增大H2浓度 d.加高效催化剂 ④若上述反应在某恒温恒容容器中发生,能说明该反应达到平衡的是____(填标号)。 a.气体平均相对分子质量保持不变 b.△H1保持不变 c. (3)在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol/L)变化如下表所示:
|
|||||||||||||||||
| 18. 综合题 | 详细信息 | |||||||||||||||
25 ℃时,电离平衡常数:
回答下列问题: |
||||||||||||||||
| 19. 填空题 | 详细信息 |
|
(10分)(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是________。 A. KMnO4B. H2O2C. Cl2水 D. HNO3 然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________。 A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2 (2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为________,Fe3+完全沉淀时溶液的pH为________,通过计算确定上述方案________(填“可行”或“不可行”)。 |
|




