2017山西高二下学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
下列说法中正确的是( ) A.基态原子是处于最低能量状态的原子 B.基态C原子的电子排布式是1s22s12p3 C.焰色反应是金属原子的电子从基态跃迁到激发态时产生的光谱 D.同一原子处于激发态时的能量一定低于基态时的能量
|
|
| 2. | 详细信息 |
|
下列各项中的X和Y两种原子,化学性质—定相似的是( ) A.X原子和Y原子最外层只有一个电子 B.X原子的核外电子排布为1s2,Y原子的3p核外电子排布为1s22s2 C.X原子的2p能级上有三个电子,Y原子的3p能级上有三个电子 D.X原子核外M层上仅有两个电子,Y原子核外N层上仅有两个电子
|
|
| 3. | 详细信息 |
|
已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( ) A.质子数c>d,离子的还原性:Y2->Z- B.氢化物的稳定性:H2Y>HZ C.原子半径X<W,第一电离能X<W D.电负性Z>Y>W>X
|
|
| 4. | 详细信息 |
|
某化学学习小组在学习元素周期系和周期的划分时提出了以下观点: ①周期系的形成是由原子的结构决定的;②元素周期系中IA族元素统称为碱金属元素属于s区;③每一周期的元素原子外围电子排布均是从 ns1开始至ns2np6结束;④元素周期系的每一周期元素的种类均相等;⑤基态原子核外电子排布为:1s22s22p3 和1s22s22p63s23p3 的两元素的原子位于同一周期;⑥周期序号越大,该周期所含金属元素一般越多。你认为正确的是( ) A.①⑥ B.①②③⑤⑥ C.①④⑥ D.②③⑤
|
|
| 5. | 详细信息 |
|
用R代表短周期元素,R原子最外层的p能级上的未成对电子只有2个。下列关于R的描述中正确的是( ) A.R的氧化物都能溶于水 B.R的最高价氧化物对应的水化物都是H2RO3 C.R都是非金属元素 D.R的氧化物都能与NaOH溶液反应
|
|
| 6. | 详细信息 |
|
下列关于原子核外电子排布与元素在周期表中的位置关系的表述中,正确的是( ) A.原子的价电子排布为ns2np1~6的元素一定是主族元素 B.基态原子的p能级上有5个电子的元素一定是ⅦA族元素 C.原子的价电子排布为(n-1)d6-8ns2的元素一定位于ⅢB~ⅦB族 D.基态原子的N层上只有1个电子的元素一定是主族元素
|
|
| 7. | 详细信息 |
|
下列叙述中,正确的是( ) A.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子 B.在一个基态多电子的原子中,不可能有两个能量完全相同的电子 C.在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高 D.如果某一基态3p能级上仅有2个电子,它们自旋方向必然相反
|
|
| 8. | 详细信息 |
|
下列说法正确的是:( ) A.分子中一定存在共价键 B.在共价化合物分子中一定存在σ键 C.Na3、Na2和Cl2的配位数都是6 D.共价键键长越短,键能一定越大
|
|
| 9. | 详细信息 |
|
用价层电子对互斥理论可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,下列判断正 确的是:( ) A.SO2、CS2、HI都是直线形的分子 B.BF3键角为120°,SnBr2键角大于120° C.COCl2、BF3、SO3都是平面三角形分子 D.PCl3、NH3、PCl5都是三角锥形的分子
|
|
| 10. | 详细信息 |
|
下列说法正确的是:( ) ①非极性分子中一定含有非极性键; ②s-sσ键与s-pσ键的电子云形状相同; ③含有π键的化合物与只含σ键的化合物的化学性质不同; ④中心原子采取sp3杂化的分子,其立体构型不一定是正四面体; ⑤氢键不仅存在于分子之间,有时也存在于分子内; ⑥3p2表示3p能级有两个轨道 A.③④⑤ B.①②③④⑤ C.②③④ D.②③④⑤⑥
|
|
| 11. | 详细信息 |
|
下列分子中所有原子都满足最外层8电子结构的是( ) A.光气(COCl2) B.六氟化硫 C.二氟化氙 D.三氟化硼
|
|
| 12. | 详细信息 |
|
下列各组微粒的空间构型相同的是①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2⑤CO2 和BeCl2 ⑥SiO44-和SO42- ⑦BF3和Al2Cl6( ) A.全部 B.除④⑥⑦以外 C.③④⑤⑥ D.②⑤⑥
|
|
| 13. | 详细信息 |
|
下列物质中不存在氢键的是( ) A.冰醋酸中醋酸分子之间 B.液态氟化氢中氟化氢分子之间 C.一水合氨分子中的氨分子与水分子之间 D.可燃冰(CH4·8H2O)中甲烷分子与水分子之间
|
|
| 14. | 详细信息 |
|
通常情况下,原子核外P能级、d能级等原子轨道上电子排布为“全空”“半充满”“全充满”的的时 候一般更加稳定,称为洪特规则的特例,下列事实能作为这个规则证据的是( ) ①元素氦(He)的第一电离能远大于元素氢(H)的第一电离能 ②Fe2+容易失电子转变为Fe3+,表现出较强的还原性 ③基态铜(Cu)原子的电子排布式为3d104s1而不是3d94s2 ④某种激发态碳(C)原子电子排布式为1s22s12p3而不是1s22s22p2 A.①② B.②③ C.③④ D.全部
|
|
| 15. | 详细信息 |
|
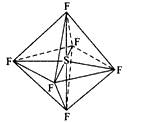
六氟化硫分分子呈八面体型(如图所示),在高电压下仍有良好的绝缘性,在电器工业方面有着广泛 的用途,但逸散到空气中会引起温室效应,下列有关六氟化硫的推测正确的是( )
A.六氟化硫易燃烧生成二氧化硫 B.六氟化硫中各原子均达到8电子稳定结构 C.六氟化硫分子中的S-F键都是σ键,且键长、键能都相等
|
|
| 16. | 详细信息 |
|
有放射性的同位素称之为稳定同位素,近20年来,稳定同位素分析法在植物生理学、生态学和环境科学研究中获得广泛应用,如在陆地生态系统研究中,2H、13C、15N、18O、34S等常用作环境分析指示物。 下列说法正确的是( ) A.34S原子核内中子数为16 B.1H216O 在相同条件下比1H218O更易蒸发 C.13C和15N原子核内的质子数相差2 D.2H+的酸性比1H+的酸性更强
|
|
| 17. | 详细信息 |
|
根据等电子原理判断,下列说法中错误的是( ) A.B3N3H6分子中所有原子均在同一平面上 B.B3N3H6分子中存在双键,可发生加成反应 C.H3O+和NH3是等电子体,均为三角锥形 D.CH4和NH4+是等电子体,均为正四面体形
|
|
| 18. | 详细信息 |
|
固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,则下列 有关说法中,不正确的是( ) A.NH5中既有共价键又有离子键 B.NH5的熔、沸点高于 NH3 C.NH5固体投入少量水中,可产生两种气体 D.1 mol NH5中含有5molN-H键
|
|
| 19. | 详细信息 |
|
0.01 mol氯化铬(CrCl3· 6H2O)在水溶液中用过量AgNO3处理,产生0.02 mol AgCl沉淀,此氯化铬最可能为( ) A.Cl3 B.Cl2·H2O C.Cl·2H2O D.·3H2O
|
|
| 20. | 详细信息 |
|
当向蓝色的硫酸铜中逐滴加入氨水,观察到溶液呈深蓝色时,再通入SO2气体,生成了白色沉淀。将白色沉淀加入稀硫酸中,又生成了红色粉末状固体和SO2气体,同时溶液呈蓝色。根据上述实验现象分析推测,下列描述正确的是( ) A.Cu2+和Ag+相似,能与NH3结合生成铜氨配离子 B.白色沉淀为+2价铜的某种亚硫酸盐,溶于H2SO4发生复分解反应 C.白色沉淀为+1价铜的某种硫酸盐,在酸性条件下发生了自身氧化还原反应 D.反应过程中消耗的SO2与生成的SO2的物质的量相等
|
|
| 21. | 详细信息 |
|
(I)(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况,试判断哪些违反了泡利原理____________,哪些违反了洪特规则_______________。哪些既没有违反泡利原理又没有违反洪特规则_______________。
(Ⅱ)等电子原理:原子数相同、最外层电子总数相同的分子互称为等电子体。等电子体的结构相似、物理性质相近。 (1)根据上述原理,仅由第二周期元素组成的分子中,互为等电子体的是:______和______;______和______. (2)此后,等电子原理又有所发展.例如,由短周期元素组成的粒子,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征.在短周期元素组成的物质中,与NO2-互为等电子体的分子有:______、______.
|
|
| 22. | 详细信息 |
|
A、B、C、D、E、F、G均是原子序数小于36的元素。A的基态原子外围电子排布式为3s2;B原子的L电子层的层的P能级上有一个空轨道;C元素的基态原子最外层有3个未成对电子,次外层有2个电子;D 的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;E是海水中除氢、氧元素外含量最多的元素;F和G在周期表中既处于同一周期又位于同一族,且原子序数F比G小2。学。 根据信息回答下列问题: (1)C的外围电子排布图为_____。C与氢元素可分别形成含10个电子的分子、阴离子和阳离子,阳离子中中心原子的杂化类型为______;分子的VSEPR模型名称为________;阴离子的立体构型为_________。 (2)G的价电子排布式为_______ 。 (3)F与BD易形成配合物F(BD)5,在F(BD)5中F的化合价为_______;与BD分子的结构式为__________1mol分子中含有_______molπ键 (4)E有多种含氧酸根①EO- ②EO2- ③EO3- ④EO4-,其中空间构型为四面体型的是___。(填序号) (5)B、C、D、E原子两两相互化合形成的分子有多种,请列举两种分子内所有原子都满足最外层8电子稳定结构的分子:_________(写分子式)
|
|
| 23. | 详细信息 |
|
根据周期表对角线原则,金属Be与铝单质及其化合物的性质相似,又知AlCl3熔、沸点较低,易升华,试回答下列问题: (1)写出Be与NaOH溶液反应的离子方程式_________。Be2+、Li+、H+ 微粒半径从小到大的顺序为:______; (2)Be(OH)2和Mg(OH)2可用试剂______鉴别;其离子方程式为____________。 (3)BeCl2是______(填“离子化合物”或“共价化合物”), BeCl2水溶液呈酸性,水解的离子方程式为__________。
|
|
| 24. | 详细信息 |
|
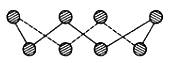
第ⅥA族的氧、硫、硒、碲等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题: (1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是_____;
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为_______; (3)Se原子序数为____,其核外M层电子的排布式为____; (4)H2Se的酸性比H2S___(填“强”或“弱”)。气态SeO3分子的立体构型为___,SO32-离子的立体构型为______;SO32-离子中S原子的杂化方式为____________。
|
|
| 25. | 详细信息 |
|
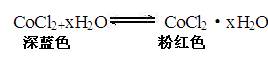
(I)无水CoCl2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水CoCl2,故常在实验室中用作吸湿剂和空气湿度指示剂。
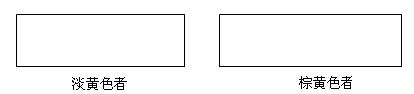
现有65g无水CoCl2,吸水后变成CoCl2·xH2O 119g。 (1)水合物中x=______; (2)若该化合物中Co2+的配位数为6,而且经测定得知内界和外界占有Cl-的个数比为1:1,则其化学式可表示为: ______ (Ⅱ)在极性分子中,正电荷中心同负电荷中心间的距离称为偶极长,通常用d表示。极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极矩(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题: (3)治癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上。已知该化合物有两种异构体,棕黄色者μ>0,淡黄色者μ=0。 ①试在方框中画出两种异构体的构型图:_________;___________________
②该化合物的两种异构体在水中溶解度较大的是___________________(填“棕黄色者”或“淡黄色者”)。
|
|