2018高一上学期人教版高中化学期中考试
| 1. | 详细信息 |
|
下列实验能达到目的的是( ) A. 将蒸发皿放置在铁架台的铁圈上的石棉网加热 B. 加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铁粉 C. 用玻璃棒搅拌漏斗中的液体以加快过滤的速度 D. 加入盐酸以除去硫酸钠中的少量碳酸钠杂质
|
|
| 2. | 详细信息 |
|
下列物质类型中,前者包括后者的是( ) A.氧化物、化合物 B.化合物、电解质 C.溶液、胶体 D.溶液、分散系
|
|
| 3. | 详细信息 |
|
研究表明:多种海产品如虾、蟹、牡蛎等,体内含有+5价的砷(As)元素,但它对人体是无毒的,砒霜的成分是As2O3,属剧毒物质,专家忠告:吃饭时不要同时大量食用海鲜和青菜,否则容易中毒,并给出了一个公式:大量海鲜+大量维生素C=砒霜.下面有关解释不正确的应该是( ) A. 青菜中含有维生素C B. 维生素C具有还原性 C. 致人中毒过程中砷发生还原反应 D. 砒霜是氧化产物
|
|
| 4. | 详细信息 |
|
下列叙述正确的是( ) A.固体氯化钠不导电,所以氯化钠不是电解质 B.铜丝能导电,所以铜是电解质 C.氯化氢水溶液能导电,所以氯化氢是电解质 D.SO3 溶于水能导电,所以 SO3 是电解质
|
|
| 5. | 详细信息 |
|
为使以面粉为原料的面包松软可口,通常用NaHCO3作发泡剂,因为它( ) ①热稳定性差 ②增加甜味 ③产生二氧化碳 ④提供钠离子 A.②③ B.①③ C.①④ D.③④
|
|
| 6. | 详细信息 |
|
下列各组物质中所含分子数一定相同的是( ) A.5.6L N2和11g CO2 B.5g CO和5g H2 C.含1mol H原子的H2O和0.5mol Br2 D.质子数相等的NH3和HCl
|
|
| 7. | 详细信息 |
|
在碱性溶液中,下列各项中的离子可以大量共存的是( ) A.Fe3+、Cu2+ 、Cl-、NO3- B.K+、NO3-、Ag+、Cl- C.Na+、SO42-、K+、Cl- D.Ca2+、MnO4-、Na+、CO32-
|
|
| 8. | 详细信息 |
|
在3NO2+H2O=2HNO3+NO中,氧化剂与还原剂的分子个数比为( ) A.2︰1 B.1︰2 C.3︰1 D.1︰3
|
|
| 9. | 详细信息 |
|
当溶液中有大量的H+和Ba2+时,下列离子中有可能大量存在的是( ) A.SO
|
|
| 10. | 详细信息 |
|
使用胆矾(CuSO4·5H2O)配制1L 0.2 mol·L-1的硫酸铜溶液,正确的操作是( ) A.将胆矾加热除去结晶水后,称取32 g溶解在1 L水里 B.称取胆矾50 g,溶解在1 L水里 C.将32 g胆矾溶于水,然后将此溶液稀释至1 L D.将50 g胆矾溶于水,然后将此溶液稀释至1 L
|
|
| 11. | 详细信息 |
|
下列反应的离子方程式书写正确的是( ) A.钠和冷水反应Na+2H2O=Na++2OH-+H2↑ B.金属铝溶于氢氧化钠溶液Al+2OH-=AlO2-+H2↑ C.金属铝溶于盐酸中2Al+6H+=2Al3++3H2↑ D.铁跟稀硫酸反应2Fe+6H+=2Fe3++3H2↑
|
|
| 12. | 详细信息 |
|
将金属钠投入饱和MgCl2溶液中,下列现象合理的是( ) A.开始时,钠浮在液面上、四处游动并熔成小球 B.反应结束后,在溶液底部有银白色金属产生 C.反应结束后,在溶液中无沉淀生成 D.反应结束后,在溶液底部析出黑色固体
|
|
| 13. | 详细信息 |
|
在①Al ②Al2O3 ③Al(OH)3 ④NaHCO3四种物质中,既能与硫酸反应又能和氢氧化钠反应的化合物是( ) A. ②③④ B. ①②③④ C. ①③④ D. ①②④
|
|
| 14. | 详细信息 |
|
下列反应的离子方程式书写正确的是( ) A. 氯化铁溶液与碘化钾溶液反应:Fe3++2I-===Fe2++I2 B. 硫酸溶液与氢氧化钡溶液反应:Ba2++SO C. 醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+===Ca2++H2O+CO2↑ D. 氯化铝溶液与过量氨水反应:Al3++3NH3·H2O===Al(OH)3↓+3NH
|
|
| 15. | 详细信息 |
|
金属加工后的废切削液中含质量分数为2%~5%的NaNO2,它是一种环境污染物。人们用NH4Cl溶液来处理此废切削液,使NaNO2转化为无毒物质,该反应分两步进行: 第一步:NaNO2+NH4Cl===NaCl+NH4NO2;第二步:NH4NO2===N2↑+2H2O。 下列对第二步反应的叙述中,正确的是( ) ①NH4NO2是氧化剂;②NH4NO2是还原剂;③NH4NO2发生了分解反应;④只有氮元素的化合价发生了变化;⑤NH4NO2既是氧化剂又是还原剂。 A.①③ B.①④ C.②③④ D.③④⑤
|
|
| 16. | 详细信息 |
|
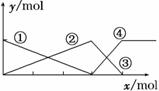
右图表示AlCl3溶液与NaOH溶液相互滴加混合,由图中判断错误的是( )
A.①线表示Al3+物质的量的变化 B.x表示AlCl3的物质的量 C.③线表示Al(OH)3物质的量的变化 D.④线表示AlO
|
|
| 17. | 详细信息 | ||||||||||||||||
|
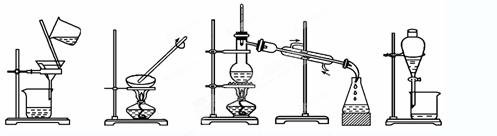
(1)下列实验需要在哪套装置中进行:(填序号,每套装置仅使用一次)
① ② ③ ④ 从海水中提取水:____________;从KCl溶液中获取KCl晶体:____________; 分离CaCO3和水:____________;分离植物油和水:____________。 (2)现有甲、乙两瓶无色溶液,已知它们可能为AlCl3溶液和NaOH溶液。现分别将一定体积的甲、乙两溶液混合,具体情况如下表所示,请回答:
①甲瓶溶液为________溶液。 ②乙瓶溶液为________溶液,其物质的量浓度为________mol·L-1。
|
|||||||||||||||||
| 18. | 详细信息 |
|
(1)向AlCl3溶液中,滴加少量NaOH溶液,现象是 继续滴加NaOH溶液至过量,现象是 。 (2)钠与水反应的离子方程式为 ,该反应中氧化剂是 ,产生1mol H2时,转移电子的物质的量为 mol。 (3)经常有人因误食亚硝酸钠(NaNO2)而中毒。原因是NaNO2像食盐一样既有咸味,又有很强毒性。已知亚硝酸钠能发生如下反应: 2NaNO2+4HI=2NO+I2+2NaI+2H2O㈤ ①该反应的氧化剂是_______,被氧化的是_________元素。 ②若此反应中电子转移数目为0.5mol,则被氧化的还原剂的物质的量为___________。
|
|
| 19. | 详细信息 |
|
国际化学年的中国宣传口号是“化学-----我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”道理。请填空: (1)①若金属钠等活泼金属着火时,应该 用来灭火。 ②经火焰灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)的元素是。 ③胃舒平(含有氢氧化铝)可治疗胃酸过多,其反应的离子反应方程式为: 。 ④明矾能净水,其电离方程式是 。 (2)过氧化钠作潜艇供氧剂时发生的化学反应方程式是_____________。 (3)加热Al片的实验现象是_________________,原因是_____________。 |
|
| 20. | 详细信息 |
|
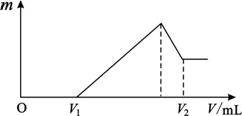
将镁、铝的混合物共0.2mol,溶于200mL4mol·L—1的盐酸溶液中,然后再滴加2mol·L—1的NaOH溶液。请回答下列问题:
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化情况如图所示。当V1=160mL时,则金属粉末中n(Mg)= mol; (2)0~V1段发生的反应的离子方程式为 ; (3)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+ 刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)= mL; (4)试计算V2的值: V2= mL。
|
|