从江县第一民族中学高二化学期末考试(2019年上学期)同步练习
| 1. 选择题 | 详细信息 |
|
下列各组物质中分子数相同的是 A. 2 L一氧化碳和2 L 二氧化碳 B. 9 g水和标准状况下11.2 L二氧化碳 C. 标准状况下1 mol氧气和22.4 L水 D. 0.2 mol 氢气和4.48 L氯化氢气体 |
|
| 2. 选择题 | 详细信息 |
|
已知某强氧化剂 A. -1 B. 0 C. +1 D. +2 |
|
| 3. 选择题 | 详细信息 |
|
下列说法正确的是 A. 二氧化硫和漂白粉都具有漂白作用,它们都能使溴水和高锰酸钾溶液褪色 B. 过氧化钠和二氧化硫都具有漂白作用,它们都能使品红溶液褪色 C. 二氧化硫和氯气都具有漂白作用,它们都能使石蕊试液先变红色再褪色 D. 盐酸能使滴有酚酞的氢氧化钠溶液褪色,所以盐酸也有漂白性 |
|
| 4. 选择题 | 详细信息 |
|
将饱和的氯化铁溶液分别滴加到下列液体中,能制备氢氧化铁胶体的是 A. 冷的自来水 B. 加热至沸的蒸馏水 C. 氢氧化钠溶液 D. 浓氨水 |
|
| 5. 选择题 | 详细信息 |
|
下列关于过滤和蒸发说法中不正确的是 A. 过滤是从液体中分离出难溶物质的实验方法 B. 蒸发是减少溶剂,让溶质析出的实验方法 C. 过滤和蒸发实验中都用到的玻璃仪器是烧杯 D. 加热蒸发可以使溶液浓缩或溶质结晶析出 |
|
| 6. 选择题 | 详细信息 |
|
t℃时CuSO4的溶解度是Sg,其饱和溶液密度为dg·cm-3,物质的量浓度为cmol·L-1。向足量饱和溶液中加入mg无水CuSO4或蒸发掉ng水后恢复t℃,均能获得Wg胆矾晶体,下列关系式正确的是 A. c= C. m= |
|
| 7. 选择题 | 详细信息 |
|
用容量瓶配制一定物质的量浓度的NaCl溶液的实验中,会使所配溶液浓度偏高的是 A. 定容时加水加多了,用滴管吸出溶液至刻度线 B. 定容时仰视刻度线 C. 没有洗涤溶解NaCl固体的烧杯和玻璃棒 D. 称量NaCl固体时砝码上有杂质 |
|
| 8. 选择题 | 详细信息 |
|
下列关于元素周期表的说法中不正确的是( ) A. 同一横行元素性质基本相同 B. 同一横行元素原子序数从左到右依次递增 C. 同一纵行元素最外层电子数相同 D. 同一纵行元素电子层数自上而下依次递增 |
|
| 9. 选择题 | 详细信息 |
A、B、C三种元素在周期表中的位置如下图所示,已知A、B、C原子序数之和为37。下列关于A、B、C三种元素的说法正确的是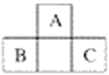 A. 元素B和C位于第四周期 B. 元素A的原子序数为7 C. 元素B最外层有5个电子 D. 元素C位于第三周期ⅤA族 |
|
| 10. 选择题 | 详细信息 |
|
世界上60%的镁是从海水中提取的,其主要步骤如下: ①把贝壳制成生石灰; ②在海水中加入生石灰,过滤,洗涤沉淀物; ③将沉淀物与盐酸反应,结晶、过滤; ④在氯化氢热气流中加热晶体; ⑤电解上述所得盐(熔融条件下) 下列说法中,不正确的是 A. 向最后一次洗涤液中滴加碳酸钠溶液可检验沉淀是否洗涤干净 B. 上述变化过程中包括了分解、化合、复分解三种反应类型 C. 步骤⑤也可以采用电解该盐水溶液的方法 D. 为节省原料、减少污染,在提取镁的工业流程中使用了物质循环的过程 |
|
| 11. 选择题 | 详细信息 |
|
比较归纳是化学学习常用的一种方法。对以下三种物质的转化关系,①C→CO2;②CH4→CO2;③CO→CO2,比较归纳正确的是 A. 三种转化关系中发生的反应都属于化合反应 B. 三种转化关系中所有的生成物在常温下都是气体 C. 三种物质都只能跟氧气反应转化为二氧化碳 D. 三种物质都能在点燃条件下转化为二氧化碳 |
|
| 12. 选择题 | 详细信息 |
利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示。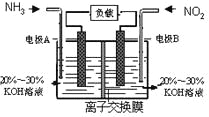 下列说法不正确的是 A. 电流从右侧电极经过负载后流向左侧电极 B. 为使电池持续放电,离子交换膜需选用阴离子交换膜 C. 电极A极反应式为:2NH3-6e-=N2+6H+ D. 当有4.48LNO2(标准状况) 被处理时,转移电子为0.8mol |
|
| 13. 选择题 | 详细信息 |
|
下列说法不正确的是 A. 煤的干馏和石油分馏都是物理变化 B. 石油主要是由多种烃组成的混合物 C. 石油分馏得到的汽油是混合物 D. 石油主要含有碳、氢两种元素 |
|
| 14. 选择题 | 详细信息 |
|
下列各糖能发生水解,且属于还原性糖的是 A. 葡萄糖 B. 蔗糖 C. 麦芽糖 D. 纤维素 |
|
| 15. 选择题 | 详细信息 |
|
下列说法正确的是 A. 氢原子光谱是所有元素的光谱中最简单的光谱之一 B. “量子化”就是不连续的意思,微观粒子运动均有此特点 C. 玻尔理论不但成功解释了氢原子光谱,而且还推广到其他原子光谱 D. 原子中电子在具有确定半径的圆周轨道上像火车一样高速运转着 |
|
| 16. 选择题 | 详细信息 |
|
下列各组微粒,没有按照半径由小到大顺序排列的是 A. Cl、Na、F、K B. F、Cl、Na、K C. Ca2+、K+、Cl-、S2- D. Na+、K+、Cl-、Br- |
|
| 17. 选择题 | 详细信息 |
|
下列各组晶体物质中,化学键类型相同,晶体类型也相同的是 ( )。 ①SiO2和SO3②晶体硼和HCl ③CO2和SO2④晶体硅和金刚石 ⑤晶体氖和晶体氮 ⑥硫磺和碘 A. ①②③ B. ④⑤⑥ C. ③④⑥ D. ①③⑤ |
|
| 18. 选择题 | 详细信息 |
|
下列基态原子的价电子排布式中,正确的是 A. 3d94s2 B. 3d44s2 C. 3d104s0 D. 3d84s2 |
|
| 19. 选择题 | 详细信息 |
|
在BrCH=CHBr分子中,C—Br键采用的成键轨道是 A.sp—p B.sp2—s C.sp2—p D.sp3—p |
|
| 20. 选择题 | 详细信息 |
|
下列说法中,不正确的是 A. 金属晶体中一定含有金属键 B. 在含有阳离子的化合物的晶体中,一定含有阴离子 C. 含有金属元素的离子不一定是阳离子 D. 金属晶体中原子的堆积方式都是A3或A1型最密堆积 |
|
| 21. 选择题 | 详细信息 |
|
下列说法正确的是 A. NaOH是含有非极性共价键的离子晶体 B. 氯化钠与氯化铯的晶体结构完全相同 C. 金刚石、硅、锗的熔点和硬度依次降低 D. NaF、MgF2、AlF3三种离子晶体的晶格能逐渐减小 |
|
| 22. 选择题 | 详细信息 |
如图是CaF2晶胞的结构。下列说法正确的是 A.一个CaF2晶胞中含有8个Ca2+ B.一个CaF2晶胞中含有8个F- C.在CaF2晶胞中Ca2+的配位数为4 D.在CaF2晶胞中F-的配位数为8 |
|
| 23. 选择题 | 详细信息 |
|
下列固态物质中,含有共价键的离子晶体是 A. KBr B. NaOH C. HCl D. I2 |
|
| 24. 选择题 | 详细信息 |
|
金属的下列性质中,不能用金属的电子气理论加以解释的是 A. 易导电 B. 易导热 C. 易腐蚀 D. 有延展性 |
|
| 25. 选择题 | 详细信息 |
|
下列关于苯分子结构或性质的描述错误的是 ( ) A. 苯分子呈平面正六边形,六个碳碳键完全相同,键角皆为120° B. 苯分子中的碳原子采取sp2杂化,6个碳原子中未参与杂化的2p轨道以“肩与肩”形式形成一个大π键 C. 苯分子中的碳碳键是介于单键和双键之间的一种特殊类型的键 D. 苯能使溴水和酸性KMnO4溶液因发生化学反应而褪色 |
|
| 26. 推断题 | 详细信息 |
已知由短周期元素构成的三种粒子:甲a(单核带一个单位正电荷)、乙I(四核不带电荷)、丙e(双核带一个单位负电荷),它们都有10个电子。物质A由甲、丙构成,B、C、D、K都是单质,反应①~⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如下图所示: 请填写下列空白: (1)写出下列物质的化学式:B________,I________,J________。 (2)A的化学式是__________________。 (3)写出下列反应的离子方程式: ①H+E(溶液)→M_________________________________________________________。 ②I溶于G_______________________________________________________。 (4)写出反应④的化学方程式____________________________________________。 |
|
| 27. 填空题 | 详细信息 |
如图是甲醛分子的模型,根据该图和所学化学知识回答下列问题: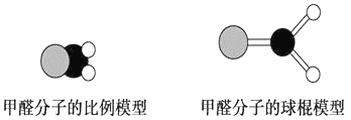 (1)甲醛分子中碳原子的杂化方式是__________,作出该判断的主要理由是__________________________。 (2)下列是对甲醛分子中碳氧键的判断,其中正确的是________(填序号)。 ①单键 ②双键 ③σ键 ④π键 ⑤σ键和π键 (3)甲醛分子中C—H键与C—H键间的夹角________(填“=”、“>”或“<”)120°,出现该现象的主要原因是____________________________________________。 |
|
| 28. 实验题 | 详细信息 |
|
海洋植物如海带和海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋中提取碘的流程如下: 某化学兴趣小组将上述流程②、③设计成如下图所示操作。 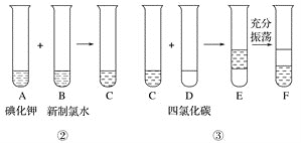 已知过程②发生反应的化学方程式为Cl2+2KI===2KCl+I2 回答下列问题: (1)写出提取过程①、③中实验操作的名称:①____________,③____________。 (2)在灼烧过程中,使用到的实验仪器有酒精灯、____________、____________(除泥三角外)。 (3)F中下层液体的颜色为________色,上层液体中溶质的主要成分为____________。 (4)从F中得到固态碘还需进行的操作是_______________________________________。 |
|
| 29. 综合题 | 详细信息 |
明矾[KAl(SO4)2·12H2O]是一复盐,在造纸等方面应用广泛。某兴趣小组采用10.0g废易拉罐(含90%的Al,还含有少量的Fe、Mg等杂质)制备明矾的实验方案如下: (1)试剂①应选用_____________(填代号)。 a.盐酸 b.H2SO4溶液 c.氯化钠溶液 d.NaOH溶液 (2)易拉罐溶解过程中主要反应的化学方程式为____________________。 (3)溶液B中溶质的主要成分为____________________ (填化学式)。 (4)从溶液C中得到明矾的实验操作步骤为蒸发浓缩、__________(填操作名称)、过滤、洗涤、干燥。如下图所示,蒸发操作中的一处错误是_____________。 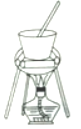 (5)该小组在实验完成之后,得到118.5 g明矾,则明矾的回收率为_____________。(已知:明矾的摩尔质量为474g·mol-1) |
|
| 30. 实验题 | 详细信息 |
已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题: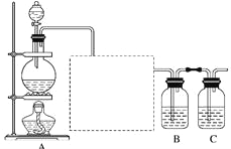 (1)装置A的分液漏斗中盛装的试剂是____________,烧瓶中发生的反应的化学方程式是______________________。 (2)画出虚线框内的实验装置图,所加试剂为____________,该装置的作用是__________________。 (3)装置B中盛放的试剂是____________(填序号),实验现象为____________________________,该反应的离子方程式是____________________________,该反应属于四种基本反应类型中的__________反应。 A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液 (4)已知:①硫酸比次氯酸稳定;②高氯酸的酸性比硫酸强;③S2-比Cl-易被氧化;④HCl比H2S稳定;⑤铜与盐酸不反应,但能与浓硫酸反应;⑥铁与氯气在加热条件下反应生成三氯化铁,铁与硫在加热条件下反应生成硫化亚铁;⑦硫原子与氯原子的电子层数相同,氯的原子半径小于硫原子。能说明氯的非金属性比硫强的是________(填序号)。 A.全部 B.②③④⑥⑦ C.①②④⑤⑥ D.②③④⑤⑥⑦ (5)装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气,写出该装置中所发生反应的离子方程式:________________________。 |
|
| 31. 填空题 | 详细信息 |
|
已知和碳元素同主族的X元素位于周期表中的第1个长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们形成的化合物的分子是XY4。 试回答: (1)X元素原子的基态电子排布式为______________________________________; Y元素原子最外层电子的电子排布图为__________________________________。 (2)若X、Y两元素电负性分别为2.1和2.85,则XY4中X与Y之间的化学键为________(填“共价键”或“离子键”)。 (3)该化合物的空间结构为____________,中心原子的杂化类型为________,分子为________(填“极性”或“非极性”)分子。 (4)该化合物在常温下为液体,它存在的分子间作用力是________。 (5)该化合物的沸点与SiCl4的比较,________(填化学式)的高,原因是__________ 。 |
|
高中化学 试卷推荐
- 2017-2018年高一上学期第二次阶段性检测化学考题带答案和解析(湖南省长沙市第一中学)
- 2017-2018年高一上学期第二次月考化学考题带答案和解析(河南省商丘市第一高级中学)
- 2017届高一上第三次月考化学试卷(安徽省淮北一中)
- 高中化学人教版 选修三 第3章 晶体结构与性质 金属晶体的原子堆积模型
- 2017-2018年高二12月月考化学考卷带参考答案和解析(安徽省铜陵市第一中学)
- 2017,2018年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 高中化学人教版 选修三 第3章 晶体结构与性质 分子晶体
- 2018届高三上学期第四次检测理综化学在线测验(四川省南充高级中学)
最近更新



