2018山东高一上学期鲁科版高中化学期中考试
| 1. | 详细信息 |
|
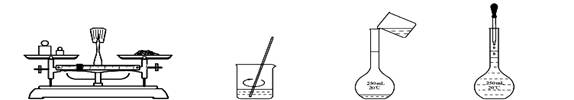
下列有关实验操作正确的是
|
|
| 2. | 详细信息 |
|
用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移、定容等操作。下列图示对应的操作规范的是
A B C D
|
|
| 3. | 详细信息 |
|
要除去氯化钠溶液中含有的少量碳酸钠,可采用的方法是 A.通入适量的CO2 B.加入过量的BaCl2溶液 C.加入适量的稀盐酸 D.加入过量的稀硝酸
|
|
| 4. | 详细信息 |
|
进行化学实验时必须注意安全,下列说法不正确的是( ) ①不慎将酸溅到眼中,应立即用大量水冲洗,边洗边眨眼睛 ②不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 ③不慎将浓盐酸洒在桌面上,应立即用浓氢氧化钠溶液冲洗 ④配制稀硫酸时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 ⑤酒精灯着火时可用水扑灭 A.①②③ B.②③④ C.③④⑤ D.全部
|
|
| 5. | 详细信息 |
|
下列说法正确的是 A.在任何条件下,1mol的任何气体的体积都是22.4L。 B.把1molNaCl溶于1L水中,所得NaCl溶液的物质的量浓度为1mol/L。 C.在标准状况下,1mol的任何气体的体积都是 22.4L。 D.同温同体积的O2和N2的分子数目一定相等。
|
|
| 6. | 详细信息 |
|
下列离子在溶液中可大量共存,形成无色溶液的一组是 A. K+、Na+、OH-、Cl- B. Ba2+、Fe2+、NO3-、SO42- C. H+、Na+、CO32-、SO42- D. H+、Ba2+、NO3-、OH-
|
|
| 7. | 详细信息 |
|
下面的离子方程式正确的是 A.碳酸钙和稀盐酸: CO32- + 2H+===CO2 ↑+ H2O B.Ba(OH)2溶液中加入CuSO4溶液: Ba2+ + SO42-===BaSO4↓ C.铁与稀盐酸反应: 2Fe + 6H+ = 2Fe3++ 3H2↑ D.锌与硫酸铜溶液反应: Zn + Cu2+ = Zn2+ + Cu
|
|
| 8. | 详细信息 |
|
1L 1mol /L FeCl3溶液与0.4L 1mol/L KCl溶液中的Cl-的物质的量浓度之比 A.5∶2 B.3∶1 C.15∶2 D.1∶3
|
|
| 9. | 详细信息 |
|
下列物质的水溶液中,加入Ba(OH)2溶液后原溶液中阴、阳离子都减少的是 A.Na2CO3 B.FeCl3 C.CuSO4 D.Ca(NO3)2
|
|
| 10. | 详细信息 |
|
下列离子反应不能发生的是 A.HCl+NaOH====NaCl+H2O B.AgNO3+NaCl====AgCl↓+NaNO3 C.KHCO3+HCl====KCl+CO2↑+H2O D.2HCl+Na2SO4====2NaCl+H2SO4
|
|
| 11. | 详细信息 |
|
2016年9月27日,宁夏石嘴山一煤矿发生瓦斯爆炸,造成18人死亡。某同学查阅资料知,瓦斯中甲烷与氧气的质量比为1:4时极易爆炸,则此时甲烷与氧气的体积比 A.1∶1 B.1∶2 C.1∶4 D.2∶1
|
|
| 12. | 详细信息 |
|
下列电离方程式正确的是 A.Na2CO3====Na+ + CO32- B.Ca(NO3)2====Ca2+ + NO32-
|
|
| 13. | 详细信息 |
|
下列物质中,属于混和物的是 A.硫酸 B.液氯 C.盐酸 D.CuSO4·5H2O
|
|
| 14. | 详细信息 |
|
在容量瓶上无须有标记的是 A.温度 B.浓度 C.刻度线 D.容量
|
|
| 15. | 详细信息 |
|
朱自清先生在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里…月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影…”。关于月光穿过薄雾所形成的种种美景的说法不正确的是 A.空气中的小水滴颗粒大小约为10﹣9m~10﹣7m B.光是一种胶体 C.雾是一种胶体 D.发生丁达尔效应
|
|
| 16. | 详细信息 |
|
下列各组混合物中,能用分液漏斗进行分离的是 A.酒精和水 B.碘和四氯化碳 C.水和四氯化碳 D.汽油和植物油
|
|
| 17. | 详细信息 |
|
在制取蒸馏水的蒸馏实验中,下列叙述不正确的是 A. 在蒸馏烧瓶中盛约 B. 将温度计水银球插入自来水中 C. 冷水从冷凝管下口入,上口出 D. 取少量收集到的液体,滴入硝酸银和稀硝酸,无明显现象
|
|
| 18. | 详细信息 |
|
溶液、胶体和浊液这三种分散系的根本区别是 A.是否是大量分子或离子的集合体 B.分散质粒子直径的大小 C.是否能透过滤纸 D.是否为均一、稳定、透明的外观
|
|
| 19. | 详细信息 |
|
河虾不宜与西红柿同食。主要原因是河虾中含有+5价砷,西红柿中含有比较多的维生素C,两者同食时会生成有毒的+3价砷。下列说法中正确的是 A.由上述信息可推知砒霜中含有的砷是+3价 B.因为河虾中含有砷元素,所以不能食用 C.上述反应中维生素C作氧化剂 D.在该反应中维生素C作催化剂
|
|
| 20. | 详细信息 |
|
用NA表示阿伏加德罗常数的值,下列叙述正确的是 A.常温常压下,14gN2含有分子数为0.5NA B.标准状况下,22.4LH2O的分子数为NA C.64gSO2含有氧原子数为NA D.物质的量浓度为0.5mol/L的MgCl2溶液,含有Cl—离子数为NA[]
|
|
| 21. | 详细信息 |
|
(1)200mL 2mol/L的Al2(SO4)3溶液中SO42﹣的物质的量浓度为 mol/L; (2)7.3gHCl的物质的量为 ,所含HCl分子数为 ,标准状况下体积为 ,将其全部溶于水配成2L溶液,溶液中HCl的物质的量浓度为__________。 (3)同温同压下,等体积的NH3和H2S气体的质量比为__________________;等质量的NH3和H2S中分子个数比为_______________,原子个数之比为 。 (4)12.4 g Na2R中含有Na+ 0.4mol,则Na2R的摩尔质量为 ,R的相对原子质量为 。
|
|
| 22. | 详细信息 |
|
某钠盐A的溶液,实验时有以下一现象:①加入Ba(NO3)2溶液时出现白色沉淀;②加入Na2CO3,有气泡产生,由此可判断出该钠盐A为___________(化学式)
|
|
| 23. | 详细信息 |
|
为了除去粗盐中的Mg2+、SO42-、Ca2+得到较纯净的食盐,可用下列操作,操作顺序为 (用序号填写,每步操作只用一次) ① 过滤 ② 加入过量氢氧化钠溶液 ③ 加热蒸发得到晶体 ④ 加水溶解 ⑤ 加过量盐酸 ⑥ 加过量碳酸钠溶液 ⑦ 加过量氯化钡溶液 步骤⑦所发生主要反应的离子方程式为: 。
|
|
| 24. | 详细信息 |
|
(1)实验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为: 2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O 回答下列问题: ①该反应中的氧化剂是_________,氧化剂和还原剂的物质的量之比为________。 ②氧化性:KMnO4________Cl2(填“﹥”、“﹤”或“=”)。 ③将上述方程式改写成离子方程式 。[] (2)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮 用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为: 10Al + 6NaNO3 + 4NaOH =10 NaAlO2 +3 N2↑+ 2H2O 请回答下列问题: ①上述反应中,_______元素的原子被还原。 ②用“双线桥法”表示反应中电子转移的方向和数目: ________________________________________________________。 ③上述反应中若标准状况下产生11.2 L气体物质,则转移电子的数目为 。
|
|
| 25. | 详细信息 |
|
化学是一门以实验为基础的自然科学,化学实验在化学学习中具有重要的作用。 (1)下列关于实验的叙述中正确的有 (填序号)。 A.不慎碰翻燃着的酒精灯失火,应立即用湿布灭火 B.不慎将酸沾到皮肤或衣物上,应立即用浓NaOH清洗 C.实验时应节约药品,实验剩余的药品应放回原试剂瓶 D.使用分液漏斗前须检查其是否漏水 E.过滤时,用玻璃棒搅动漏斗内液体,使之过滤完全 F.在振荡分液漏斗时,须不断放气,以减小分液漏斗内压强 (2)欲用CCl4从碘的水溶液里提取碘,充分振荡后静置,观察到的现象是: ________________________________________________________。 (3) 实验室配制480mL1.0mol/L的NaOH溶液,用托盘天平称量的NaOH固体的质量是 ,配制过程用到的玻璃仪器除量筒、烧杯、胶头滴管外,还有 。 分析以下操作对配制的溶液浓度造成的影响,影响偏高的是 。 ①蒸馏水洗完容量瓶后没有烘干 ②转移溶液过程中出现漏液 ③称量时用滤纸 ④定容时俯视 ⑤摇匀后发现液面降低,再加蒸馏水 (4)在盛放18mol/L浓硫酸时,包装上应标出的危险化学品标志是______。
|
|
| 26. | 详细信息 |
|
现有甲、乙、丙三位同学分别进行Fe(OH)3胶体的制备实验。 甲同学:向1mol/L的FeCl3溶液中加入少量NaOH溶液。 乙同学:直接加热饱和FeCl3溶液。 丙同学:向25 ml沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。 试回答下列问题: (1)其中操作正确的同学是 。 (2)甲同学的实验中发生的反应的离子方程式为: 。 (3)向Fe(OH)3胶体中加入浓盐酸产生的现象为: , 解释该现象的原因: 。
|
|