江苏省徐州市2017届九年级化学下学期第二次模拟试题及答案
| 1. | 详细信息 |
|
针对能源、环境、水资源等方面的危机,以下4个设想中合理可行的是 A.大量开采地下水,以满足社会对水的需求 B.生活中严禁使用塑料制品,以解决“白色污染”问题 C.面对金属矿物储量有限的危机,寻找金属的替代品 D.禁止开发和使用化石燃料,以应对全球能源危机
|
|
| 2. | 详细信息 |
|
国产大型客机C919于2017年5月5日在上海浦东国际机场首飞成功。C919大型客机的研制,使用了大量的铝锂合金、钛合金和复合材料等。下列有关说法错误的是 A.锂的密度应该比较小 B.金属铝质轻、耐腐蚀、延展性好 C.铝锂合金属于复合材料 D.钛合金是以钛为基础加入其他元素熔合而成的
|
|
| 3. | 详细信息 |
|
.甲醛的水溶液俗称福尔马林,是有刺激性气味的液体,常用于浸制生物标本,但是不能用来保存、保鲜 A.甲醛属于氧化物 B.甲醛的相对分子质量是30 g C.甲醛中氢氧元素的质量比为2︰1 D.甲醛中氢元素的质量分数最小
|
|
| 4. | 详细信息 |
|
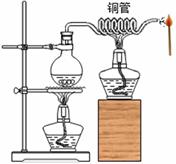
.如图所示,加热烧瓶中的水使之沸腾。水蒸气从铜管喷出,此时将火柴靠近管口处,再迅速移开火柴,火柴立即燃烧。下列说法错误的是
B.管口处水蒸气的作用是使火柴温度达到着火点 C.火柴移离水蒸气,与氧气充分接触,从而燃烧 D.火柴完全燃烧的产物含有二氧化碳和水等
|
|
| 5. | 详细信息 |
|
学习化学要树立正确的观念。下列有关叙述错误的是 A.硅元素在二氧化硅中显+4价 B.呈碱性的物质不一定是碱 C.pH< 5.6的降水,属于酸雨 D.通过化学变化可以使黄铜变成黄金
|
|
| 6. | 详细信息 | ||||||
|
临近中考,家长为了给孩子增加营养,制定了如下食谱:
从营养均衡的角度考虑,你认为家长应该增加的食物是 A.烤面包 B.炒蔬菜 C.炖豆腐 D.水煮虾
|
|||||||
| 7. | 详细信息 | |||||||||||||||
|
.W、X、Y、Z四种物质在一定条件下充分反应后,测得反应前后各物质的质量如下:
下列说法错误的是 A.反应生成40 g的 C.W可能是反应的催化剂 D.Y一定是化合物
|
||||||||||||||||
| 8. | 详细信息 |
|
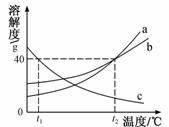
A.t1 ℃时,a、b、c溶解度的大小顺序是:a>b>c B.t2 ℃时,a、b饱和溶液中溶质质量分数相等 C.t2 ℃时,将40 g 的c加到100 g水中,制得的溶液不饱和 D.欲使c从溶液中结晶,可以采用降温结晶或蒸发溶剂的方法
|
|
| 9. | 详细信息 | ||||||||
|
下列对某一主题的知识归纳,有错误的一组是
|
|||||||||
| 10. | 详细信息 |
|
对暴露在空气中部分变质的氢氧化钠溶液(以下简称样品)进行如下的四个实验,其中叙述错误的是 A.向样品中滴入澄清石灰水,有白色沉淀生成 B.向样品中滴入足量的稀盐酸,有气体产生 C.除去样品中的杂质,可以加入过量石灰水,充分反应后再过滤 D.先向样品中加入足量CaCl2溶液,充分反应后滴加酚酞试液,上层清液变红色
|
|
| 11. | 详细信息 |
|
生活中处处有化学。请完成下列空白: (1)在净 (2)我们身边的物质主要是有机物,这是因为 ▲ (填写元素符号)能以很多连接方式组成形形色色的物质。 (3)从微观的角度分析可知:“八月桂花满园香”能说明 ▲ ;“物质一般有三态变化”能说明 ▲ 。 (4)医疗上常用小苏打治疗胃酸过多,其原理是 ▲ (写化学方程式)。
|
|
| 12. | 详细信息 |
|
生产生活中常用到氯化钠溶液。请回答: (1)氯化钠溶液中的含有的阴离子是 ▲ (写离子符号)。 (2)农业上常用15%的氯化钠溶液筛选粮种,若要配制200 kg这种氯化钠溶液,需要氯化钠的质量是 ▲ 千克,需要水 ▲ 升。 (3)在化学实验室里,配制一定溶质质量分数的氯化钠溶液,实验步骤有:①计算、②转移、③量取水、④称取氯化钠、⑤溶解。正确的操作顺序为 ▲ (填写序号)。
|
|
| 13. | 详细信息 |
|
【查阅资料】 ①白磷剧毒,着火点低(40℃),易燃烧,且耗氧彻底。 ②硫酸铜溶液能与白磷反应,从而化解白磷的毒性。 【实验探究】 (1)在确保装置不漏气时,按图装入药品、连好仪器。 (2)将锥形瓶底部放入热水中,白磷很快被引燃。白磷燃烧的化学方程式是 ▲ 。 (3)燃烧结束后,等到锥形瓶冷却到室温,按下注射器,使注射器针头穿透橡皮塞,此时注射器里的硫酸铜溶液会 ▲ ,以弥补氧气的体积。如果实验比较成功,测得氧气的体积分数约是 ▲ ,最终注射器里的液面约停留在 ▲ mL刻度处。 【反思评价】 (1)实验结束、振荡锥形瓶,硫酸铜溶液能与剩余的白磷发生反应,有关的化学方程式为: 11Px + 60CuSO4 + 96H2O = 20Cu3P↓ + 24H3PO4 + 60H2SO4,则x= ▲ 。 (2)此改进装置与课本上“测量空气中氧气体积分数”实验装置相比,有不少的优点,请你写出1条: ▲ 。
|
|
| 14. | 详细信息 |
|
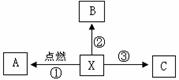
下图是金属X化学性质网络图(箭头表示转化方向,部分反应物、生成物省略),其中X是目前世界上年产量最高的金属,A是具有磁性的黑色物质,B是可燃性气体,反应③常用于湿法冶金。
(1)做反应①的实验时,为防止集气瓶炸裂,必须 ▲ 。 (2)反应②的实验现象是 ▲ 。 (3)反应③的化学方程式是 ▲ 。 (4)工业上冶炼金属X的设备叫 ▲ ,用到的原料有 ▲ (写出3种即可)。
|
|
| 15. | 详细信息 |
|
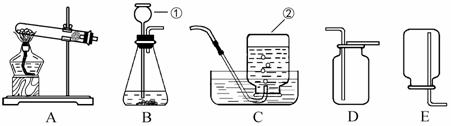
下图是实验室制取气体的有关装置,请回答:
(1)写出标号仪器的名称 (2)用B装置制氧气的化学方程式为 ▲ ;能用C装置收集氧气,因为氧气 ▲ 。 (3)实验室制取甲烷的装置组合是AC或AE,据此可知制取甲烷的反应物状态是 ▲ 、反应条件是 ▲ ,甲烷具有的物理性质是 ▲ (写出1条即可)。 (4)初中化学实验中,能用发生装置B制取的气体除氧气外,还有 ▲ (填写两种气体),其中制气原理属于复分解反应的化学方程式是 ▲ 。
|
|
| 16. | 详细信息 |
|
向160 g硫酸铜溶液中,逐滴加入40 g 氢氧化钠溶液,恰好完全反应,生成4.9 g沉淀。回答下列问题: (1)恰好完全反应后,所得溶液的质量为 ▲ g。 (2)将反应结束后的混合物过滤,滤液中的溶质是 ▲ (写名称)。 (3)求原硫酸铜溶液中溶质的质量分数(写出计算过程)。
|
|
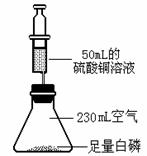 化学兴趣小组在李老师指导下,改进了“测量空气中氧气体积分数”的实验装置(见下图),并进行以下实验探究活动,请你一同参与。
化学兴趣小组在李老师指导下,改进了“测量空气中氧气体积分数”的实验装置(见下图),并进行以下实验探究活动,请你一同参与。