课题2 溶解度 知识点题库
甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法正确的是( )

A . 甲物质的溶解度是20g
B . 将丙物质的饱和溶液变为不饱和溶液可以采用加水或降温的方法
C . t2℃时,等质量水分别配成甲、乙、丙的饱和溶液,所得溶液质量的大小关系是乙>甲>丙
D . t3℃时,甲、乙、丙三种溶液中溶质的质量分数的大小关系是甲>乙>丙
60℃时,KNO3的溶解度为110g.在60℃时,将60g KNO3投入到50g水中,充分搅拌后所得溶液的质量分数为( )
A . 54.5%
B . 37.5%
C . 52.4%
D . 47.5%
如图是甲、乙、丙三种固体物质的溶解度曲线。

-
(1) P点的含义。
-
(2) 要使接近饱和的甲溶液变成饱和溶液,可采用的方法有(写出一种)。当甲溶液中含有少量乙时,可采用的方法提纯甲。
-
(3) t2℃时,将30g甲物质放入50g水的烧杯中,所得溶液溶质的质量分数为(精确到0.1)。若烧杯内物质升温到t3℃(不考虑水蒸发),溶液中变化的是。Ⅰ.溶质的质量 Ⅱ.溶剂的质量 Ⅲ.溶质的质量分数
-
(4) t2℃时,在含有50 g水的甲和乙的饱和溶液中,分别加入mg甲和mg乙,升温至t3℃,甲完全溶解,乙仍有剩余,则m的质量范围是。
如图是a、b两种固体物质的溶解度曲线.

-
(1) 从图中你能获得的信息是(答出两条即可).
-
(2) 40℃时,a物质的饱和溶液中溶质和溶剂的质量比是.
下表为两种物质在不同温度时的溶解度
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 |
KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
请回答:
(1)60℃时,KCl的溶解度是 g;
(2)40℃时,将30g KCl加入到50g水中,充分溶解后所得溶液是 溶液(填写“饱和”或“不饱和”);
(3)将20℃时KNO3和KCl的两种饱和溶液升温至60℃,则两种溶液的溶质质量分数大小关系是:KNO3 KCl(填写“>”、“<”或“=”).
由于人类将使用含磷洗涤剂后的污水排入湖泊中,使得湖泊中的藻类大量繁殖,导致水体富营养化,生物耗氧量大大增加,湖水受到严重污染.你认为下列哪种情况下湖水的溶解氧最低( )
A . 白天、未污染
B . 黑夜、污染
C . 白天、污染
D . 黑夜、未污染
下列叙述正确的是( )
A . 用含有氢氧化铝的药物治疗胃酸过多
B . 氢氧化钠暴露在空气中易与二氧化碳反应而变质,因此常用作某些气体干燥剂
C . 喝了汽水以后,常常会打嗝,说明二氧化碳的溶解度随温度的升高而增大
D . 酒精能溶解许多物质,是最常用的溶剂
关于溶液的叙述正确的是( )
A . 溶液都是无色的
B . 饱和溶液一定是浓溶液
C . 糖水的溶质是水
D . 医用生理盐水是溶液
下列图象不能正确反映其对应关系的是( )
A .  向一定量的NaCl饱和溶液中加入NaCl固体
B .
向一定量的NaCl饱和溶液中加入NaCl固体
B .  向等质量的锌粉和铁粉中分别滴加质量分数相同的足量稀盐酸
C .
向等质量的锌粉和铁粉中分别滴加质量分数相同的足量稀盐酸
C .  用一定量的过氧化氢溶液制取氧气
D .
用一定量的过氧化氢溶液制取氧气
D .  高温煅烧一定质量的石灰石
高温煅烧一定质量的石灰石
 向一定量的NaCl饱和溶液中加入NaCl固体
B .
向一定量的NaCl饱和溶液中加入NaCl固体
B .  向等质量的锌粉和铁粉中分别滴加质量分数相同的足量稀盐酸
C .
向等质量的锌粉和铁粉中分别滴加质量分数相同的足量稀盐酸
C .  用一定量的过氧化氢溶液制取氧气
D .
用一定量的过氧化氢溶液制取氧气
D .  高温煅烧一定质量的石灰石
高温煅烧一定质量的石灰石
如图所示是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。
![]()

根据图示回答:
-
(1) P点的含义是。
-
(2) 在不改变溶液的溶质质量分数的情况下,把c物质的不饱和溶液变成饱和溶液的方法是。
-
(3) t2℃时40g a物质加入到60g水中不断搅拌,溶液质量为 g。
-
(4) 将t1℃a、b、c三种物质饱和溶液升温至t2℃时,三种溶液的溶质质量分数大小关系是(填选项序号)。
Ⅰ.a>b=c Ⅱ.a=b>c Ⅲ.a>b>c Ⅳ.b > a >c
 、
、 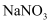 、
、  三种物质的溶解曲线如下图所示,下列说法正确的是()
三种物质的溶解曲线如下图所示,下列说法正确的是() 
A .  的溶解度比
的溶解度比  大
B . 将
大
B . 将  饱和溶液降温,溶液中
饱和溶液降温,溶液中  的质量分数不变
C .
的质量分数不变
C .  饱和溶液中含少量
饱和溶液中含少量  ,可通过降温结晶的方法提纯
D . 将100g40℃的
,可通过降温结晶的方法提纯
D . 将100g40℃的 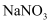 饱和溶液降温至0℃,析出31g晶体
饱和溶液降温至0℃,析出31g晶体
 的溶解度比
的溶解度比  大
B . 将
大
B . 将  饱和溶液降温,溶液中
饱和溶液降温,溶液中  的质量分数不变
C .
的质量分数不变
C .  饱和溶液中含少量
饱和溶液中含少量  ,可通过降温结晶的方法提纯
D . 将100g40℃的
,可通过降温结晶的方法提纯
D . 将100g40℃的 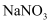 饱和溶液降温至0℃,析出31g晶体
饱和溶液降温至0℃,析出31g晶体
下图是某实验小组绘制的两种固体物质溶解度曲线图。请你根据图示回答下列问题:

-
(1) t1℃时,a物质的溶解度b物质的溶解度(填“>”、“<”或“=”)。
-
(2) 将t2℃时a、b两种物质相同质量的饱和溶液,分别冷却到t1℃,析出晶体最多的是物质。
-
(3) 温度是影响固体物质溶解度的重要因素。图中a、b两种物质的溶解度受温度影响较大的是(填“a”或“b”)
室温时,对100mL氯化钠饱和溶液作如下操作,最终甲、乙两烧杯中溶液()

A . 溶质质量相同
B . 溶质质量分数相同
C . 均为不饱和溶液
D . 溶剂质量相同
小明同学计划研究“溶质的种类对溶解限量的影响”,下列实验设计中最合理的是( )
A . 20℃,分别向20g油和水中加入食盐,达到饱和,比较溶解量
B . 20℃,向20g水中加入食盐,向30g水中加入熟石灰,比较溶解情况
C . 20℃,分别向20g水中加入食盐和熟石灰,观察溶解情况
D . 20℃,分别向20g水中加入食盐和熟石灰,直至饱和,比较两物质溶解的量
由128克硝酸钾、60克氯化钠组成的混合物投入200g热水溶解,对该溶液进行如图实验(假设实验过程中无损耗):


-
(1) 两种物质溶解在水中,用玻璃棒搅拌的目的是。
-
(2) 实验时温度t的范围为。
-
(3) 操作1用到的玻璃仪器除玻璃棒以外还有。
-
(4) 请定量描述晶体1的组成(忽略操作中的误差)。
-
(5) 溶液2为(填物质名称)的饱和溶液。
-
(6) 关于溶液1和溶液2中溶解的NaCl的质量大小关系:溶液1溶液2(选填“>”、“<”或“=”)。
-
(7) 关于上述实验说法错误的是_______________________。A . 晶体1与晶体2比较,晶体1中KNO3的纯度更高 B . 溶液1中KNO3为饱和溶液,NaCl为不饱和溶液 C . 溶液1恒温蒸发90g水后,与溶液2的溶质质量相同
甲、乙、丙三种固体物质的溶解度曲线如图所示.下列叙述不正确的是( )

A . t1℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量:甲>乙
B . 将t1℃时甲、丙的饱和溶液升温到t2℃,两种溶液中溶质的质量分数相等
C . 将t2℃时甲的饱和溶液变为t3℃时甲的饱和溶液,可以采用蒸发水的方法
D . 将t3℃时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:甲>乙>丙
如图是 KNO3和 NH4Cl 的溶解度曲线,下列叙述错误的是( )

A . t1℃时,KNO3与 NH4Cl 的溶解度相等
B . 若 t1℃=20℃,则 NH4Cl 属于易溶的物质
C . t2℃时,NH4Cl 的不饱和溶液降温,肯定无晶体析出
D . t2℃时,KNO3饱和溶液中溶质的质量分数是 37.5%
如图所示是a、b、c三种物质的溶解度曲线,据图回答下列问题:

-
(1) 三种物质的溶解度随着温度升高而减小的是。
-
(2) P点的含义是。
-
(3) t3℃时,把80g物质a加入200g水中充分搅拌、静置,形成的是溶液(填“饱和”或“不饱和”)。
-
(4) t3℃时将a和b的饱和溶液降到t1℃,析出晶体的质量关系正确的是______(填字母序号)。A . a>b B . a=b C . a<b D . 不能确定
-
(5) 若a中含有少量b,要提纯a时,可采取的方法是。
向氯化钠饱和溶液中,逐渐加入氯化钠固体(不考虑溶解时的热量变化),边加边搅拌。下列图形中变化关系正确的是( )
A . 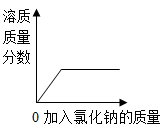 B .
B . 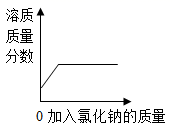 C .
C . 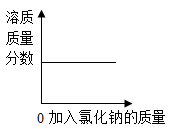 D .
D . 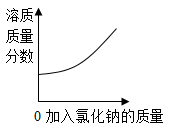
 B .
B .  C .
C .  D .
D . 
如表是KCl与KNO3的溶解度数据。则下列说法正确的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 |
KCl | 30g | 33g | 35g | 38g | 41g |
KNO3 | 21g | 31g | 45g | 65g | 88g |
A . 两物质的溶解度相等的温度在20﹣30℃间
B . KNO3比KCl的溶解度大
C . 在20℃时,10g水中加入5g KCl可得到33.3%的KCl溶液
D . 在50℃时,两物质各5g分别加入10g水中,充分溶解均得到饱和溶液
最近更新



