第十一单元 盐 化肥 知识点题库

-
(1) 取水后加入明矾的作用是。
-
(2) 如图3是小明同学用来除去水中难溶性杂质时所采用的过滤装置图。写出标号仪器的名称:a ;写出图3中存在的明显错误:①②。
-
(3) 向滤液中加入活性炭,利用其 性,除去水样中的色素和异味。
-
(4) 在制取蒸馏水的过程中,在清水中加入消毒剂,其作用是。
-
(5) 净化后的水变为蒸馏水的步骤是 。图2所示是制取蒸馏水的简易装置,写出仪器名称:b 。
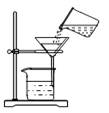 过滤
B .
过滤
B . 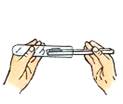 取用固体粉末
C .
取用固体粉末
C .  闻气体的气味
D .
闻气体的气味
D . 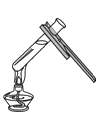 加热液体
加热液体

-
(1) 配制波尔多液时,发生反应的化学方程式是,配制过程中不能用铁制容器,原因是(用化学方程式表示);
-
(2) 喷洒波尔多液后,不到采摘期的蔬果表面有一些蓝色斑点(一种难溶性喊),蓝色斑点的成分是(填化学式),不易用水清洗,可用厨房中的调味剂浸泡除去。
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别 H2SO4 溶液和 NaOH 溶液 | 取样,滴加酚酞溶液,观察现象 |
| B | 证明氢氧化钠溶液与稀盐酸能反应 | 取氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,振荡,再滴入稀盐酸至溶液变为无色 |
| C | 除去CaCl2溶液中的少量盐酸 | 加入适量的铁粉 |
| D | 除去CO中含有的少量CO2 | 通入氢氧化钠溶液中,再通过浓硫酸干燥 |

-
(1) “酸溶”过程中,将一定浓度的盐酸缓慢加入粉碎后的优质石灰石中,同时搅拌。搅拌的目的是。
-
(2) “操作1”、“操作2”步骤中,需要用到的玻璃仪器有烧杯、玻璃棒和。
-
(3) “操作2”中分离得到的NH4Cl,在农业上可用作。
[提出问题]蚁酸的成分是什么?蚁酸分解的产物是什么?
[在阅资料] 蚁酸是一种有机酸,化学名称叫做甲酸,化学式为HCOOH;
蚁酸在一定条件下会分解生成两种氧化物:
[猜想假设]
-
(1) 小芳同学根据蚁酸的元素组成推测出生成物中一定含有;
-
(2) 另一种生成物,小敏提出两种猜想:猜想①:该气体是CO2;猜想②:该气体是;
-
(3) [进行实验]他们将蚁酸分解产生的气体通过如下装置(铁架台已略去),观察现象。

I.实验时装置A中无明显变化,则猜想① (填“成立”或“不成立”);
Ⅱ.装置B中的现象是;
装置C中发生反应的化学方程式为;
[实验结论]通过实验探究证明:猜测②成立
-
(4) [讨论交流]
①从环保角度看,该装置的不足之处是;
②如B装置中硬质玻璃管(含内容物)实验前质量为112.8g,实验后质量为109. 6g,则参与反应的氧化铜质量为g。
-
(1) 推断:A是;E是。
-
(2) 写文字表达式:产生C气体的反应文字表达式; D在C中燃烧的反应文字表达式。
-
(3) 用坩埚钳将红热的E缓慢由瓶口伸入,其目的是。
 B . 加热高锰酸钾制取氧气
B . 加热高锰酸钾制取氧气 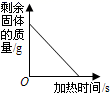 C . 用等质量、等浓度的过氧化氢溶液分别制取氧气
C . 用等质量、等浓度的过氧化氢溶液分别制取氧气  D . 测定空气中氧气的含量
D . 测定空气中氧气的含量 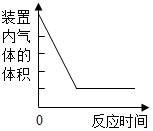
(提出问题)①三种溶液的酸碱性?
②它们与酸反应时溶液的pH如何变化?
(查阅资料)
|
pH |
2~3 |
4~6 |
7 |
8~9 |
10~11 |
12~14 |
|
紫甘蓝汁液显示的颜色 |
紫红 |
浅紫 |
紫色 |
蓝色 |
绿色 |
黄色 |
(实验1)向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
|
液体名称 |
蒸馏水 |
碳酸氢钠溶液 |
碳酸钠溶液 |
氢氧化钠溶液 |
|
紫甘蓝汁液显示的颜色 |
紫色 |
蓝色 |
绿色 |
黄色 |
(实验2)向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图1所示。
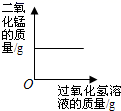
(实验3)向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图2、图3所示。将图2与图3的阴影部分进行叠加,发现两者基本重合。

(解释与结论)
-
(1) 实验1得出三种溶液的碱性由强到弱的顺序为。
-
(2) 实验2证明了氢氧化钠能与盐酸发生反应,其理由是,实验结束,向反应后的溶液中滴加紫甘蓝汁液,观察到的现象是。
-
(3) 实验3中,b点的溶质为,c点后发生反应的化学方程式为。
-
(4) 依据实验3获取的信息,鉴别Na2CO3和NaHCO3固体的实验方案为。
(提出问题)试管中浅黄色溶液的溶质是什么?
-
(1) (猜想假设)同学们都认为溶质中一定含有Fe2(SO4)3 , 理由是,然后提出如下猜想:
猜想①溶质是Fe2(SO4)3;
猜想②溶质是Fe2(SO4)3和FeSO4;
猜想③溶质是Fe2(SO4)3和H2SO4;
猜想④溶质是Fe2(SO4)3、H2SO4和(填化学式)。
-
(2) (查阅资料)FeSO4溶液能使酸性KMnO4溶液的紫红色褪去;
H2SO4溶液和Fe2(SO4)3溶液均不能使酸性KMnO4溶液的紫红色褪去。
(实验探究)同学们分组合作进行如下实验探究。
组次
实验操作
现象与结论
小组同学相互评价
第1组

现象:产生大量气泡,……
结论:溶质中一定含有H2SO4 , 猜想③或④成立。
第2组同学认为:此结论正确。产生大量气泡的化学反应方程式为。
第2组

现象:。
结论:结合第1组的实验现象,推理出猜想④成立。
第1组同学认为:此结论正确。
-
(3) (实验反思)上述实验探究说明,在用稀硫酸或稀盐酸除铁制品上的铁锈时,应该注意的事项是。
 稀释浓硫酸
B .
稀释浓硫酸
B .  测定溶液的pH值
C .
测定溶液的pH值
C .  过滤
D .
过滤
D .  验证酸碱中和反应
验证酸碱中和反应

下列叙述错误的是 ( )

-
(1) B的化学式为,D的化学式为,E的化学式为。
-
(2) 写出A + E → H2O + B的化学方程式:。
-
(3) 写出C的一种用途。

-
(1) 金属B的活动性(填“>”“<”或“=”)金属D的活动性。
-
(2) 向C的溶液中加入BaCl2溶液,有白色沉淀产生,加入稀盐酸,沉淀不溶解,写出C的化学式。
-
(3) 反应②的化学方程式为。

-
(1) 写出A与废液中的物质发生反应的化学方程式。
-
(2) 操作2的名称是。
-
(1) 能导致人中毒的碳的氧化物。
-
(2) 可用作干燥剂的酸(写溶质的化学式)。
-
(3) 可用作补钙剂的盐。

-
(1) C和F的分别是:C、F。
-
(2) D→E的化学方程式为。
-
(3) A→B属于(填“吸热”或“放热”)反应
【查阅资料】①锌锰干电池的负极为锌筒;正极为带有铜帽的碳棒。
②滤液中可能含有NH4Cl和ZnCl2中的一种或两种。
③向ZnCl2溶液中逐滴滴入稀氨水,先生成白色沉淀,然后沉淀溶解。
-
(1) 【提出问题】黑色滤渣中可能含有哪些物质?滤液中溶质的主要成分是什么?
实验步骤
实验现象
实验结论
实验一
取黑色滤渣在氧气流中充分加热,产生无色无味气体,并将气体通入澄清的石灰水。
①澄清石灰水变浑浊,可用化学方程式表示为:
②有黑色粉末有剩余
根据现象(1)可知,黑色滤渣中一定含有元素
实验二
取实验一中剩余的黑色粉末于试管中,加入5mL5%的溶液,将带火星的木条放在试管口。
带火星的木条复燃
黑色粉末中可能含有MnO2
实验三
取少量无色滤液加入盛有NaOH固体的试管中,加热:将湿润的红色石蕊试纸放在试管口
红色石蕊试纸变蓝
滤液中溶质的成分为
另取适量无色滤液于试管中,逐滴加入稀氨水
先生成白色沉淀,然后沉淀
-
(2) 【交流反思】通过上述探究活动,体现化学学习的特点是。
A.关注物质的性质和变化
B.关注物质变化的过程以及对结果的解释和讨论



