第十一单元 盐 化肥 知识点题库

-
(1) 操作①的名称是,实验室进行该操作时需要用到的仪器为铁架台、烧杯和、 ;
-
(2) 操作②主要是活性炭的性除去一些异味和色素:
-
(3) 取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明是(填“硬水”或“软水”),生活中硬水软化采用方法;
-
(4) 请你列举一条有利于保护水资源的做法。
(查阅资料)新鲜的鸡血遇一氧化碳变为樱桃红色。
(提出猜想)小组成员对水煤气的成分提出以下四种猜想:
猜想1:H2、CO2;猜想2:H2、CO;猜想3:CO、CO2;猜想4:H2、CO、CO2。
-
(1) 请你说明猜想3不能成立的理由。
-
(2) (实验探究)小组设计了下图所示的实验装置进行探究。
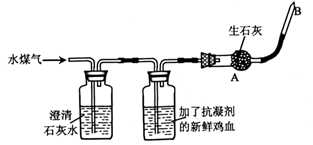
(实验现象)通入水煤气后,澄清石灰水不变浑浊,新鲜鸡血变樱桃红色。
由此可知,水煤气中不含,含有(均填化学式)。
(继续实验)在B处点燃气体,然后用一个干冷的烧杯罩在火焰上方。
-
(3) A处生石灰的作用是,气体通过A后再在B处点燃时,观察到所罩烧杯的内壁,由此证明水煤气中含有H2 , 猜想成立。
-
(4) 由探究结果可知,焦炭与水蒸气在高温下反应的化学方程式为。
| | | | |
| A.将水通电电解一 段时间 | B.加热一定量的高 锰酸钾固体 | C.向两份相等质量的块状大理石和粉末状大理石中分别加入过量的等浓度的稀盐酸 | D.向一定量的二氧化锰中加入过氧化氢溶液 |

-
(1) (一)、操作①的名称是 ,该操作的装置如图

写出标号仪器的名称:a b
-
(2) 该装置图中存在明显不正确,指出其中的两处:
① ②
-
(3) 操作过程中,发现液体流速一直很慢,产生的原因可能是
-
(4) (二)、操作②主要是除去异味和色素,应选用的物质是,此过程体现了该物质的性质(填“物理”或“化学”)。
-
(5) (三)、通过操作③(填操作③的名称)即可得到蒸馏水,蒸馏水是(选填“纯净物”或“混合物”)
-
(6) (四)、保护水环境,珍爱水资源,是每个公民应尽的责任和义务,下列做法有利于保护水资源的是____(填字母)A . 实验室的废液不经处理直接排放 B . 工业废水处理达标后排放 C . 化肥和农药的过度过度使用 D . 煤炭脱硫后燃烧,减少酸雨对水源的污染
| 选项 | 实验目的 | 实验操作 |
| A | 鉴别空气和氧气 | 放入带火星的木条 |
| B | 鉴别硬水和软水 | 加入肥皂水 |
| C | 鉴别白糖水和蒸馏水 | 观察颜色 |
| D | 鉴别氢氧化钠和硝酸铵 | 加水溶解并测温度 |

-
(1) A试管中溶液变为红色,说明碳酸钠溶液显性。
-
(2) B试管中有气泡产生,发生反应的化学方程式为。
-
(3) C试管中发生反应的化学方程式为。
-
(4) D试管中产生明显的现象是。
-
(5) 实验结束后,同学们将上述四支试管中的物质倒入同一烧杯内,烧杯底部有白色固体,上层为红色溶液。为处理废液,将烧杯内混合物过滤后,向红色滤液中加入稀盐酸,有气泡产生,说明滤液中一定没有的溶质为(填字母序号);
A氢氧化钠
B碳酸钠
C氯化钙
D氢氧化钙
继续加稀盐酸至溶液颜色恰好消失,此时溶液中的溶质为(除酚酞外)。
-
(1) 该反应生成二氧化碳的质量为g。
-
(2) 求该样品中碳酸氢钠的质量分数(写出计算过程)。

实验结束,甲先将废液缓慢倒入废液缸中;随后乙也将废液缓慢倒入到同一废液缸中。
-
(1) (观察与分析)乙同学观察到废液缸中先有气泡产生,然后又出现了白色沉淀。产生的气体是;白色沉淀是Na2CO3溶液与溶液反应产生的。
-
(2) (提出问题)最终废液中含有什么溶质?
(猜想与假设)猜想一:废液中含有NaCl、CaCl2两种溶质;猜想二:废液中含有NaCl、Na2CO3两种溶质;猜想三:废液中含有NaCl、HCl两种溶质。
(实验设计与探究)
实验方案
实验现象
结论
甲
取少量废液于试管中,向其中滴加Na2CO3溶液
无明显现象
猜想一、三不成立,猜想二成立
乙
取少量废液于试管中,向其中滴加CaCl2溶液
出现白色沉淀
猜想一、三不成立,猜想二成立
(反思与评价)
(猜想与假设)中,猜想是不合理的。猜想也不完整,请补充:猜想四:。
-
(3) 老师认为甲同学的(实验设计与探究)结论实际上是不合理的,理由是。
-
(4) 若猜想四成立,则所得溶液中溶质的质量为g。


-
(1) 为了充分吸收SO2 , A实验中集气瓶内水的最好换成溶液;
-
(2) B实验中玻璃管的作用是;
-
(3) C实验过程中,当蒸发皿中出现时,停止加热;
-
(4) D实验中酒精灯加网罩的作用。
 B . 溶解
B . 溶解  C . 过滤
C . 过滤  D . 蒸发
D . 蒸发 
 在两个烧杯中分别盛有等质量的铁粉和锌粉以及足量等浓度的稀盐酸
B .
在两个烧杯中分别盛有等质量的铁粉和锌粉以及足量等浓度的稀盐酸
B .  在两个烧杯中分别盛有等质量、等浓度的稀盐酸以及足量的铁粉和锌粉
C .
在两个烧杯中分别盛有等质量、等浓度的稀盐酸以及足量的铁粉和锌粉
C .  向盛有等质量、等浓度稀盐酸的两个烧杯中,分别不断加入铁粉和锌粉
D .
向盛有等质量、等浓度稀盐酸的两个烧杯中,分别不断加入铁粉和锌粉
D .  向盛有等质量铁粉和锌粉的两个烧杯中,不断滴加等浓度的稀盐酸
向盛有等质量铁粉和锌粉的两个烧杯中,不断滴加等浓度的稀盐酸

-
(1) 请写出下列物质的化学式:D。E。G。H。
-
(2) B物质的用途是(任写一种)。
-
(3) 请写出下列反应的文字(符号)表达式:①B→F,②B→G,其基本反应类型是。

-
(1) 滤液Y中含有的溶质有(填化学式)。
-
(2) 证明CaCl2已过量的正确操作是静置悬浊液X,取少量上层清液于试管中,滴加少量,然后观察现象判断。
-
(3) 若沉淀不经过洗涤操作会造成Na2CO3的质量分数(填“偏大”“偏小”或“无影响”)。
-
(4) 通过以上数据计算出样品中Na2CO3的质量分数。(写出计算过程,结果精确至0.1%)
-
(1) 【提出问题】滤液里含有什么溶质?
【提出猜想】猜想①: ;
猜想②:NaCl、Na2SO4;
猜想③:NaCl、Na2CO3;
猜想④:NaCl、Na2CO3、Na2SO4 ;
猜想⑤:NaCl
-
(2) 【实验探究】

观察到现象a:只有气泡产生,则小组同学认为猜想③成立,他们的结论是否正确?
请说明理由 ;
-
(3) 向滤液中加入过量BaCl2溶液,若产生的现象b为:生成白色沉淀,然后加入足量的稀硝酸沉淀完全溶解,有气泡产生,则猜想 成立,上述实验过程中发生的反应的化学方程式为 ;若猜想④成立,则上述实验过程加入足量稀硝酸后观察到的现象为 。
-
(4) 经过讨论,小组同学一致认为猜想③成立。要把废液变为中性才能排放,应如何处理废液 。
 B . 蒸发
B . 蒸发 C . 测定溶液pH
C . 测定溶液pH D . 过滤
D . 过滤
-
(1) 可做干电池电极的物质是。
-
(2) 可作为人体重要能量来源的是。
-
(3) 可用来制造人造骨的是。
-
(4) 食品包装袋内填充的保护气是。
-
(5) 人体胃液中主要的酸是。
-
(6) 可用于生产化肥、农药、火药等的是。

-
(1) 图1是硒元素在元素周期表中的相关信息和硒的原子结构示意图。硒原子的相对原子质量为,硒原子在化学反应中容易得到电子,形成的离子符号为。
-
(2) 以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图。如图2为铁的价类图。写出一个由C通过中和反应转化为E的化学方程式。
-
(3) 我们常常借助微观模型来表示微观粒子的反应变化。
①稀盐酸不能与氯化钡溶液反应,而稀硫酸则能与之反应生成白色沉淀,根据图3从微观角度分析实际参加反应的微粒是(用符号表示)。
②通过分析组成和结构,可以预测物质的某些性质。根据图4硫酸氢钠溶液的微观图示,分析推测NaHSO4的性质,其中合理的是。
A.硫酸氢钠溶液中含有氢离子,所以硫酸氢钠属于酸
B.硫酸氢钠溶液能与碳酸钠反应
C.硫酸氢钠溶液能与铜粉反应生成氢气
D.硫酸氢钠溶液能与硝酸钡溶液反应生成硫酸钡沉淀







