第十一单元 盐 化肥 知识点题库

-
(1) 烧杯中盛放的是溶液;
-
(2) 曲线上b点坐标为(18,7),该点所表示的意义是。
-
(3) 同学们对反应后溶液的成分进行探究如下:
【提出问题】反应后溶液中的微粒有什么?
【假设猜想】依据曲线上的点和已学
知识分析,提出了以下四种猜想:
猜想一:只有Na+、Cl-、H2O;
猜想二:有Na+、Cl-、H2O、H+;
猜想三:有Na+、Cl-、H2O、OH-
猜想四:有Na+、Cl-、H2O、H+、OH-。
小红同学认为猜想是不合理的,理由是 。
-
(4) 【实验探究】
①小芳同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,说明猜想 不成立;
②小君同学取烧杯中的溶液少量于试管中,滴加几滴酚酞溶液,无明显变化,认为猜想一成立。小明同学认为小君同学的判断不科学,理由是 。
③小兰同学取烧杯中的溶液少量于试管中,滴加几滴碳酸钠溶液,观察到有气泡产生,由此断定猜想二成立。该实验中发生反应的化学方程式是。
【实验拓展】
请你用与①、②、③不同类别的试剂,设计另一种方案验证猜想二成立。
实验操作
实验现象
实验结论
猜想二成立
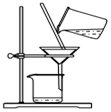 过滤悬浊液
B .
过滤悬浊液
B .  加热液体
C .
加热液体
C . 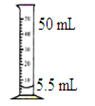 量5.5 mL液体
D .
量5.5 mL液体
D .  放置胶头滴管
放置胶头滴管
①利用泥沙难溶于水而NaCl的性质,我们可以通过溶解、、蒸发等操作除去粗盐中的泥沙,得到较纯净的NaCl。
②NaCl、KNO3的部分溶解度数据见下表。
|
温度(℃) |
20 |
40 |
60 |
80 |
100 |
|
|
溶解度(g/100g水) |
NaCl |
36 |
36.6 |
37.1 |
38 |
39.2 |
|
KNO3 |
31.6 |
63.9 |
110 |
169 |
246 |
|
Ⅰ由上表可知,溶解度受温度影响变化较小的物质是;80℃时KNO3的溶解度是g/100g水,此温度下10克水中最多能溶解KNO3克。
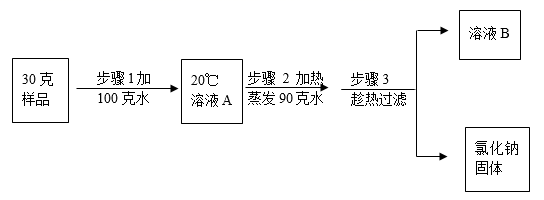
Ⅱ某NaCl样品中含有KNO3杂质。现有30克NaCl样品,经测定含4克KNO3 , 现设计如下实验提纯NaCl;
溶液B是NaCl的(填“饱和”或“不饱和”)溶液。步骤3趁热过滤的设计意图是。

-
(1) 随着不断加热,试管①里逐渐有红色固体产生,同时试管②里的现象是。
-
(2) 小明发现通入试管②里的气体有逸出液面的现象怀疑试管①里还有其他气体生成,比如一氧化碳。老师首先赞扬小明有科学的质疑精神,建议在化学兴趣小组的活动中展开探究。请你也参与其中,一起探究。
(提出问题)碳还原氧化铜的反应还有一氧化碳生成吗?
(猜想与假设)猜想一:没有一氧化碳生成
猜想二:还有一氧化碳生成
(设计方案)
在老师的帮助下,小明设计出如图乙实验。为了提高实验效果,小明加大了反应物的用量。老师提示:先将两个开关都打开,再加热,反复挤压气球一会儿。老师这样提示的目的是。
-
(3) (进行实验)

请你完成下列表格。
实验操作
实验现象
实验结论
先按老师的提示操作,加热一会儿后,关闭开关2待充分反应,关闭开关1,停止加热
逸出液面的气体不是二氧化碳
逸出液面的气体是一氧化碳。猜想二成立
-
(4) (交流与提高)
同学们通过对以上实验的讨论与分析,认为一氧化碳的产生至少源自两个反应:一是试管内反应物直接反应生成;二是生成物又发生反应而生成。请你写出其中一个化学方程式:。
实验中生成的二氧化碳被氢氧化钠浓溶液吸收没有明显现象,同学们想进一步检验该反应的生成物,可选用的药品有(填序号)
①酚酞溶液 ②氢氧化钙溶液 ③稀盐酸 ④锌粒 ⑤氯化钙溶液
|
实验编号 |
① |
② |
③ |
④ |
|
氢氧化钙溶液质量/g |
1000 |
2000 |
3000 |
4000 |
|
沉淀质量/g |
1 |
m |
2.5 |
2.5 |
-
(1) 实验②中m的数值为。
-
(2) 计算该氢氧化钠固体中碳酸钠的质量分数。(写出计算过程)
-
(3) 请在如图中画出生成沉淀质量随加入氢氧化钙溶液质量变化的曲线图,并标出图中的必要数据。

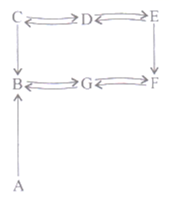
已知A~G为初中化学常见的七种物质。其中A是大理石的主要成分,B、C、G、F分别属于不同类别的物质。各种物质间的转化关系如图所示(“→”表示一种物质可以通过一步反应转化为另一种物质,反应条件、部分反应物和生成物已略去)。
-
(1) 请写出A的化学式。
-
(2) 请写出E→F的化学方程式。
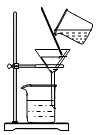 B . 测定溶液pH
B . 测定溶液pH  C . 蒸发结晶
C . 蒸发结晶 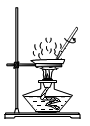 D . 稀释浓硫酸
D . 稀释浓硫酸 

-
(1) A物质的化学式;
-
(2) 写出B物质的一种用途;
-
(3) 写出反应E→D的化学方程式;
-
(4) 写出反应F→E的化学方程式;
-
(5) C与E的反应属于(填“分解”或“化合”)反应。
-
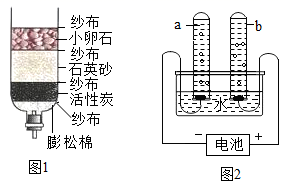
(1) 河水属于(填“纯净物”或“混合物”),若用图1净水器处理河水,其中属于活性炭的作用是。
-
(2) 在图一中纱布有过滤的作用,实验室过滤操作中所必需的仪器为(填字母)。
A.烧杯B.酒精灯C.试管D.铁架台E.玻璃棒F.漏斗G.托盘天平
进行过滤时,下列操作规范的是(填字母)。
A.用玻璃棒引流
B.滤纸边缘高出漏斗
C.漏斗下端未紧靠烧杯内壁
D.将滤纸湿润,使其紧贴漏斗内壁
E.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
-
(3) 将净化后的河水进行如图2所示的电解水的实验,试管(填“a"或“b”)中收集的气体是氧气,请写出这里发生的符号表达式。
-
(4) 长期饮用硬水可能会引起体内结石。若想检验自来水是硬水还是软水,可加入适量的;生活中用方法降低水的硬度。

-
(1) 写出化学式:B。
-
(2) 物质G的用途。
-
(3) 反应III的基本反应类型是。
-
(4) 反应II的化学方程式为。
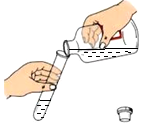 B . 稀释浓硫酸
B . 稀释浓硫酸 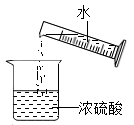 C . 蒸发食盐水
C . 蒸发食盐水 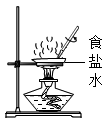 D . 加热并振荡液体
D . 加热并振荡液体 
| 选项 | 实验目的 | 实验方法 |
| A | 分离获取空气中的主要组成成分 | 先将空气液化,再升温逐一气化 |
| B | 区分羊毛制品和化纤制品 | 取样灼烧,闻气味 |
| C | 鉴别黄金和黄铜(铜锌合金) | 分别加入稀盐酸,观察现象 |
| D | 除去NaCl固体中混有的少量Na2SO4杂质 | 加入过量BaCl2溶液,过滤 |

-
(1) 大量CO2直接排放到空气中会导致的加剧,破坏人类生存的环境。捕捉室内反应的化学方程式为。
-
(2) 操作①的名称,所用到的玻璃仪器有烧杯、玻璃棒和。
-
(3) 往纯碱溶液中加入X溶液,得到NaOH溶液和CaCO3 , X的化学式是。
-
(4) 整个流程中可以循环使用的物质是。(写化学式)

-
(1) 粗盐提纯实验过程中发现过滤速度较慢,可能的原因是;在蒸发操作中,当蒸发皿中出现时,停止加热。
-
(2) 配制100g质量分数为6%的氯化钠溶液,计算需要水的质量为g;从上图选出配制该溶液的主要操作顺序(选填序号);若向烧杯中倒水时部分水洒出,最终会导致配制的溶液中溶质的质量分数(填“>”或“=”或“<”)6%。
选项 | 实验目的 | 实验设计 |
A | 除去CO中的水蒸气 | 通过足量的生石灰 |
B | 除去CaCl2溶液中少量的盐酸 | 加入足量的生石灰,过滤 |
C | 鉴别NaOH溶液和Na2CO3溶液 | 分别滴加无色酚酞溶液 |
D | 鉴别Na2SO4溶液与稀H2SO4溶液 | 分别滴加Ba(NO3)2溶液 |

-
(1) C物质的化学式为。
-
(2) F物质的一种用途为。
-
(3) A-B反应的化学方程式为。
-
(4) D→E的基本反应类型为。



