第1节 性质活泼的氧气 知识点题库
-
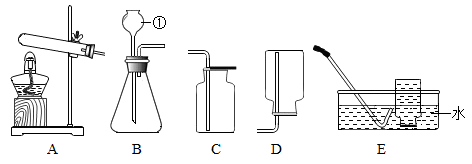
(1) 写出图中仪器①的名称。
-
(2) 实验室制备气体时,应先,实验室用加热氯酸钾和二氧化锰混合物的方法制取并收集氧气,应选用的装置为(填字母)反应的化学方程式为。若选用装 置 E 的方法收集氧气,待时开始收集氧气。
-
(3) 氨气是一种无色、有强烈刺激性臭味的气体,密度小于空气,极易溶于水。水溶液 呈碱性。实验室常用加热氯化铵和熟石灰两种固体混合物来制取氨气。其发生和收集装置为(填字母)
-
(4) 实验室收集气体,根据、选择收集装置。
-
(5) 工业上可以利用制取氧气。
-
(6) 如果选如图装置收集氢气(最轻气体),气体应从(填“a”或“b”)端导入。 若用如图排水法收集氧气,装满水后,氧气应从 (填“a”或“b”)端导入。
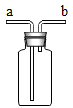
A、H2
B、O2
C、H2O
D、N2
-
(1) 能作食品保护气体是;
-
(2) 电解水时负极产生的气体的是;
-
(3) 保持水的化学性质的最小粒子是;
-
(4) 能支持燃烧的气体是。

-
(1) 写出有标号的仪器的名称:
①.
② .
③ .
④.
-
(2) ①实验室制取氧气时,将导管、橡皮塞和大试管连接后,
进行气密性检查的方法是:将,如果导管口有,则装置不漏气.
②试管口塞一团棉花,作用是.
③试管口略向下倾斜,目的是.
④除了可以用排水法收集到氧气,还可以用法收集氧气.
-
(3) 写出加热高锰酸钾制取氧气的化学方程式:.
 用氯酸钾制取氧气
B .
用氯酸钾制取氧气
B .  等质量碳酸钙与足量同浓度稀盐酸反应
C .
等质量碳酸钙与足量同浓度稀盐酸反应
C .  硝酸铵溶于水时溶液的温度变化
D .
硝酸铵溶于水时溶液的温度变化
D .  发生的反应为:2KNO3
发生的反应为:2KNO3  2KNO2+O2↑
2KNO2+O2↑

-
(1) 图中d仪器的名称:
-
(2) 若用高锰酸钾制取氧气,反应的化学方程式是;应选用的发生装置和收集装置是(填字母)。
-
(3) 若用F装置检验二氧化碳,应在其中装入适量的,出现现象时,证明有二氧化碳产生。
-
(4) 若要收集氢气,可以使用C或E装置收集的原因是;若选用F装置收集氢气,气体应从(填“a”或“b”)导管口通入。
-
(1) 占空气体积78%的是。
-
(2) 绿色植物光合作用吸收的气体是。
-
(3) 空气中能支持燃烧的气体是。
-
(4) 证明空气中含有水蒸气的事例是。
-
(5) 氮气可以充填食品的包装袋中用于防腐,其原因是。

①写出图中标号的仪器名称:a,b;
②写出用A装置制取氧气的文字表达式:;B装置中试管口略向下倾斜的原因是;若将B、C装置组装在一起制氧气,实验结束,停止加热前要先进行的操作是。
③若用过氧化氢溶液和二氧化锰制取氧气,应选用的发生装置是(填字母)。在加试剂之前的操作是。
④收集较纯净的氧气可选用的装置是(填字母)。
⑤已知一氧化氮气体的密度比空气略大,难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置(填字母)。

-
(1) 请写出标有序号的仪器名称:①,②。
-
(2) 实验室若用高锰酸钾制取氧气,选择的发生装置是(填字母);但要对装置进行改进,改进的地方是。
-
(3) 选择E装置收集氧气的理由是,若用排水法收集氧气,所得气体不纯的原因可能是(答一条)。
-
(4) 向组装好的气体发生装置中加入药品前,应该进行的操作是。实验结束后,应先将导管从水中取出,再熄灭酒精灯,其目的是。
-
(5) 用过氧化氢溶液和二氧化锰制氧气,二氧化锰在反应中的作用是。该反应的文字表达式是
-
(6) 与集气瓶配套使用的玻璃片一般一面为光滑面,另一面为磨砂面,收集气体时用玻璃片的(填“光滑面”或“磨砂面”)盖好集气瓶。

| A | B |
| ⑴实验室用高锰酸钾制取氧气的化学方程式是。 ⑵选用的发生装置和收集装置分别是。 ⑶检验集气瓶内为氧气的操作是。 | ⑴实验室制取二氧化碳的化学方程式是。 ⑵选用的发生装置和收集装置分别是。 ⑶检验集气瓶内若为二氧化碳的操作是。 |

-
(1) 利用A装置制取氧气,试管口处棉花的作用是。
-
(2) 若用过氧化氢制取氧气,选择的反应装置是(填字母),写出反应的文字表达式。
-
(3) 用D装置收集二氧化碳时,检验二氧化碳已经收集满的方法是。
-
(4) D装置的用途很广。下列关于该装置用法正确的是(填序号)。
①当装置内盛满氧气时,若将装置内的氧气排出来,水应从b口通入
②当装置内盛满水,若收集氧气,气体应从b口通入
③当装置内盛有一半水时,为观察给病人输氧气的速率,a口应连氧气钢瓶
-
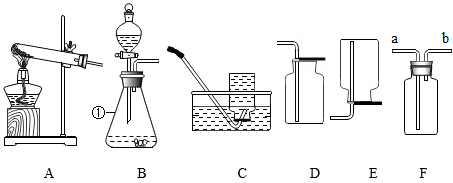
(1) 写出图中标有数字的仪器名称,①的名称是。
-
(2) 实验室用氯酸钾来制取氧气,选择的发生装置为(填序号),试管口稍向下倾斜的原因是,该反应的化学方程式为;为了收集较为纯净的氧气,最好选用的收集装置是(填序号);若改用高锰酸钾制取氧气,发生装置应作出的改进是:;实验结束时的正确操作顺序为:先,后;用向上排空气法收集氧气时的验满方法是。
-
(3) 实验室用石灰石和稀盐酸反应制取二氧化碳,选用的发生装置是(填序号), 该发生装置的优点是;若用装置F收集二氧化碳气体,气体应从(填a或b)端进入。
-
(4) 若用装置E收集某种气体,则该种气体应具备的性质。
-
(1) 空气是与我们人类生存密切相关的物质,空气是一种宝贵的资源。
①蜡烛能在空气中燃烧,说明空气中含有;
②随着工业的发展,排放到空气中的会加剧温室效应;
③酥脆的饼干露置在空气中变软,说明含有;
④新鲜食品常采用真空包装或向包装内填充氮气做保护气,目的是。
-
(2) 化学是一门以实验为基础的科学,认识仪器和学会基本操作是做好实验的保证。
①初中化学实验室常用于测量液体体积的仪器是;
②倾倒细口瓶里的药液时,标签没向着手心的后果是。
-
(3) 用实验探究物质的性质也是化学常用方法。氧气是一种化学性质比较活泼的气体,它可以和许多物质发生化学反应。如图所示是硫粉、红磷、光亮的细铁丝在氧气中燃烧的实验装置:

①小冉是个善于思考、善于总结的学生,做完实验后,她发现了一些共同点:在反应条件方面,三个实验都要,在能量变化方面,三个实验都是反应(填“吸热”或“放热”),在反应基本类型方面,三个化学反应都是反应。
②小冉同时也总结出在生成物的种类、状态和观察到的实验现象三个方面存在不同。请你替小冉同学填写空格:甲中发生反应的文字表达式是,丙中观察到的反应现象是。
③小冉还总结出:三个实验的集气瓶底部都放有少量水,其中甲集气瓶底部放少量水的目的是。丙集气瓶中的水也可以用代替。
-
(4) 对常见物质进行分类是学习化学物质的基础。现有下列七种物质:①清新的空气;②铁粉;③从空气中分离出来的稀有气体;④二氧化碳;⑤液氧;⑥一种黑色的固体粉末。肯定属于混合物的有(填序号,下同),肯定属于纯净物的有,肯定含有氧气的是。
-
(1) 露在空气中的饼干变软是因为空气中有;
-
(2) 五彩霓虹灯内充的气体是;
-
(3) 可用于炼钢、气焊的气体是;
-
(4) 能使澄清石灰水变浑浊的气体是。
-
(1) 从空气成分看,请根据下列现象说明空气中分别存在哪种物质(填物质名称)。
①很多物质在空气中能燃烧。
②敞口存放在空气中的澄清石灰水过一段时间后变浑浊了。
-
(2) 从空气的用途角度看。
①稀有气体可用于填充霓虹灯,所利用的稀有气体的性质是。
②冰箱中常用“气调保鲜”来达到对食物保鲜的效果。下图所示是工业上用膜分离技术实现“气调保鲜”的流程。

在空气分离后,进入冰箱保鲜室内的气体是(填“富氧空气”或“富氮空气”)。富氧空气中氧气和其他气体的体积比可能是(填字母代号)。
A.1:3 B.1:4 C.1:5
-
(3) 从防治空气污染角度看,空气质量日益受到人们的关注。目前计入空气污染指数的有害气体和烟尘主要包括:一氧化碳、二氧化硫、二氧化氮、臭氧、可吸入颗粒物(PM2.5、PM10),总悬浮颗粒物等,其中的“PM2.5”是指下列____(填字母代号)。A . 空气的湿度 B . 空气的透明度 C . 空气中有害气体的浓度 D . 空气中直径不超过2.5um的颗粒物
-
(4) 从环保角度看,某同学就有关改善空气质量的具体措施给市“创城办”提出建议:①安排洒水车在城市主干道洒水②植树造林,增加小区绿地面积③将有污染的化工厂搬迁至城郊④将公交车全部改成电车以上四条建议中,你认为符合实际,且有利于提高空气质量的合理化建议是(填数字序号)。
-
(1) 验证质量守恒定律。
步骤1:在锥形瓶中加入适量的CuSO4溶液,塞好橡胶塞。将几根铁钉用砂纸打磨干净,将盛有CuSO4溶液的锥形瓶和铁钉一起放在托盘天平上称量,记录所称质量为m1。
步骤2:将铁钉浸入到CuSO4溶液中,塞好橡胶塞。观察实验现象,待反应有明显现象后,将盛有CuSO4溶液和铁钉的锥形瓶一起放在托盘天平上称量,记录所称质量为m2
①用砂纸将铁钉打磨干净的作用是。
②步骤2中可观察到明显的实验现象是。该变化可说明Fe和Cu的金属活动性由强到弱的顺序是。
③若m1=m2 , 可证明参加反应的Fe和CuSO4的质量总和等于。
-
(2) 探究CuSO4溶液对H2O2分解具有催化作用。
①若要证明CuSO4溶液对H2O2分解具有催化作用,除需证明CuSO4在反应前后化学性质和质量不发生改变外,还需证明的是。
②为探究CuSO4在反应前后质量是否发生改变,某同学设计如下实验:
向H2O2溶液中滴入10ga%的CuSO4溶液,待反应完全后,向试管中加入足量的BaCl2溶液,产生沉淀,过滤、洗涤、干燥,称量沉淀物为bg。
上述实验步骤中若缺少“洗涤、干燥”,则通过沉淀物bg计算出溶液中CuSO4的质量0.1ag。(填“大于”或“小于”或“等于”)
-
(3) 将16.0gCuSO4置于坩埚中加热,固体质量与成分随温度变化的曲线如图所示。

①650℃时,CuSO4开始发生分解反应,生成CuO和另一种氧化物X,X的化学式为。
②1000℃时,CuO开始发生分解反应,生成Cu2O和O2.计算图中m的值。(写出计算过程)



