第2节 化学反应中的质量关系 知识点题库
我国使用“长征3号甲”运载火箭的动力是由高氯酸铵(NH4ClO4)分解所提供的,反应方程式为2NH4ClO4  N2↑+Cl2↑+4X↑+2O2↑,则X的化学式为( )
N2↑+Cl2↑+4X↑+2O2↑,则X的化学式为( )
 N2↑+Cl2↑+4X↑+2O2↑,则X的化学式为( )
N2↑+Cl2↑+4X↑+2O2↑,则X的化学式为( )
A . NH3
B . H2
C . H2O
D . HCl
推理是学习化学的一种重要方法,下列推理关系成立的是( )
A . MnO2是加快H2O2分解的催化剂,所以催化剂是加快化学反应速率的物质
B . 水电解产生氢气和氧气,所以水是由氢气和氧气组成的
C . 空气中可燃物燃烧必须与氧气接触,所以把可燃物与氧气隔绝是灭火的有效方法之一
D . 镁条在空气中燃烧得到的氧化镁的质量与参加反应的镁条质量不同,故该反应不符合质量守恒定律
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示。下列说法中不正确的是( )

A . 该反应为化合反应
B . 丙可能为该反应的催化剂
C . 乙、丁两物质的相对分子质量之比为7:5
D . 该反应中,甲、乙的质量变化之比为2:7
取锌、铜的混合物8g与154.7g稀硫酸恰好完全反应,称得剩余物质的总质量为162.5g。请计算:
-
(1) 产生氢气的质量是多少?
-
(2) 混合物中铜的质量是多少?
鸡蛋壳的主要成分是碳酸钙,为了测定蛋壳中碳酸钙的质量分数,小东和小军同学进行了如下实验,相关实验数据如图所示:

-
(1) 小东根据“蛋壳残渣质量为4.3克”,求得蛋壳中碳酸钙的质量分数为;
-
(2) 小军根据“反应过程中减少的质量”(10克+100克﹣106.7克=3.3克)也求得了蛋壳中碳酸钙的质量分数,请你写出小军的计算过程和结果。
-
(3) 小东和小军经过反复实验得出该鸡蛋壳中碳酸钙的质量分数与小军结果吻合,请分析小东开始所得结果出现误差的可能原因是。
下列关于用红磷验证质量守恒定律说法错误的是()

A . 暗红色的红磷燃烧,放热,产生大量白烟
B . 小气球的作用之一是为了使装置保持密闭
C . 该实验不能用于验证质量守恒定律
D . 冷却到室温时,拔开橡胶塞后又盖好,称量,指针偏左
下列归纳和推理,你认为不合理的是( )
A . 氢气点燃前需验纯,则点燃任何可燃性气体前都需验纯
B . 某物质在空气中燃烧生成水,则该物质中一定含有氢元素
C . 化合物含有不同种元素,则由不同种元素组成的纯净物一定是化合物
D . NaOH溶液能使无色酚酞试液变红,则 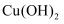 也能使无色酚酞试液变红
也能使无色酚酞试液变红
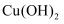 也能使无色酚酞试液变红
也能使无色酚酞试液变红
四种物质在一定的条件下充分混合反应,测得反应前后各物质的质量分数如图所示。则有关说法中错误的是()

A . 该反应一定是分解反应
B . 生成的甲、丙两物质的质量比为8:1
C . 乙可能是这个反应的催化剂
D . 参加反应的丁的质量一定等于生成甲和丙的质量之和
高氯酸铵(NH4ClO4)可以为运载火箭提供动力,它分解可能排放出的气体()
A . H2O
B . SO2
C . CO2
D . CH4
科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为4NH3+3O2  2X+6H2O。下列说法中不正确的是( )
2X+6H2O。下列说法中不正确的是( )
 2X+6H2O。下列说法中不正确的是( )
2X+6H2O。下列说法中不正确的是( )
A . 氨气在常压下液化是物理变化
B . X的化学式为N2
C . 液氨具有可燃性属于化学性质
D . 液氨属于混合物
如图为某化工企业生产流程示意图。下列说法正确的是()

A . 钛酸亚铁(FeTiO3)中钛元素为+3价
B . ①中反应为:2FeTiO3+6C+7Cl2  2X+2TiCl4+6CO,则X为FeCl2
C . ③中为提高转化效率,可使用足量的金属镁
D . ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1
2X+2TiCl4+6CO,则X为FeCl2
C . ③中为提高转化效率,可使用足量的金属镁
D . ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1
 2X+2TiCl4+6CO,则X为FeCl2
C . ③中为提高转化效率,可使用足量的金属镁
D . ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1
2X+2TiCl4+6CO,则X为FeCl2
C . ③中为提高转化效率,可使用足量的金属镁
D . ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1
你认为下列物质不能用作制取氧气的物质是( )
A . 水  B . 甲烷
B . 甲烷  C . 氯酸钾
C . 氯酸钾  D . 高锰酸钾
D . 高锰酸钾 
 B . 甲烷
B . 甲烷  C . 氯酸钾
C . 氯酸钾  D . 高锰酸钾
D . 高锰酸钾 
气焊和气割都需要用到乙炔。乙炔俗称电石气(化学式为C2H2),是一种无色无味的气体,密度比空气略小,难溶于水。实验室常用块状固体碳化钙(CaC2)与水反应制备乙炔,该反应比二氧化锰催化过氧化氢分解更加剧烈。请回答:

-
(1) 图中仪器a的名称是,b的名称是。
-
(2) 写出乙炔的物理性质之一:。
-
(3) 从图中选择实验室制备乙炔所用仪器的最佳组合是(填序号)。
-
(4) 碳化钙(CaC2)与水反应的化学方程式为CaC2+2H2O=X+C2H2↑,X是一种碱,则X的化学式为。
同学们在实验室加热20克高锰酸钾制取氧气,制得所需气体后,停止加热冷却后称量剩余固体质量为18.4克。计算。
-
(1) 生成氧气的质量。
-
(2) 参加反应的高锰酸钾的质量。
下列对四类化学基本观念的认识错误的是( )
A . 元素观:金刚石和石墨均由碳元素组成
B . 分类观:从组成上看干冰和酒精都属于化合物
C . 能量观:氢气和天然气都会放出大量的热
D . 守恒观:水电解前后,分子的种类和质量均不变
已知某两种物质在光照条件下能发生化学反应,其微观示意图如下,图中相同小球代表同种原子,原子间的短线代表原子结合。下列从图中获得的信息中正确的是( )

A . 图中共有3中不同的分子
B . 说明反应中分子不可分
C . 该反应中没有单质参加
D . 图中反应符合质量守恒定律
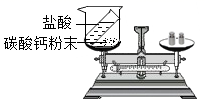
某学校某兴趣小组设计了用盐酸与碳酸钙粉末反应来验证反应前后物质的总质量是否发生变化。
| 编号 | A | B | C | D |
| 反应前/g | 55.5 | 55.3 | 55.6 | 55.8 |
| 反应后/g | 55.5 | 58.5 | 54.2 | 54.8 |
-
(1) 某同学使用如图装置进行实验,四组实验中分别进行了两次称量,得到下表数据,其中有问题的两组数据是(填序号)。
-
(2) 根据质量守恒定律判断,镁条在空气中完全燃烧,生成物质量与镁条质量相比,生成物质量(填“减少”、“不变”、“增大”)。
-
(3) 通过交流反思得到启示,在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加的反应一定要在装置中进行。
-
(4) 从微观角度分析,在化学反应前后一定不变的是(填序号)。
A 原子种类
B 分子种类
C 元素质量
D 原子数目
E 分子数目
科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为  .X的化学式为是( )
.X的化学式为是( )
 .X的化学式为是( )
.X的化学式为是( )
A . N2
B . N
C . NO
D . N2O
84消毒液是一种以次氯酸钠为主的消毒剂,主要成分为次氯酸钠(NaClO).它的消毒原理为:2NaClO+CO2+H2O=X+2HClO,则X的化学式为( )
A . NaCl
B . NaHCO3
C . NaOH
D . Na2CO3
在“质量守恒定律”的课堂教学中,老师引导学生们进行“化学反应中,反应物与生成物的质量关系”实验探究。他们使用的实验装置和药品如下图所示,现分别以A、B、C表示。

-
(1) (实验验证)A、B、C三个实验分别由甲、乙、丙三个组的同学来完成,他们都进行了规范的操作、准确的称量和细致的观察。
A实验装置中小气球的作用是。
-
(2) B实验反应后天平不平衡,指针向(填“左”或“右”)偏转,反应后天平不平衡的原因是。
-
(3) C实验反应前物质总质量反应后物质总质量(填“>”、“<”或“=”)。
-
(4) (反思与评价)
上述实验A、B、C中能用来验证质量守恒定律的是(选填字母编号)。
-
(5) 在探究化学变化中反应物和生成物的质量关系时,若是有气体参加或有气体生成的反应,应采用容器。
-
(6) (拓展应用)下列事实遵守质量守恒定律的是(选填字母编号)。
A.10g水受热变成10g水蒸气 B.蜡烛燃烧变短
C.酒精久置变轻 D.在一定条件下,石墨转化为金刚石
最近更新



