3.1 氧气的性质和用途 知识点题库
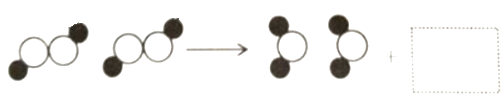
如图为某化学反应在催化剂作用下的微观模拟示意图,其中“

![]() ”和“
”和“![]()
![]() ”分别表示氢原子和氧原子.
”分别表示氢原子和氧原子.

-
(1) 虚线框内应填的微观示意图是 (填序号).A .

 B .
B . 
 C .
C . 
 D .
D . 

-
(2) 结合如图,从原子、分子的角度分析,在化学反应过程中,可分,而不能再分.
-
(3) 请写出该反应的化学方程式.
-
(1) 【猜想和假设】根据所学知识,猜想三种金属在金属活动顺序中的相对位置关系:
猜想一:Cr Al Cu 猜想二:Al Cr Cu 猜想三:。
-
(2) 【实验和探究】
小娟的实验:取大小相同的铝、铬、铜三种金属片(用砂纸打磨光亮)
实验步骤
实验现象
解释与结论
分别取三支试管,向其中入等质量、等浓度的稀硫酸,然后将铝、铬、铜三种金属分别插入三支试管中.
铝片表面产生的气泡较快;
铬片表面产生气泡较缓慢,溶液变蓝色;
铜片无明显现象.
猜想成立.
铬与稀硫酸反应生成蓝色的
硫酸亚铬(CrSO4)溶液,该反应的化学方程式为.
-
(3) 小涛的实验:
小涛只选用了三种药品进行实验,也得出了三种金属在金属活动顺序中的相对位置关系.则他选用的三种药品可能是.
-
(4) 【总结与归纳】由上述实验得出比较金属活动性强弱的方法有:①②。
-
(1) 煅烧石灰石可制得活性CaO,反应的化学方程式为。
-
(2) 为测定不同煅烧温度对CaO活性的影响,取石灰石样品分为三等分,在同一设备中分别于800℃、900℃和1000℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时间的变化如下图所示。
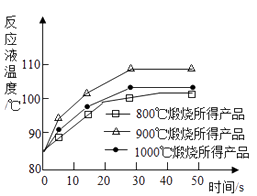
可知:CaO与水反应会热量(填“放出”或“吸收”);上述温度中,℃煅烧所得CaO活性最高。要得出正确结论,煅烧时还需控制的条件是。
-
(3) 以电石渣(主要成分为Ca(OH)2 , 还含有少量MgO等杂质)为原料制备高纯CaCO3的流程如下:
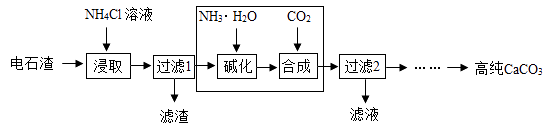
①如图为NH4Cl浓度对钙、镁浸出率的影响:
(浸出率=
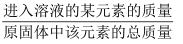 ×100%)
×100%)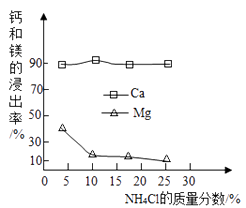
可知:较适宜的NH4Cl溶液的质量分数为;浸取时主要反应的化学方程式为
②流程中方框内部分若改用溶液(填化学式),可一步得到与原流程完全相同的生成物。
③流程中方框内部分若改用Na2CO3溶液,也能得到高纯CaCO3 , 试从生成物的角度分析原流程的优点:
a.NH3可循环利用; b.。
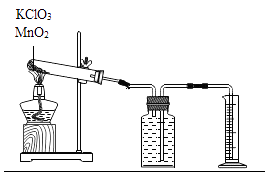
实验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
二氧化锰的质量/g | 0.1 | 0.2 | 0.33 | 0.4 | 0.5 | 0.66 | 1 | 1.3 | 2 | 3 |
二氧化锰与氯酸钾的质量比 | 1:20 | 1:10 | 1:6 | 1:5 | 1:4 | 1:3 | 1:2 | 2:3 | 1:1 | 3:2 |
生成200mL氧气时间/秒 | 235 | 186 | 162 | 147 | 133 | 117 | 143 | 160 | 211 | 244 |
请回答下列问题:
-
(1) 请写出实验室加热氯酸钾和二氧化锰混合物制取氧气的化学方程式。
-
(2) 此实验中,收集气体前集气瓶内未装满水,对本实验的结果(填“有”或“没有”)影响。
-
(3) 分析上述数据,你认为利用此法制取氧气,二氧化锰与氯酸钾的最佳质量比为。
-
(4) 催化剂能影响化学反应速率,温度、反应物浓度、接触面积等也会对化学反应速率带来影响。分析上表数据,结合影响化学反应速率的因素分析:当二氧化锰与氯酸钾的质量比高于最佳质量比时,反应速率变低的原因是:。
在陆老师的指导下,A组同学将二氧化锰与氯酸钾以最佳质量比混合,成功的制取并收集了几瓶气体,但意外的发现制得的气体有刺激性气味,于是在陆老师的指导下对该气体成分进行探究。
-
(5) 【提出问题】氯酸钾与二氧化锰混合加热后产生的气体成分是什么?
【查阅资料】
Ⅰ.氯酸钾与二氧化锰混合加热产生的气体只以单质形式存在;
Ⅱ.氯气(Cl2)是有刺激性气味的气体,能溶于水,能使湿润的淀粉碘化钾试纸变蓝。
【猜想与假设】
猜想一:该气体为 ; 猜想二:该气体为Cl2; 猜想三:该气体为Cl2和O2。
-
(6) 【实验探究】
序号
实验操作
实验现象
实验结论
①
小芳用排水集气法收集A、B两瓶气体,将带火星木条伸入A中;湿润的淀粉碘化钾试纸伸入B中
A中带火星木条复燃,B中淀粉碘化钾试纸不变色。
猜想成立
②
小兰用向上排空气法收集C、D两瓶气体,将带火星木条伸入C中,湿润的淀粉碘化钾试纸伸入D中
C中带火星木条(填“复燃”或“不复燃”),D中淀粉碘化钾试纸变蓝。
猜想三成立
-
(7) 【反思与评价】小虎认为小芳的结论不正确,原因是。
-
(8) 【拓展应用】
Ⅰ.若取氯酸钾和二氧化锰混合加热后的少量固体,加入足量水溶解,过滤,滤液成紫红色,该现象说明该反应还生成了。
-
(9) Ⅱ.MnO2不仅能作催化剂还可以作反应物,实验室通常用MnO2与浓盐酸共热制取Cl2。请完成该反应的化学方程式:
MnO2+4HCl(浓)
 MnCl2+2+Cl2↑.
MnCl2+2+Cl2↑. -
(10) 【计算】12.25g纯净的氯酸钾固体中氧元素的质量是克。

| 内容步骤 | 【实验1】研究氧气性质 |
| Ⅰ | 烧杯中盛有石灰水,燃烧匙中放入木炭,点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞 |
| Ⅱ | 推入适量H2O2 溶液 |
-
(1) 实验1中,推入H2O2溶液后,集气瓶中现象是;推入H2O2溶液后,观察到烧杯中的现象是。
-
(2) 推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶.该实验中,集气瓶内压强的变化过程是。
-
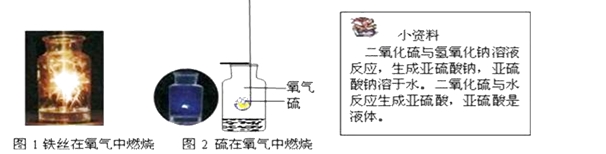
(1) 图1中反应的文字表达式,集气瓶中加入水的作用是。
-
(2) 图2中反应的文字表达式为,集气瓶中加入的液体可能,其目的为。硫在空气中燃烧,不如在氧气中燃烧剧烈的原因是。
①都产生热量 ②都发光 ③都属于氧化反应 ④都很激烈 ⑤都与氧接触 ⑥温度都达到着火点
-
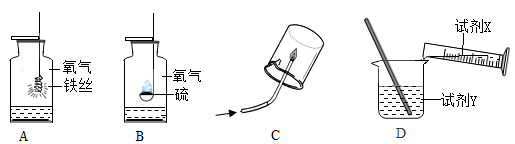
(1) 在做“物质在盛有氧气的集气瓶中燃烧”的实验时,常常要在集气瓶里预先加少量的水。B实验中水的主要作用是,A、B两个实验中的水可用少量细沙代替的是。
-
(2) C是某气体在空气中燃烧的实验。能观察到火焰上方冷而干燥的烧杯壁有水滴出现说明该气体中一定含有元素;然后迅速把烧杯倒过来,向烧杯内注入少量澄清石灰水,振荡,观察到澄清石灰水变浑浊,说明该气体中一定含有元素。
-
(3) D是稀释浓硫酸的实验。正确操作中试剂X是,用玻璃棒搅拌的目的是。
-
(1) 能支持燃烧的是
-
(2) 能使人中毒的
-
(3) 能是紫色石蕊试液变红色的是
-
(4) 天然气的主要成分
-
(5) 能在空气中燃烧的单质
-
(6) 焊接金属时常用保护气的是
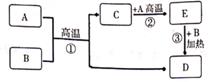
请回答:
-
(1) 物质B的化学式为;
-
(2) 反应①的化学方程式为;
-
(3) 反应②属于哪种基本类型 。



