课题2 化学是一门以实验为基础的科学 知识点题库
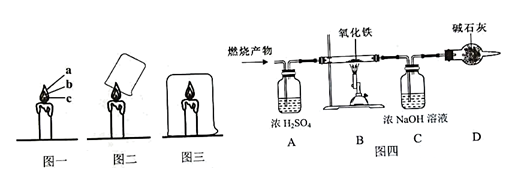
(1)如图1所示是实验室制取气体时常用的装置,回答下列问题:
①写出图中有标号的仪器名称.a:;b: .
②用A或B装置都可以制取氧气,用高锰酸钾制取氧气的化学反应方程式为;C、E、F均可用于收集氧气,若用F装置收集氧气,气体应从端进入(填“m”或“n”).若用C装置收集氧气,验满的方法是 .
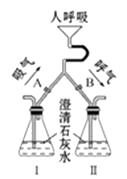
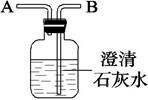
(2)为了证明人体新陈代谢过程中有CO2气体产生,某校兴趣小组的学生设计了如图2所示实验装置进行实验(实验室只用嘴吸气和呼气).请回答:
①图2中瓶Ⅱ的作用是 .
②实验中若猛吸猛呼,会造成不安全后果.猛吸时会使装置Ⅰ中的溶液进入口腔.猛呼时会 . 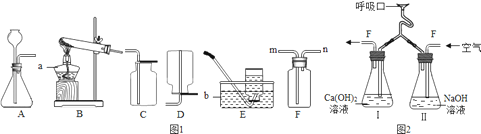
-
(1) 提出问题:生产蜡烛的原料中主要有哪些元素?
假设与猜想:主要原料为有机物,猜想:①一定有元素;②可能还有氢元素和氧元素.
实验设计:根据上述三种元素的猜想制订实验方案.
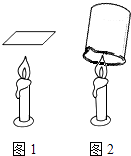
如图1所示,在蜡烛火焰上方放置一块洁净、干燥的玻璃片,一会儿观察到玻璃片上生成一些细小的水珠.
-
(2) 如图2所示,在蜡烛火焰上方罩一个内壁附着有的烧杯,观察现象.
证据与结论:
实验(1),观察到玻璃片上有细小水珠时,说明原料中一定存在(填元素符号).
实验(2),观察到烧杯内壁附着的,则猜想①成立.
分析与交流:实验(1)和实验(2)获得的证据均不能证明原料中一定存在元素,因为
-
(1) 取一支蜡烛,用小刀切下一小块,把它放入水中,蜡烛浮在水面.
结论:石蜡的硬度比较,密度比水.
-
(2) 点燃蜡烛,观察到蜡烛火焰分为外焰、内焰、焰心三层.把一根火柴梗放在蜡烛的火焰中(如图)约1s,取出可以看到火柴梗在层部分最先碳化(出现焦黑斑).
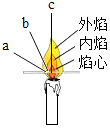
结论:蜡烛火焰的层温度最高.
-
(3) 再将一只干燥的烧杯罩在蜡烛火焰的上方,烧杯内壁出现,片刻后取下烧杯,迅速向烧杯内倒入少量的澄清石灰水,振荡后发现.
结论:石蜡燃烧产生了和.
-
(1) 取一支蜡烛,用小刀切下一小块,把它放入水中,蜡烛浮在水面上.结论:石蜡的密度比水;
-
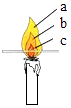
(2) 点燃蜡烛,观察到火焰分为、、三层.把一根火 柴梗放在火焰中(如图)约1s后取出可以看到火柴梗的(填“a”、“b”或“c”)处最先碳化.结论:蜡烛火焰的温度最高;
-
(3) 再将一只干燥的烧杯罩在蜡烛火焰上方,烧杯内壁出现,片刻后取下烧杯,迅速向烧杯内倒入少量澄清的石灰水,振荡后发现结论:蜡烛燃烧以后的生成物是.
【查阅资料】普通蜡烛由石蜡和烛芯制成,而吹不灭蜡烛是在烛芯上包裹一层打火石的粉末.打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃.当蜡烛燃烧时,金属并不燃烧.但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃.
-
(1) 【探究与反思】打火石是(填“混合物”或“纯净物”);
-
(2) 这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?.
-
(3) 这种蜡烛也可以熄灭,你采用的方法是:.
-
(4) 【实验探究】吹不灭蜡烛芯内的金属可能是镁、铁或铜的一种,为确定该金属的成分,请你继续探究并完成下列有关问题:(不考虑打火石中稀土元素对探究金属性质的影响)
实验
操作步骤
实验现象
实验结论
1
切开蜡烛,取出打火石,用砂纸打磨.
打火石是银白色
.
2
取少量打磨后的打火石加入试管中,滴加盐酸.
该金属一定不是铁.
3
取少量打磨后的打火石加入试管中,滴加硫酸铜溶液.
有色物质析出.
该金属一定是镁.
-
(5) 【分析思考】请写出“实验3”中可能涉及的化学方程式:.
-
(1) 人吸气时,应将活塞A、B具体的操作。(填“打开”或“关闭”)
-
(2) 人呼气时可观察到Ⅱ瓶内的现象是。Ⅱ瓶中所装试剂的作用是。将上述操作反复进行,能证明人呼出的气体中含有的二氧化碳不是来自空气,而是人体的代谢产物。
探究二氧化碳与水的反应
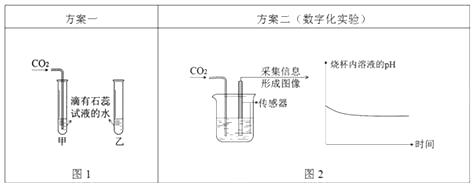
Ⅰ.图1中可观察到甲试管中的紫色液体变为色,写出发生反应的化学方程式,乙试管的作用是;
Ⅱ.由图2坐标图中的曲线可知,烧杯内溶液的酸性逐渐变(填“强”或“弱”)。
探究蜡烛燃烧的产物
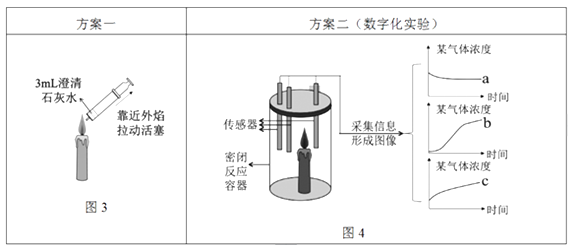
Ⅰ.如图3所示,用注射器在蜡烛外焰部位抽气并振荡,可观察到,证明反应生成了二氧化碳;若将干冷的烧杯罩在火焰上方,观察到,证明反应生成了水。
Ⅱ.如图4所示,蜡烛在密闭容器内燃烧,同时监测容器内氧气、二氧化碳和水蒸气含量的变化,形成三条曲线如坐标图所示,曲线(选填“a”、“b”、“c”)能够说明蜡烛燃烧生成了二氧化碳和水。
③ 比较块状碳酸钙、碳酸钙粉末与稀盐酸反应的速度
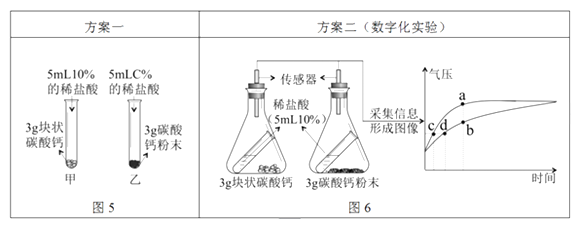
Ⅰ.写出碳酸钙与稀盐酸发生反应的化学方程式;
图5中,乙试管中稀盐酸的浓度C%应为;
较之块状碳酸钙,碳酸钙粉末与稀盐酸的反应更为剧烈,原因是。
Ⅱ.按图6所示进行实验,倾斜锥形瓶使小试管内的稀盐酸流入瓶中与固体接触发生反应,瓶内气压的变化如坐标图所示。对比分析坐标图中的点(选填a~d)可知:两个锥形瓶内达到相同的压强时,碳酸钙粉末与稀盐酸反应所需时间更短。
 B . 滴入数滴澄清石灰水,振荡
B . 滴入数滴澄清石灰水,振荡  C . 燃着的木条伸入集气瓶中
C . 燃着的木条伸入集气瓶中 
-
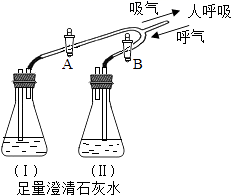
(1) 首先,由(填“A”或“B”)导管吸气约20 s,观察到澄清石灰水,说明空气中二氧化碳的含量(填“低”或“高”)。
-
(2) 然后,由(填“A”或“B”)导管呼气约20s ,观察到澄清石灰水,说明呼出的气体中二氧化碳的含量(填“低”或“高”)。
-
(3) 比较以上两次实验结果,该小组同学得出人体呼出的气体中二氧化碳的含量比吸入的空气中的(填“低”或“高”)
| 鉴别物质 | 实验方法 | |
| A | 二氧化碳、氮气 | 燃着的木条分别伸入集气瓶 |
| B | 水与酒精 | 分别闻气味 |
| C | 呼出气体和新鲜空气 | 分别同速通入澄清的石灰水 |
| D | 蒸馏水与食盐水 | 分别取两种液体少量,加热蒸发 |
-
(1) 如图一,观察到蜡烛燃烧时火焰分为a、b、c三层,其中温度最高的是(填字母序号)。
-
(2) 如图二,取一个冷而干燥的小烧杯罩在火焰上方,观察到烧杯内壁出现,快速倒转烧杯,倒入少量澄清石灰水,振荡,观察到澄清石灰水变浑浊。由此可知,蜡烛燃烧后的产物一定有H2O和(填化学式)。
-
(3) 如果用一个大烧杯扣住蜡烛(如图三),一段时间后,观察到蜡烛熄灭,说明燃烧需要。
-
(4) 为测定某有机物的组成(如图四),往装置中先通入一段时间干燥的氮气,再将6.4g样品在氧气中燃烧后的产物(样品无剩余)依次通过装置A、B、C、D(装置中涉及的每步反应均反应完全),结果发现装置A增重7.2g,装置C增重8.8g。试分析:
①装置A中利用了浓硫酸的。
②装置B中红色粉末变成黑色的原因是(用化学方程式表示)。
③装置C中反应的化学方程式为。
④由此可知,该有机物化学式中碳、氧原子的个数比为(填最简整数比)。
|
实验步骤 |
实验现象 |
实验结论 |
|
点燃其中一支蜡烛,过一会儿用大烧杯罩住点燃的蜡烛 |
|
|
|
|
|
火灾逃生时,需低下身子或贴近地面跑出火灾区 |
-
(1) 人吸气时应将活塞A (填“打开”或“关闭”),活塞B (同上).
-
(2) 人呼气时应将活塞A (填“打开”或“关闭”),活塞B (同上),此时可观察到Ⅱ瓶内的现象是 .
-
(3) Ⅰ瓶所装试剂的作用是 ;Ⅱ瓶所装试剂的作用是 ;将上述操作反复进行,能证明人所呼出的气体中所含的二氧化碳不是来自空气,而是人体的代谢产物.
A.组成完全相同 B.水蒸气含量高 C.二氧化碳含量较低 D.



