实验活动2 二氧化碳的实验室制取与性质 知识点题库
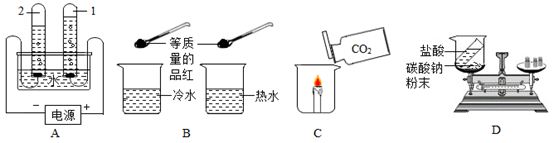
使用如图装置完成的实验是( )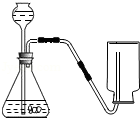
利用化学反应中气体产生的压力,可使多个化学反应依次发生,根据图示回答下列问题(A装置中的试剂足量,B、C、D中的试剂少量):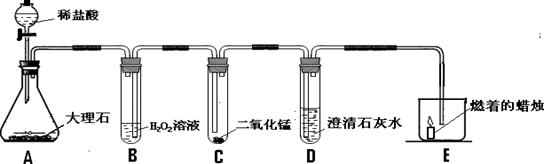
(1)打开A中分液漏斗的活塞,使稀盐酸逐滴滴下,A中的反应方程式是 。
(2)B中观察到的现象是 。
(3)C中开始和后来观察到的现象是 。
(4)D中发生反应的方程式 。
(5)E中的现象是 。

-
(1) 【活动与探究一】收集不同体积比例的二氧化碳和一氧化碳混合气体.
方案一:如图1所示
①请写出硬质玻璃管中发生反应的化学方程式;
②该实验能获得二氧化碳和一氧化碳混合气体,其原因是;
-
(2) 方案二:根据如图2装置所示请回答下列问题:(提示:饱和NaHCO3溶液的作用是除去HCl气体,部分夹持装置及导管已略去)
①写出装置A中发生反应的化学方程式:.
②CO气体应由(填“a”或“b”)通入,在C中混合后,由另一导管导出.
-
(3) 装置C中浓硫酸的两点主要作用:
①干燥气体,减少实验误差;② .
-
(4) 测定某钙片(主要成分CaCO3)中碳酸钙的质量分数,用如图3装置进行如下实验:①取研碎后的钙片4克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入过量的稀盐酸,置于电子天平上测出装置总质量.②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量.③整理相关数据如下表
反应前总质量(克)
275.58
反应后总质量(克)
274.92
小明结合表中数据,计算该钙片中碳酸钙的质量分数.(其它成分不与盐酸反应).
该实验中,如果装置中不加固态干燥剂(干燥剂的作用:吸水但不吸二氧化碳),则最终所算得钙片中碳酸钙的质量将(填“偏大”“偏小”或“不变”).
-
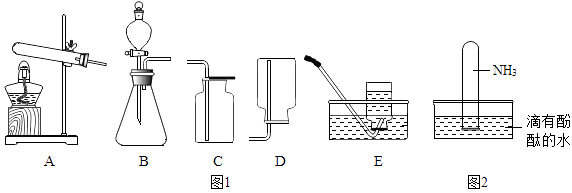
(1) 写出用A装置制取氧气的化学方程式。
-
(2) 加热氯化铵和熟石灰的固体混合物可制取氨气(NH3)。氨气密度比空气小,极易溶于水形成氨水,氨水呈碱性。
①则图2可观察到的现象是:。
②制取氨气应选用的一套装置为(填字母序号)。
-
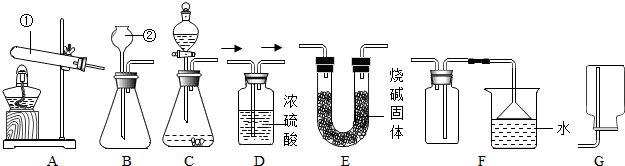
(1) 仪器
 的名称是,洗涤仪器
的名称是,洗涤仪器  时,用到的仪器是;
时,用到的仪器是;
-
(2) 装置B可用于实验室制取,G装置可以收集的气体为,要得到干燥的二氧化碳气体,可以通过下图的装置
 均填字母即可
均填字母即可  ;
;
-
(3) 装置B和装置C都可用于实验室制取氧气,装置C的优点是:可以控制反应的速率,你觉得此说法对吗?
 填“对”或“不对”
填“对”或“不对” 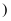 ;
;
-
(4) 实验室可以对用加热氯化铵和熟石灰固体混合物的方法制取氨气。已知氨气是一种无色有刺激性气味的气体,密度比空气小,极易溶于水。为了制取并收集一瓶干燥的氨气,且减少对空气的污染,在上述装置中选出最佳的实验装置组合是。
-
(1) 不同实验对反应速率有不同要求。某同学探究CO2制取实验,按要求答题。 限选控制反应速率的方法:①反应物的浓度 ②反应物的状态
限选试剂:A.稀盐酸
B.浓盐酸
C.块状石灰石
D.碳酸钠溶液 E.粉末状石灰石
填写下表并回答相关问题
实验名称
控制速率的方法
所选用的最佳试剂
灭火器反应原理
①
和D
CO2的实验室制法
;
A和C
写出实验室制备CO2的化学反应方程式:。
-
(2) 已知:CO2和SO2既有相似性,又有差异性。
实验:水槽中滴入紫色石蕊溶液,将收集满两种气体的试管同时倒立于水槽中,片刻后实验现象如下图所示,说明相同条件下的溶解性:SO2 (填“>”或“<”)CO2 , 试管内溶液变成色。
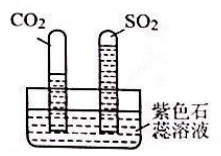
 气体的制取和性质。
气体的制取和性质。
-
(1) A,B,C三套发生装置都可用于实验室制取
 气体。
气体。 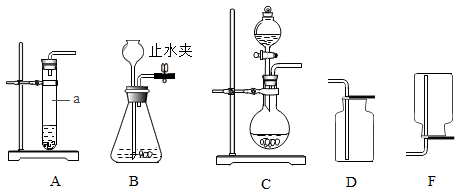
①仪器a的名称是。
②实验室制取
 的化学方程式是;收集
的化学方程式是;收集  可选用的装置是(填序号),检验
可选用的装置是(填序号),检验  收集满的方法是。
收集满的方法是。③利用B装置制取
 时,反应未停止前关闭止水夹,可观察到的现象是。
时,反应未停止前关闭止水夹,可观察到的现象是。④与A装置相比,利用C装置制取
 的优点是。
的优点是。 -
(2) 某化学兴趣小组对
 的性质进行了探究。实验步骤如下:
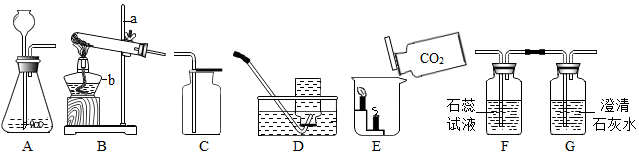
的性质进行了探究。实验步骤如下: 步骤1:如图5所示装置的气密性良好(图中a处连接气体压力传感器),甲、乙、丙三个烧瓶的容积均为250mL,分别收集满
 ,三个注射器内各装有85mL液体。
,三个注射器内各装有85mL液体。步骤2:三位同学同时迅速将注射器内液体全部注入各自烧瓶中,关闭活塞;一段时间后,同时振荡烧瓶。
步骤3:利用“数字化实验”测定烧瓶内的气压变化,得到如图6所示的烧瓶内压强与时间的关系曲线图,曲线1、2、3分别表示甲、乙、丙三个烧瓶内的气压变化。

①实验过程中,观察到烧瓶乙中有白色沉淀生成。写出该反应的化学方程式:。
②曲线1中BC段气压逐渐变小的原因是,导致CD段气压快速变小的操作是。
③对比曲线1与曲线3,能得出的结论是(填序号)。
a.
 能溶于水
能溶于水b.
 能与水发生反应
能与水发生反应c.
 能与NaOH溶液发生反应
能与NaOH溶液发生反应
-
(1) 写出图中有标号的仪器名称:a、b。
-
(2) 写出实验室用B装置制取氧气发生的化学反应方程式。
-
(3) 若装置A中反应剧烈,从实验安全角度考虑,可以将长颈漏斗换成来控制液体的滴加速度。
-
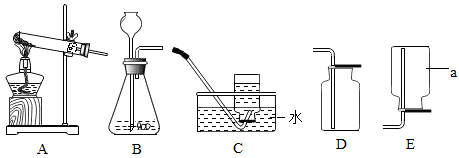
(4) 欢欢同学制取了一瓶二氧化碳气体,按图E进行实验,观察到的现象是,实验说明二氧化碳的性质有。(至少写出两条)。
-
(5) 梅梅同学用图中A、F、G装置组合制取二氧化碳气体并验证相关性质。
①写出制取二氧化碳气体反应方程式,
②F装置中反应现象是,
③G装置中发生的化学反应方程式为。
-
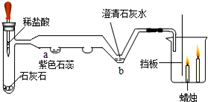
(1) 写出仪器a的名称:。
-
(2) 实验室用加热高锰酸钾的方法制取并收集氧气,应选用的发生装置为(填序号,下同),若要收集较纯净的氧气,则收集装置为。
-
(3) 实验室用过氧化氢溶液和二氧化锰制取并收集氧气,若用D收集,则检验氧气是否收集满的操作为,制取氧气反应的文字表达式为。
-
(4) 比较上述两种制取氧气的方法,请指出用过氧化氢溶液和二氧化锰制取氧气的优点有(写一条即可)。
-
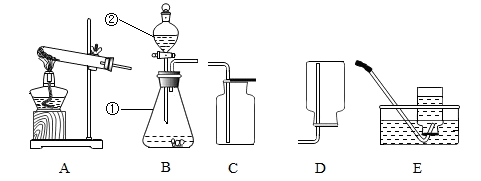
(1) 反应发生后,a处现象为,烧杯内现象为。
-
(2) b处发生的化学方程式为。
-
(3) 若用酒精灯对反应后的a处加热,则现象为。
-
(4) 为测定某石灰石样品中碳酸钙的质量分数,称取10g石灰石(杂质不参加反应)放入烧杯中,加入100g稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为106.7g(气体的溶解忽略不计)。请计算该样品中碳酸钙的质量分数。
-
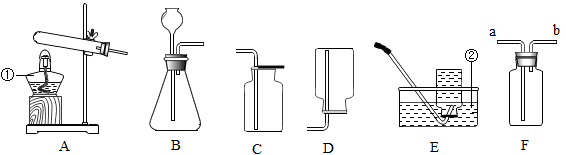
(1) 写出图中带标号仪器的名称:①②
-
(2) 实验室用过氧化氢溶液和二氧化锰制取氧气时,反应的化学方程式为将药品加入装置前,应进行的操作是
-
(3) 实验室用图中B与D组合的装置制取和收集某种气体,由此可推知该气体的物理性质是制取气体的反应一定是(填序号)。
a.不需要加热
b. 需要催化剂
c. 制取氧气的反应
d.反应物中至少一种是液体
-
(1) 写出有标号仪器的名称:①,②。
-
(2) 图A中的试管口略向下倾斜的原因是:。
-
(3) 李强用高锰酸钾制取氧气,他选择上述装置中的A作为制取装置。你认为A装置中还缺少,写出该反应的符号表达式;如果采用排水法收集氧气,应该与(填序号)装置连接,此时当收集满氧气后,应该进行的操作是先,再撤酒精灯。
-
(4) 实验室只用B和C装置也可以制取氧气。请写出在实验室中用B和C装置制取氧气的符号表达式。
-
(5) F是多功能瓶,若用于收集氧气应从(填“a端”或“b端”)通入气体。
-
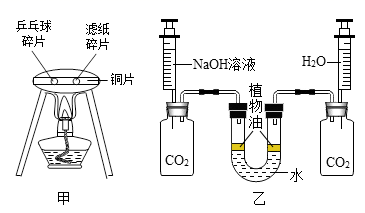
(1) 实验A,试管2中产生的气体是。
-
(2) 实验B,品红在热水中扩散速度比冷水中快,说明影响分子运动速率的因素是。
-
(3) 实验C,观察到蜡烛熄灭。该实验能得出二氧化碳的性质有(填序号)。
A不燃烧 B不支持燃烧 C密度比空气大
-
(4) 用实验D不能验证质量守恒定律,因为反应后逸散到空气中。
-
(1) 实验甲的目的主要是对比出乒乓球碎片和滤纸碎片的不同;
-
(2) 实验乙利用对比实验排除了水对实验的干扰,若观察到U形管左端的液面(填“升高”或“降低”),则证明溶液中的氢氧化钠能与二氧化碳反应,其反应的化学方程式为。
-
(3) 实验丙中,只有A中铁钉生锈了,对比铁钉不同的现象,可推知铁生锈的条件是铁与同时接触。下图的对比实验丙和丁能实现探究目的的是(填序号)。
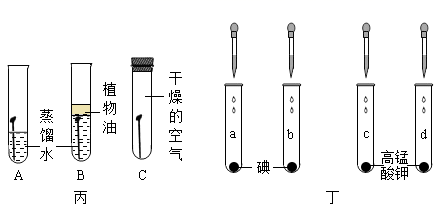
A 实验丙中A,B对比可探究铁的锈蚀与植物油是否有关
B 实验丙中A,C对比可探究铁的锈蚀与水是否有关
C 实验丁中a、b对比可探究物质溶解性与溶质种类是否有关
D 实验丁中b、d对比可探究物质溶解性与溶剂种类是否有关
-
(1) 写出实验室制取CO2的化学方程式: 。
-
(2) 若用如图所示装置(固定装置省略)制CO2:连接好装置后,需检查装置的气密性。具体操作方法是:先 (填字母,下同),后 若导管口有气泡,放手后导管内上升一段稳定的水柱,则气密性良好。
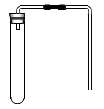
A用手捂住试管
B将导管一端浸入水中
-
(3) 实验室收集CO2可用的方法是 (填字母)。
A排水法
B向下排空气法
C向上排空气法
-
(4) 实验室常用澄清石灰水检验CO2 , 二氧化碳可以使澄清石灰水 。
-
(1) Ⅰ、探究药品选择:
按下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),产生CO2体积随时间变化曲线如图1所示:
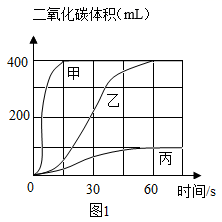
实验编号
药品
1
块状大理石、10%H2SO4溶液
2
块状大理石、7%HCl溶液
3
大理石粉末、7%HCl溶液
图1中甲对应实验(选填“1”“2”或“3”):不选用丙对应的药品制取CO2的理由是;确定选用乙对应的药品制取CO2的化学方程式是。
-
(2) Ⅱ、探究改进装置创新实验:
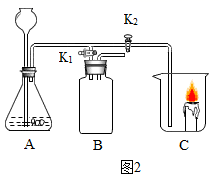

连接装置,检验装置气密性良好。
利用改进装置(如图2)收集并验证二氧化碳的性质:
①打开K2、关闭K1时,可利用A、C装置验证CO2的性质。
②打开K1、关闭K2时,可利用A、B装置制取一瓶CO2。请将B装置中的导管补画完整。补画后检验B中CO2已收集满的方法是。
-
(3) 利用创新实验(图3)粗略测定收集的CO2的体积:
①打开活塞,把稀盐酸加入试管,观察到的现象是。反应结束后进行读数,读数前调节水准管与量气管液面相平的原因是。
②实验中,加入稀盐酸体积为V1mL,左侧量气管最后读数为VmL,则反应生成CO2体积约为mL。该实验条件下CO2密度为dg/mL,则大理石样品中碳酸钙质量表达式为g。
-
(4) Ⅲ、探究不同物质对CO2的吸收效果:
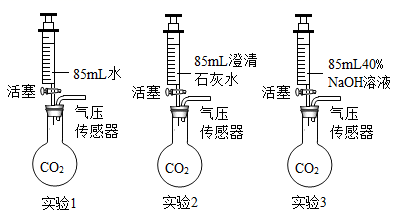
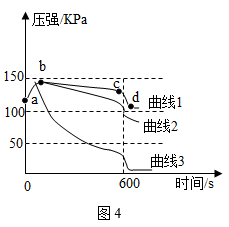
利用已收集满250mLCO2的3个的烧瓶进行实验,如下图所示,同时迅速将注射器内液体全部注入各自烧瓶中,关闭活塞:一段时间后,同时振荡三个烧瓶。分别得到图4所示的烧瓶内压强与时间的关系曲线图。
回答下列问题:
①实验步骤中,曲线1、2、3中导致气压快速变小(如:cd段)的原因是。
②曲线1对应反应的化学方程式为。
③根据图4所示曲线,可以得出的结论是(填字母序号)。
A. 1体积水中溶解CO2的量约为1体积
B. CO2能与水发生反应生成碳酸
C. CO2能与NaOH溶液发生反应
D. 40%NaOH溶液比澄清石灰水更适合用于吸收CO2
-
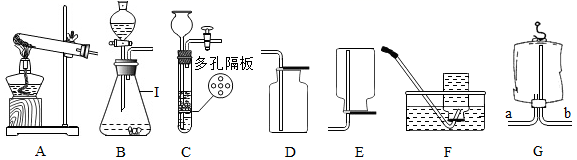
(1) 写出编号I仪器的名称。
-
(2) 实验室既可以制取CO2 , 又可以制取O2并能控制反应速率的发生装置为(填装置编),实验室制取CO2的化学方程式为。
-
(3) 某同学利用空塑料输液袋收集二氧化碳(如图G),验满时,把燃着的木条放在玻璃管(填“a”或“b”)端,如果熄灭则证明满了。
-
(4) 实验室如果用过氧化氢制取较纯净的氧气时,收集装置应选用,药品用(填序号)比较合适。
A6%的过氧化氢溶液
B20%的过氧化氢溶液
-
(5) 工业制氧气,利用的原料是空气。步骤:首先将空气净化,除去二氧化碳和水蒸气,然后在低温下加压使空气液化,利用氮气和氧气的不同分离出氧气。
-
(6) 常温下进行如图所示实验。A中固体逐渐减少,发生(填“物理”或“化学”)变化。C中有气泡,溶液颜色。

-
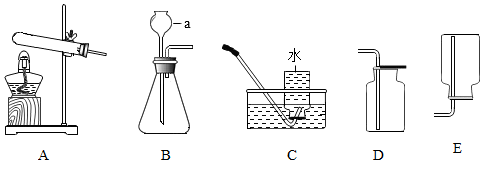
(1) 写出图中仪器a的名称:。
-
(2) 实验室制取氢气的原理为(写化学方程式):你选择的发生装置是(填序号)。
-
(3) 若实验室制取二氧化碳,你选择的收集装置是(填序号),验满的方法及现象是。



