第一节 化学实验基本方法 知识点题库
-
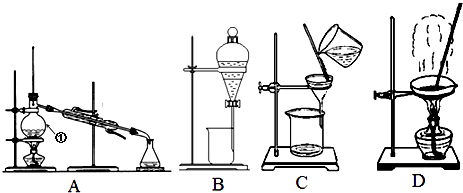
(1) 从氯化钠溶液中得到氯化钠固体,选择装置(填代表装置图的字母,下同);除去自来水中的Cl﹣等杂质,选择装置;从碘水中分离出I2 , 选择装置,该分离方法的名称为.
-
(2) 装置A中①的名称是,进冷却水的方向是.装置B在分液时为使液体顺利下滴,应进行的具体操作是.
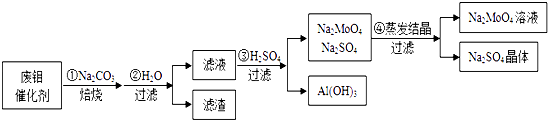
回答下列问题:
-
(1) 已知MoO3、Al2O3与SiO2相似,均能在高温下跟Na2CO3发生类似反应.试写出MoO3与Na2CO3反应的化学方程式:.
-
(2) 第②步操作所后的滤液中,溶质有Na2MoO4、和过量的Na2CO3;检验第②步操作所得滤渣中含有三价铁的方法是.
-
(3) 第③步操作H2SO4需要适量,通常是通过来调控H2SO4的用量;与Na2SO4相比,Na2MoO4的溶解度受温度的影响变化(填“较大”或“较小”).
-
(4) 利用铝热反应可回收金属钼.将所得钼酸钠溶液用酸处理得到沉淀,再加热可得MoO3 . 写出MoO3发生铝热反应的化学方程式:.
-
(5) 取废钼催化剂5.00g,加入5.30g Na2CO3(足量),经上述实验操作后,最终得到2.34g Al(OH)3和6.39g Na2SO4晶体,则废钼催化剂中钼元素的质量分数为.
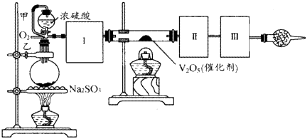
已知:SO3的熔点是16.8℃,沸点是44.8℃。
-
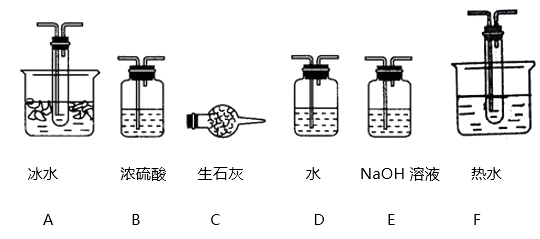
(1) 请从下图A~F装置中选择最适合装置并将其序号填入下面的空格中Ⅰ、Ⅱ、Ⅲ。
-
(2) 用1mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了12.8g,则实验中SO2的转化率为 % 。
-
(3) 为使SO2有较高的转化率,应均匀通入O2, , 且试验中在加热催化剂与滴加浓硫酸的顺序中,应采取的操作顺序是;尾端球形干燥管的作用是。
-
(4) 将SO2通过Na2O2粉末,完全反应后除生成O2外还生成一种白色粉末。证明该白色粉末既有Na2SO3又有Na2SO4所需的试剂是水、、、品红溶液。
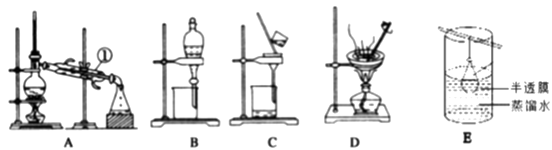
请根据装置A、B、C、D、E回答下列问题:
-
(1) 从硫酸钡和硫酸钠的混合液中分离出硫酸钡,可选择装置(填字母,下同);
-
(2) 从氯化钠(大量)和硝酸钾(少量)的混合溶液中分离出氯化钠(晶体)的方法是,洗涤,干燥。整个过程选择装置;
-
(3) 分离酒精和水,选择装置;
-
(4) 装置A中①的名称是,冷却水的流动方向是.
-
(5) 从淀粉和氯化钠的混合液中分离出氯化钠,选择装置 ;该实验称为(填方法)。
-
(6) 碘水中提取碘单质(固体)的方法是: 先用装置,可选用哪种萃取剂(填代号)然后用装置,分离出的碘单质(固体) 处于装置中(填名称)。
①酒精 ②苯 ③醋酸 ④汽油
-
(7) 在用装置B进行操作时,为使液体顺利滴下,应进行的具体操作是。分液后漏斗内剩余的液体从分液漏斗的(填“上口”或“下口”)倒入烧杯。
-
(8) Ⅱ.用如图装置测定水中氢、氧元素的质量比,其方法是分别测定Ⅱ、Ⅲ中通氢气前后玻璃管的质量差(设为m) 和U型管的质量差(设为n),
计算m(H):m(O)= (用含m、n的式子表示)
-
(9) 若实验测得m(H):m(O)>1:8。下列对导致这一结果的原因的分析中,一定错误的是________
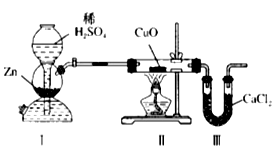 A . CuO没有全部被还原 B . Ⅲ装置后缺少干燥装置 C . Ⅱ装置中玻璃管内有水冷凝 D . I、Ⅱ装置之间缺少干燥装置 E . U 型管中CaCl2失效
A . CuO没有全部被还原 B . Ⅲ装置后缺少干燥装置 C . Ⅱ装置中玻璃管内有水冷凝 D . I、Ⅱ装置之间缺少干燥装置 E . U 型管中CaCl2失效
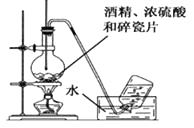 实验室制乙烯
B .
实验室制乙烯
B .  实验室制氨
C .
实验室制氨
C . 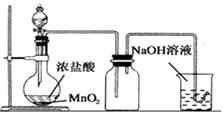 实验室制氯气
D .
实验室制氯气
D .  实验室制乙酸乙酯
实验室制乙酸乙酯
选项 | A | B | C | D |
物质的化学式 | NaOH | 汽油 | KClO3 | 乙醇 |
危险警告标签 |
|
|
|
|

-
(1) 步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是________(从下列仪器中选出所需仪器,用标号字母填写在横线上)。A . 烧杯 B . 坩埚 C . 表面皿 D . 泥三角 E . 酒精灯 F . 干燥器
-
(2) 步骤③的实验操作名称是 ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是。
-
(3) 步骤④反应的离子方程式是
-
(4) 步骤⑤中,某学生选择用苯来提取碘的理由是
-
(5) 请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法
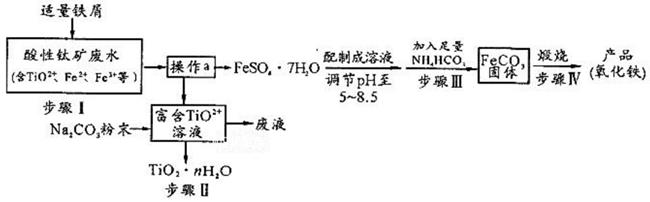
已知:TiO2+易水解,只能存在于强酸性溶液中。
-
(1) TiO2+钛的化合价为。
-
(2) 步骤Ⅰ中检验钛矿废水中加入铁屑是否足量的试剂是。
-
(3) 操作a是蒸发浓缩、冷却结晶、。
-
(4) 步骤Ⅲ中发生反应的化学方程式为;反应温度一般需控制在35℃以下,其目的是。
-
(5) 已知Ksp=[Fe(OH)2] = 8×10-16。步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5, c(Fe2+) = 1×10-6mol/L。试判断所得的FeCO3中(填“有”或“没有”)Fe(OH)2;步骤Ⅳ中,为了得到较为纯净的Fe2O3 , 除了适当的温度外,还需要采取的措施是。
-
(6) 向“富含TiO2+溶液”中加入Na2CO3粉末易得到固体TiO2• nH2O。请结合原理和化学用语解释其原因。
 B . 制取收集氨气
B . 制取收集氨气  C . 实验室制取溴苯
C . 实验室制取溴苯  D . 碳酸氢钠受热分解
D . 碳酸氢钠受热分解 
-
(1) 由FeCl3∙6H2O制得干燥FeCl2的过程如下:
i.向盛有FeCl3∙6H2O的容器中加入过量SOCl2(液体,易水解),加热,获得无水FeCl3。
ii.将无水FeCl3置于反应管中,通入一段时间的氢气后加热,生成FeCl2。
①FeCl3∙6H2O中加入SOCl2获得无水FeCl3的化学方程式为。(已知该反应为非氧化还原反应)
② ii中通入一段时间的氢气后再加热的目的是。
-
(2) 利用反应2FeCl3 + C6H5Cl
 2FeCl2+ C6H4Cl2 +HCl↑,制取无水FeCl2。在三颈烧瓶中加入无水氯化铁和过量的氯苯,控制反应温度在一定范围内加热3 h,冷却、分离、提纯得到粗产品,实验装置如图。(加热装置略去)
2FeCl2+ C6H4Cl2 +HCl↑,制取无水FeCl2。在三颈烧瓶中加入无水氯化铁和过量的氯苯,控制反应温度在一定范围内加热3 h,冷却、分离、提纯得到粗产品,实验装置如图。(加热装置略去) 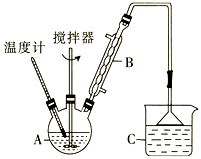
①仪器B的名称是 。反应前需向A中通入N2的目的是。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经、、干燥后,得到FeCl2粗产品。
③该装置存在的不足之处是。
-
(3) FeCl2的纯度测定。
①取a g样品配制成100 mL溶液;③用移液管移取所配溶液5.00mL,放入500 mL锥形瓶内并加水200mL;③往上述锥形瓶中加入硫酸锰溶液20.00 mL,用0.1 mol∙L-1酸性KMnO4标准溶液滴定,终点时消耗酸性KMnO4标准溶液V mL。滴定至终点的判断依据是。若所配溶液中ω(FeCl2)=kV(V为消耗的酸性高锰酸钾标准溶液的毫升数)g·L-1 , k=。
-
(1) I.已知:NaBr+H2SO4(浓)
 NaHSO4+ HBr CH3CH2OH+HBr
NaHSO4+ HBr CH3CH2OH+HBr  CH3CH2Br+H2O
CH3CH2Br+H2O 溴乙烷的沸点38.4℃,实验室制备溴乙烷(CH3CH2Br)的装置和步骤如下:
①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;
②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热,使其充分反应。
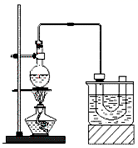
回答下列问题:
为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是。
-
(2) 浓硫酸具有强氧化性,能氧化还原性气体HBr为Br2 , 导致U形管中粗制的溴乙烷呈棕黄色。为了除去粗产品中的杂质Br2 , 可选择下列试剂中的:(填序号)
A.NaOH溶液 B.H2O
C.Na2SO3溶液 D.CCl4
分离时所需的主要玻璃仪器是(填仪器名称)。要进一步制得纯净的溴乙烷,可用水洗,然后加入无水CaCl2 , 再进行(填操作名称)。
-
(3) II.溴乙烷在不同溶剂中与NaOH可发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。
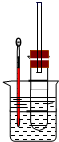
在试管中加入5 mL 1 mol/L NaOH水溶液和5 mL 溴乙烷,将试管如图固定后,加热。
①试管口安装一长导管的作用是。
②鉴定生成物中乙醇的结构,可用的波谱是和。
-
(4) 在试管中加入5 mL NaOH乙醇溶液和5 mL 溴乙烷,将试管如图固定后,加热。
①请写出该反应的化学方程式。
②为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在设计的实验方案中,需要检验的是,检验的装置如图所示,在气体通入酸性高锰酸钾溶液前加一个盛水的试管,其作用是。
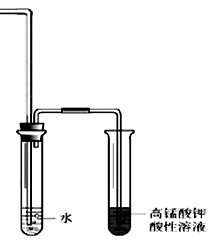
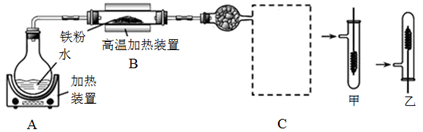
-
(1) 实验I:探究二氧化碳与过氧化钠反应是否有氧气生成,设计了如图的实验装置。B中盛有饱和碳酸氢钠溶液吸收挥发出的HCl,E为收集氧气装置。
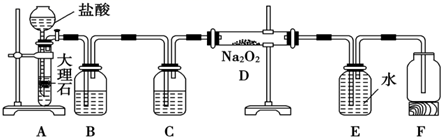
C中盛有,目的是。
-
(2) 指出装置E的不正确:。
-
(3) 取a g C3H6O2某物质在氧气中完全燃烧,将其产物跟足量的Na2O2固体完全反应,反应后固体的质量增加(填大于、等于或者小于)a g。
-
(4) 实验II:利用如图装置(省略夹持装置)模拟工业级NaN3的制备。
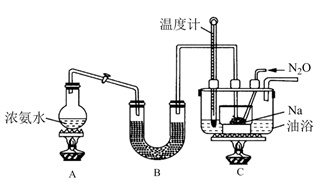
已知:2NaNH2+N2O
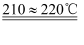 NaN3+NaOH+NH3
NaN3+NaOH+NH3装置B中盛放的药品为。
-
(5) 实验中使用油浴加热相比水浴加热的优点是。
-
(6) 氨气与熔融的钠反应生成NaNH2的化学方程式为。
-
(7) N2O可由NH4NO3(熔点为169.6℃)在240℃下分解制得,应选择的气体发生装置是。

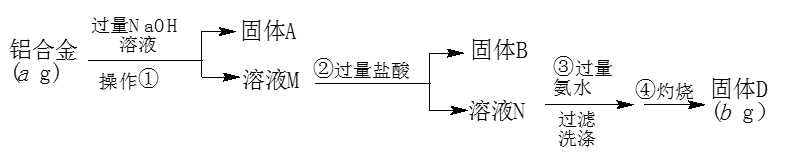
请回答下列问题:
-
(1) 固体A的成分是(填写化学式);操作①的名称是。
-
(2) 步骤③中生成沉淀的离子方程式为。
-
(3) 固体B的主要成分为(填写化学式)。
-
(4) 该样品中铝的质量分数是。(用含a、b代数式表示)
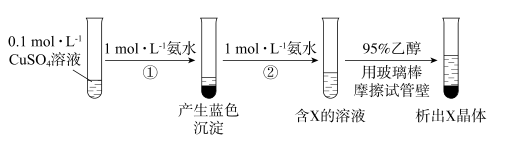
下列说法不正确的是( )
 B . 在①和②中,氨水参与反应的微粒相同
C . X中所含阴离子是SO
B . 在①和②中,氨水参与反应的微粒相同
C . X中所含阴离子是SO D . X的析出利用了其在乙醇中的溶解度小于在水中的溶解度
D . X的析出利用了其在乙醇中的溶解度小于在水中的溶解度







