第二节 化学计量在实验中的应用 知识点题库
标准状况下,2.24L己烷含有分子的数目为0.1NA (判断对错)
下列关于SO2的叙述中,正确的是( )
A . SO2的摩尔质量是64 g
B . 1mol SO2中所含分子数为6.02×1023
C . 1 mol SO2的质量是64 g/mol
D . 常温常压下,1 mol SO2的体积为22.4 L
448mL 某气体在标准状况下的质量为1.28g,该气体的摩尔质量约为( )
A . 46 g
B . 44
C . 64 g/mol
D . 32 g/mol
下列说法中,正确的是( )
A . 22.4 L N2含阿伏加德罗常数个氮分子
B . 在标准状况下,22.4 L水的质量约为18 g
C . 22 g二氧化碳与标准状况下11.2 L HCl含有相同的分子数
D . 标准状况下,相同体积的任何气体单质所含的原子数相同
下列溶液中物质的量浓度为1mol•L﹣1的是( )
A . 将40g NaOH溶解于1L水中
B . 10g NaOH溶解在水中配成250mL溶液
C . 从100mL 10mol•L﹣1的浓盐酸中取出10mL
D . 将22.4L氯化氢气体溶于水配成1L溶液
实验室欲用Na2CO3﹒10H2O晶体配制1mol/L的Na2CO3溶液100mL,下列说法正确的是( )
A . 要完成实验需称取10.6gNa2CO3﹒10H2O晶体
B . 本实验需用到的仪器是天平、药匙、玻璃棒、烧杯、100mL容量瓶
C . 配制时若容量瓶不干燥,含有少量蒸馏水会导致浓度偏低
D . 定容时俯视刻度线会导致浓度偏高
设NA表示阿伏加德罗常数的值。下列说法正确的是( )
A . NA的单位是摩尔
B . 12g12C中所含的碳原子数为NA
C . 标况下22.4L的任何气体所含原子数为NA个
D . 相同体积的O2(g)和NO2(g)分子数均为NA
已知某溶液的①体积 ②密度 ③溶质和溶剂的质量比 ④溶质的摩尔质量,要根据溶质的溶解度计算其饱和溶液的物质的量浓度时,上述条件必不可少的是( )
A . ①②③④
B . ①②③
C . ②④
D . ①④
下列溶液中Cl- 的物质的量浓度最大的是( )
A . 30mL0.2mol/LKCl溶液
B . 20mL0.1mol/LCaCl2溶液
C . 10mL0.1mol/LAlCl3溶液
D . 100mL0.25mol/LNaCl溶液
实验室中需要配制2 mol·L-1NaOH溶液950mL,配制时应选的容量瓶的规格和称取NaOH的质量分别是( )
A . 950 mL 76.0g
B . 500 mL 80.0 g
C . 1000mL 80.0g
D . 1000m L 76.0g
在t℃时,将a g NH3完全溶于水,得到V mL溶液,设该溶液的密度为ρ g·cm-3,质量分数为ω,其中含NH4+的物质的量为b mol。下列叙述中错误的是( )
A . 溶质的质量分数ω= 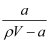 ×100%
B . 溶质的物质的量浓度c= 1000a/17Vmol·L-1
C . 溶液中c(OH-)= 1000b/Vmol·L-1+c(H+)
D . 上述溶液中再加入V mL水后,所得溶液中溶质的质量分数小于0.5ω
×100%
B . 溶质的物质的量浓度c= 1000a/17Vmol·L-1
C . 溶液中c(OH-)= 1000b/Vmol·L-1+c(H+)
D . 上述溶液中再加入V mL水后,所得溶液中溶质的质量分数小于0.5ω
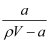 ×100%
B . 溶质的物质的量浓度c= 1000a/17Vmol·L-1
C . 溶液中c(OH-)= 1000b/Vmol·L-1+c(H+)
D . 上述溶液中再加入V mL水后,所得溶液中溶质的质量分数小于0.5ω
×100%
B . 溶质的物质的量浓度c= 1000a/17Vmol·L-1
C . 溶液中c(OH-)= 1000b/Vmol·L-1+c(H+)
D . 上述溶液中再加入V mL水后,所得溶液中溶质的质量分数小于0.5ω
某学生只有下列仪器和用具:烧杯、试管、硬质玻璃管、圆底烧瓶、量筒、铁架台(带铁夹)、酒精灯、集气瓶、玻璃片、水槽、导气管、橡皮塞、橡皮管、100mL容量瓶、玻璃棒、药匙、火柴。从缺少仪器或用品的角度看,该学生能进行的实验操作是( )
A . 制蒸馏水
B . 粗盐提纯
C . 用氢气还原氧化铜
D . 用氯化钠晶体配制100mL0.1mol·L—1的氯化钠溶液。
下列叙述不正确的是( )
A . 丁达尔效应可以区别溶液和胶体
B . 合金与各组分金属相比一般具有更大的硬度
C . 向醋酸溶液中加入Na2CO3固体,溶液的导电性明显增强
D . 配制一定物质的量浓度溶液,定容时仰视容量瓶刻度线,使所得溶液浓度偏大
如图表示1g O2与1g X气体在相同容积的密闭容器中压强(P)与温度(T)的关系,则X气体可能是( )
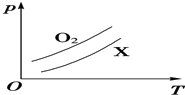
A . C2H4
B . CO2
C . CH4
D . NO
下列说法正确的是( )
A . 氧的摩尔质量是32 g/mol
B . CO的摩尔质量是60 g
C . CO2的相对分子质量是44 g
D . 硫酸的摩尔质量是98 g/mol
某种气体的摩尔质量为M g·mol-1 , 将标况下的该气体V L溶解在1000 g水中,该气体不与水反应,所得溶液密度为ρ g·cm-3 , 则所得溶液中溶质的物质的量浓度为 ( )mol·L-1
A . V/22.4
B . V ρ/(MV+22400)
C . V ρ/22400
D . 1000V ρ/(MV+22400)
氮化铬(CrN)是一种耐磨性良好的新型材料,难溶于水。探究小组同学用下图所示装置(夹持装置略去)在实验室中制取氮化铬并测定所得氮化铬的纯度。
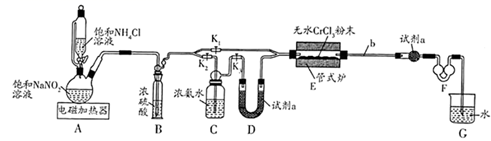
已知:实验室中常用  溶液与
溶液与  溶液反应制取
溶液反应制取  ;
;  能溶于水和乙醇。
能溶于水和乙醇。
回答下列问题:
-
(1) 实验准备就绪后,应先加热(填装置代号)装置,此时
 所处的状态是。
所处的状态是。
-
(2) 实验中
 的作用是。
的作用是。
-
(3) 改变
 的状态,加热E装置。试剂a的名称是,写出装置E中发生反应的化学方程式。
的状态,加热E装置。试剂a的名称是,写出装置E中发生反应的化学方程式。
-
(4) 实验过程中需间歇性微热b处导管的目的是。
-
(5) 向
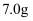 所得
所得  中加入足量
中加入足量  溶液,然后通入水蒸气将
溶液,然后通入水蒸气将  全部蒸出,将
全部蒸出,将  用
用 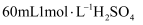 溶液完全吸收,剩余的
溶液完全吸收,剩余的  用
用  溶液恰好中和,则所得产品中
溶液恰好中和,则所得产品中  的质量分数为。
的质量分数为。
实验室需要 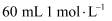 的硫酸溶液,现用市售98%浓硫酸(密度为
的硫酸溶液,现用市售98%浓硫酸(密度为  )配制,用量筒取用的浓硫酸体积最适宜的是( )
)配制,用量筒取用的浓硫酸体积最适宜的是( )
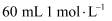 的硫酸溶液,现用市售98%浓硫酸(密度为
的硫酸溶液,现用市售98%浓硫酸(密度为  )配制,用量筒取用的浓硫酸体积最适宜的是( )
)配制,用量筒取用的浓硫酸体积最适宜的是( )
A . 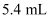 B .
B .  C .
C . 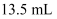 D .
D . 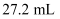
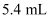 B .
B .  C .
C . 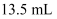 D .
D . 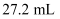
“消洗灵”是一种广谱、高效、低毒的消毒洗涤剂,消毒原理与“84消毒液”相似,但更稳定、易保存。某“消洗灵”产品化学组成可以表示为 , 实验室制备装置和过程如下:
, 实验室制备装置和过程如下:
 , 实验室制备装置和过程如下:
, 实验室制备装置和过程如下:
回答下列问题:
-
(1) I打开A中分液漏斗活塞,制备
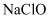 碱性溶液。
碱性溶液。X试剂为。
-
(2) C中盛装
 溶液的仪器名称是。采用多孔球泡的目的是。
溶液的仪器名称是。采用多孔球泡的目的是。
-
(3) 若D中
 溶液恰好耗尽,则所得溶液中各离子浓度由大到小的关系为。
溶液恰好耗尽,则所得溶液中各离子浓度由大到小的关系为。
-
(4) Ⅱ.关闭A中分液漏斗活塞,打开C中分液漏斗活塞,一段时间后C中溶液经蒸发浓缩、冷却结晶、过滤得到粗产品。
产品中氯元素的化合价为。
-
(5) 已知
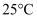 时,
时, 溶液的
溶液的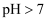 , 原因是(用离子方程式表示)。
, 原因是(用离子方程式表示)。
-
(6) Ⅲ.产品纯度测定(
 的摩尔质量为
的摩尔质量为 )。
)。①取
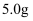 待测试样溶于蒸馏水配成
待测试样溶于蒸馏水配成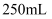 溶液;
溶液;②取
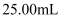 待测液于锥形瓶中,加入
待测液于锥形瓶中,加入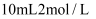 稀硫酸、
稀硫酸、 碘化钾溶液(过量),此时溶液出现棕色;
碘化钾溶液(过量),此时溶液出现棕色;③滴入3滴
 淀粉溶液,用
淀粉溶液,用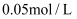 硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗
硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗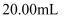 。已知:
。已知:
产品的纯度为。
化学仪器的规范使用是实验成功的关键。下列对装置或仪器的使用或操作规范的是( )

A . 图A是向容量瓶中转移溶液
B . 图B是振荡分液漏斗中混合液
C . 图C是称量5.1g固体
D . 图D是煅烧石灰石
最近更新



