课题一 实验化学起步 知识点题库
①给试管中的药品加热,必须先 ,后集中加热.
②点燃可燃性气体(如H2、CO等)时,都要先 ,后点燃.
(2)实验室要配制250ml,1mol/L的NaCl溶液,请按使用的先后顺序写出所需仪器名称
掌握仪器的名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.

-
(1) 写出下列仪器的名称:
① ;② ;④
-
(2) 仪器①~④中,使用时必须检查是否漏水的有 .(填序号)
-
(3) 若利用装置Ⅰ分离四氯化碳和酒精的混合物,还缺少的仪器有 ,将仪器补充完整后进行的实验操作的名称为; .现需配制250mL 0.2mol/L NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,图中两处错误是
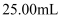 待测液时,若移液管内残留少量液体,必须用洗耳球将其吹出,否则使测量结果偏低
B . 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
C . 滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面变化
D . 吸滤完毕停止吸滤时,应先拆下连接抽气泵和吸滤瓶的橡皮管,再关闭水龙头
待测液时,若移液管内残留少量液体,必须用洗耳球将其吹出,否则使测量结果偏低
B . 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
C . 滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面变化
D . 吸滤完毕停止吸滤时,应先拆下连接抽气泵和吸滤瓶的橡皮管,再关闭水龙头
[制备产品]
将氯气和空气(不参与反应)按体积比1:3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O(不含Cl2)制备次氯酸溶液。

-
(1) 各装置的连接顺序为→→→C→;(填字母)
-
(2) 装置B中多孔球泡和搅拌棒的作用是;装置C的作用是;
-
(3) 制备Cl2O的化学方程式为;
-
(4) 此方法相对于用氯气直接溶于水制备次氯酸溶液的主要优点是;
-
(5) 反应过程中,装置B需放在中:(选填“冷水”或“热水”)
-
(6) [测定浓度]
已知次氯酸可被FeSO4等物质还原。用下列实验方案测定装置E所得溶液中次氯酸的物质的量浓度:量取10 mL上述次氯酸溶液,并稀释至100 mL,再从中取出10.00 mL于锥形瓶中,并加入10.00 mL 0.8 mol/L的FeSO4溶液,充分反应后,用0.05000 mol/L的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液24.00 mL,则原次氯酸的物质的量浓度为。(保留四位有效数字)

 NaCl+N2↑+2H2O
B . 加热片刻后需要将酒精灯移开,说明该反应是放热反应
C . 装置II的作用是冷凝水蒸气
D . 在装置III末端收集纯净干燥的N2只能用向下排空气法
NaCl+N2↑+2H2O
B . 加热片刻后需要将酒精灯移开,说明该反应是放热反应
C . 装置II的作用是冷凝水蒸气
D . 在装置III末端收集纯净干燥的N2只能用向下排空气法
已知:①SiHCl3的沸点为33.0℃,密度为1.34g·cm-3;易溶于有机溶剂;能与H2O剧烈反应;在空气中易被氧化;
②CaCl2+xCH3CH2OH→CaCl2·xCH3CH2OH;
③银氨溶液中存在:[Ag(NH3)2]++2H2O  Ag++2NH3·H2O。
Ag++2NH3·H2O。
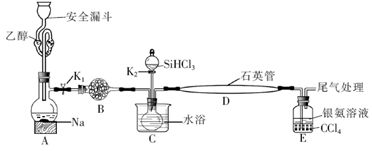
回答下列问题:
-
(1) 装置B中试剂宜选择(填字母,单选)。
a.碱石灰 b.无水氯化钙 c.五氧化二磷 d.硅胶
-
(2) 实验操作步骤有:
①加热装置D至1357K;
②关闭K1;
③加热装置C,打开K2 , 滴加VmLSiHCl3;
④关闭K2;
⑤打开K1 , 向安全漏斗中加入足量乙醇,装置A中反应一段时间。
正确的操作顺序为(填序号)。
-
(3) E中CCl4的作用是防倒吸和。
-
(4) 石英管中发生反应的化学方程式为。
-
(5) 本实验制得高纯硅a g,则SiHCl3的利用率为(只列计算式)。实验结束后,有同学认为根据高纯硅与消耗钠或乙醇的量也可以计算SiHCl3的利用率,这种观点(填“是”或“否”)正确。
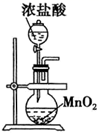
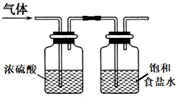
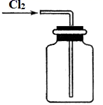
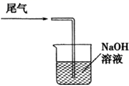
| A | B | C | D |
| | | | |
| 制备Cl2 | 净化Cl2 | 收集Cl2 | 尾气处理 |
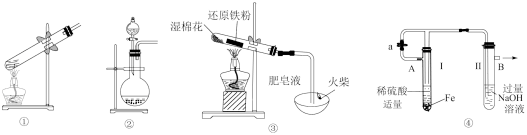


按上述流程进行操作,下列仪器中不需要用到的有( )
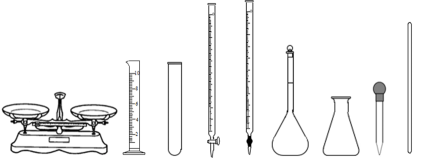
①烧杯②100mL量筒③托盘天平(带砝码)④玻璃棒⑤胶头滴管
-
(1) 配制时,还缺少的玻璃仪器是。应称量的NaOH的质量是g。
-
(2) 使用容量瓶前必须进行的一步操作是。
-
(3) 下列图片表示配制溶液的步骤,请写出正确的操作顺序是:(用数字表示,每个数字只能用一次)

-
(4) 若其它操作均正确,以下操作会引起所配溶液浓度偏大的是____(填写字母)。
A.在滤纸上称量NaOH
A . 定容时俯视刻度线 B . 转移前,容量瓶中有少量蒸馏水 C . NaOH溶解后,未冷却就立即转移到容量瓶 D . 定容摇匀后,发现液面低于刻度线,再加水至刻度线