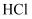课题一 实验化学起步 知识点题库
下列仪器中,常用于物质分离的是( )

A . ①③
B . ②③
C . ②④
D . ①②
下列分离和提纯的实验操作中,正确的是( )
A .  蒸发
B .
蒸发
B .  过滤
C .
过滤
C .  蒸馏
D .
蒸馏
D .  分液
分液
 蒸发
B .
蒸发
B .  过滤
C .
过滤
C .  蒸馏
D .
蒸馏
D .  分液
分液
下列图示实验均不正确,请给以纠正.

A;B;C;D;E.

-
(1) 写出图中仪器甲、乙的名称:甲,乙。
-
(2) 用充满水的装置C收集氧气,则氧气需从(填“a”或“b“)端通入,实验室用高锰酸钾制取氧气,发生装置可选择图中的(填标号),写出该反应的化学方程式 。
-
(3) 实验室制取二氧化碳的化学方程式是,用装置C收集二氧化碳,验满时,燃着木条应放在(填“a”或“b“)端,检验二氧化碳的试剂是。
下图仪器中名称为圆底烧瓶的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B . 
下列解释不科学的是( )
A . 高压氧舱可治疗煤气中毒,原因是和血红蛋白结合的 CO 跟氧气反应生成无毒的 CO2
B . 在溶洞中当溶有 Ca(HCO3)2 水溶液,析出固体(在洞顶或洞底),日久天长便形成了钟乳石
C . 氮是植物体内蛋白质、核酸和叶绿素的组成元素
D . “通风橱”利用排风扇将橱内废气直接排放到室外,它是一种不完善的防污措施
当我们外出旅游的时候,在车站会看到这样的告示:严禁携带易燃、易爆、剧毒品、易腐蚀品等上车。现有:①汽油 ②酒精 ③鞭炮 ④浓硫酸 其中旅客不可带上车的是( )
A . 只有①③
B . 只有②④
C . 只有①②③
D . 全部
下列说法错误的是( )
A . 蒸馏实验时,若冷凝管内壁上出现馏出物固体,此时可以减小通入冷却水的流速
B . 浓硝酸应保存在带磨口玻璃塞的棕色细口试剂瓶中
C . 滴瓶中的滴管在加完药品后应将滴管洗净后再放回原瓶
D . 摩尔盐制备实验中,向FeSO4溶液中加入少量稀硫酸抑制Fe2+的水解
下列实验操作会使实验最终结果偏高的是( )
A . 用湿润的pH 试纸测定NaOH的pH
B . 配制100 mL 1.00 mol·L -1 NaCl溶液,定容时俯视刻度线
C . 用0.0001 mol·L -1盐酸滴定20.00 mL NaOH溶液,起始读数时仰视
D . 测定中和热的数值时,将0.5 mol·L -1NaOH溶液倒入盐酸后,立即读数
贴有图所示标志的槽罐车内可能装有:( )

A . 液氯
B . 汽油
C . 浓硫酸
D . 四氯化碳
用98%的浓硫酸(密度为1.84 g/cm3 )配制100 mL 1mol/L的稀硫酸。现给出下列仪器(配制过程中可能用到):①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒,按使用仪器的先后顺序排列正确的是( )
A . ④③⑦⑤⑥;
B . ②⑤⑦⑥;
C . ①③⑤⑥⑦;
D . ②⑥③⑦⑤⑥
-
(1) KClO3+ 6HCl (浓)=3Cl2 ↑+KCl +3H2O其中氧化剂为;还原产物为;氧化产物与还原产物的质量比为;
-
(2) Fe(OH)3胶体的制备:取一小烧杯,加入25 mL蒸馏水,加热至沸腾,然后向沸水中逐滴加入5~6滴,继续煮沸至体系呈,停止加热,即制得Fe(OH)3胶体。
如图是盛放液溴的试剂瓶剖面图,仔细观察分成了明显的气相、溴溶液相和液溴相三相,下列说法错误的是( )

A . 气相呈现红棕色,因为其中含有Br2的蒸汽
B . 溴溶液相中显酸性,主要因为HBr电离出了H+
C . 液溴保存时加水形成水封的目的是减少Br2的挥发
D . 液溴保存时不可敞口放置,应保存在细口瓶中并塞上橡胶塞
实验室中下列做法错误的是( )
A . 贮存液溴时加水液封
B . 用无水氯化钙干燥氨气
C . 用坩埚灼烧固体
D . 用二硫化碳洗涤内壁附有单质硫的试管
下列装置不能达到相应实验目的的是( )

A . 利用甲装置除去  中混有的
中混有的  B . 利用乙装置测定
B . 利用乙装置测定  的生成体积
C . 利用丙装置分离
的生成体积
C . 利用丙装置分离  和
和 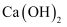 固体
D . 利用丁装置做喷泉实验
固体
D . 利用丁装置做喷泉实验
 中混有的
中混有的  B . 利用乙装置测定
B . 利用乙装置测定  的生成体积
C . 利用丙装置分离
的生成体积
C . 利用丙装置分离  和
和 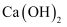 固体
D . 利用丁装置做喷泉实验
固体
D . 利用丁装置做喷泉实验
某兴趣小组对氢氧化钠溶液和稀盐酸混合后的有关问题进行了如下探究:
-
(1) 配制溶液:甲同学配制100mL1.5 mol·L-1氢氧化钠溶液,乙同学取20mL36.5%(密度为1.20g·mL-1)的盐酸稀释到200mL。甲为了证明氢氧化钠溶液与稀盐酸能发生化学反应,设计并完成了如图所示的实验。

X溶液滴入的量一般为,使用酸式滴定管前要检查活塞是否漏水的操作方法是。
-
(2) 乙设计完成了另一个实验,以证明氢氧化钠溶液与盐酸能够发生反应。他在盛有20mL稀盐酸的锥形瓶里,用碱式滴定管滴入氢氧化钠溶液,不断振荡溶液,同时用pH计测定溶液的pH,直到盐酸过量。则在滴定过程中,滴定终点附近的操作是。
-
(3) 你认为甲、乙两位同学的实验中,(填“甲、乙、甲和乙”)的实验能充分证明氢氧化钠与盐酸发生了反应。
-
(4) 丙同学为了测定上述36.5%盐酸的物质的量浓度,进行了如下实验:在锥形瓶中加入已稀释的盐酸并滴入甲基橙,用碱式滴定管滴入甲配制的氢氧化钠溶液,测定的结果如表:
测定次数
盐酸的体积/mL
氢氧化钠溶液的体积
滴定前刻度/mL
滴定后刻度/mL
1
25.00
1.02
21.03
2
25.00
2.00
21.99
3
25.00
0.20
20.20
达到滴定终点的判断。据此通过计算可知实验测定的盐酸浓度与标签说明的浓度相比(填“偏高、偏低、相等”)。
人类离不开化学,下列叙述错误的是( )
A . 金属钠着火时,可用细沙覆盖灭火,也可用水去灭火
B . 纳米铁粉可以去除被污染水体中的Pb2+、Cu2+、Hg2+ , 利用了其还原性
C . 钠钾合金(液态)可用于原子反应堆的导热剂
D . 碳酸氢钠是烘制糕点所用发酵剂的主要成分之一
下列说法不正确的是( )
A . 实验室少量的钠保存在煤油中,工业上大量的钠采用蜡封的方法保存
B . 滴定管用水洗涤干净之后,需要用烘干的方法除去内容附着的水
C . 除去工业酒精中的水,可采用加入生石灰蒸馏的方法
D . 明矾、胆矾、石膏等都可以作为工业制硫酸的原料
如图a、b、c表示相应仪器中加入的试剂,可用图中装置制取、净化、收集的气体是( )
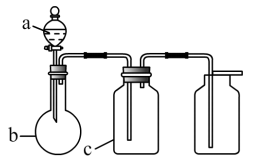
编号 | 气体 | a | b | c |
A | NH3 | 浓氨水 | 固体氢氧化钠 | 浓硫酸 |
B | CO2 | 盐酸 | 碳酸钙 | 饱和NaHCO3溶液 |
C | Cl2 | 浓盐酸 | 二氧化锰 | 浓硫酸 |
D | NO2 | 浓硝酸 | 铜屑 | NaOH溶液 |
A . A
B . B
C . C
D . D
下列装置能达到实验目的的是 ( )
A | B | C | D |
|
|
|
|
实验室制氨气 | 蒸馏时的接收装置 | 除去 | 吸收多余的 |
A . A
B . B
C . C
D . D
最近更新


 中少量
中少量