课题一 实验化学起步 知识点题库
甲柜 | 乙柜 | 丙柜 | 丁柜 | 戊柜 |
盐酸、硫酸 | 烧碱、氢氧化钡 | 硫、红磷 | 铜、锌 | 碳酸钠、硝酸钾 |
现在新购进硝酸、苛性钾、碘和硝酸银溶液,下列对其保存方法不正确的是( )
(1)下列仪器中:①漏斗 ②容量瓶 ③蒸馏烧瓶 ④天平 ⑤分液漏斗
⑥量筒 ⑦燃烧匙.常用于物质分离的是 ,其中根据物质沸点不同来分离物质的仪器是 .
(2)实验室有贮存以下物质的方法:
A.氯水不宜长期存放,短期保存则需避光;
B.浓硝酸用棕色瓶盛放,贮存在阴凉处
C.通常向盛有溴单质的试剂瓶中加入适量的水
D.金属钠常保存在煤油中
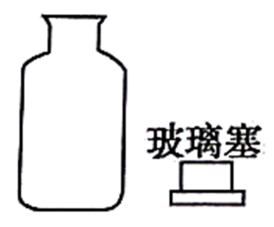
E.NaOH溶液通常用带玻璃塞的磨口试剂瓶保存;
其中正确的是 .
①残留在试管内壁上的碘,用酒精洗涤
②残留有苯酚的试剂瓶,用酒精洗涤
③做银镜反应后试管壁上的银镜,用稀氨水洗涤
④沾附在试管内壁上的油脂,用热碱液洗涤.
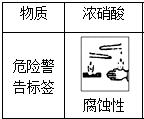 B .
B . 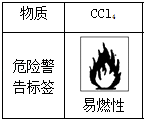 C .
C .  D .
D . 
-
(1) 写出图中序号①~④仪器的名称:

① ;②;③;④;
-
(2) 仪器①~④中,使用时必须检查是否漏水的有.(填仪器序号)
-
(3) 若向II装置中加入碘水和少量CCl4 , 振荡后静置,会观察到什么现象?
;静置后,再将液体分离的操作是
-
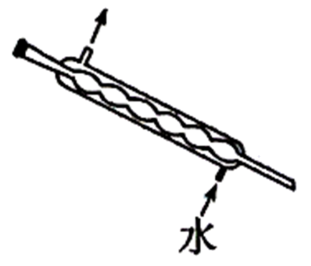
(4) 装置I 中 冷凝水由(填a或b)口通入,温度计水银球的位置是
-
(5) 分离以下混合物应该选用什么方法,将答案填写在横线上.
食盐和大理石粉末: 汽油和酒精: 汽油和水:
-
(6) 除掉硝酸钠中少量的食盐,某学生用AgNO3溶液,确认Cl﹣已沉淀完全的实验方法是.

请回答问题:
-
(1) 按气流方向,各仪器接口从左到右的连接顺序为:
i→→→g→h→→→j → k→ →。(填字母编号)
-
(2) 证明Fe2O3己被还原的现象是。
-
(3) 研究小组对黑色粉末的成分提出下列猜想:
【猜想一】黑色粉末的成分可能是Fe。
【猜想二】黑色粉末的成分可能是FeO。
【猜想三】黑色粉末的成分可能是。
设计并完成实验如下:
步骤
操作
现象
Ⅰ
加入稀盐酸
溶解,无气泡
Ⅱ
取步骤1中溶液,滴加K3[Fe(CN)6]溶液
蓝色沉淀
Ⅲ
变红
①根据实验现象,则猜想成立。
②研究小组又向步骤3的溶液中滴加新制氯水,发现溶液红色褪去。可能的原因及验证方法为。
-
(4) 上述装置还有不妥之处,改进措施为。
 B .
B .  C .
C .  D .
D . 


实验步骤如下:
I.SO2含量的测定
烧瓶A中加中药粉10g,加蒸馏水300mL;锥形瓶中加蒸馏水125nL和淀粉试液1mL作为吸收液;打开冷凝水,通氮气,滴入盐酸l0mL;加热烧瓶A并保持微沸约3min后,用0.01000mol/L碘标准溶液一边吸收一边滴定,至终点时消耗碘标准溶液V1mL;
Ⅱ.空白实验
只加300mL蒸馏水,重复上述操作,需碘标准溶液体积为V0mL。
-
(1) 仪器C的名称。仪器B的入水口为(填“a”或“b”)
-
(2) 滴入盐酸前先通氮气一段时间作用是,测定过程中氮气的流速过快会导致测量结果。(填“偏大”“偏小”或“不变”)
-
(3) ①滴定过程中使用的滴定管为。
A.酸式无色滴定管
B.酸式棕色滴定管
C.碱式无色滴定管
D.碱式棕色滴定管
②滴定时锥形瓶中反应的离子方程式为,滴定终点的现象是。
-
(4) 空白实验的目的是。
-
(5) 该中药中含SO2含量为mg/kg。

回答下列问题:
-
(1) 装置A中,仪器a的名称叫,该仪器中盛放的试剂为,写出A装置发生反应的离子方程式:。
-
(2) 装置B的作用是。
-
(3) 当有少量Cl2通过后,观察到装置C中溶液变成色。
-
(4) 当Cl2持续通过时,装置D中干燥的有色布条能否褪色?为什么?,。
-
(5) 若要证明Cl2无漂白性,则必须在装置D之前加一个。
-
(6) 装置E的作用是,该反应的离子方程式为。
-
(7) 家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下。
注意事项:
1.本品对棉织品有漂白脱臼作用,对金属制品有腐蚀作用。
2.密封保存,请勿与洁厕灵同时使用。
3.保质期为一年。
消毒液与洁厕灵不能同时使用,原因是(用离子方程式表示)。

已知: BCl3 的熔点为- 107.3℃ 沸点为 12.5 ℃ , 遇水水解生成 H3BO3和HCl。
下列说法错误的是( )

其中:常温常压下ⅹ是一种有特殊气味、易挥发的无色液体,由三种常见的短周期元素组成。
请回答:
-
(1) 组成X的3种元素是(填元素符号),沉淀C的化学式是。
-
(2) X反应生成A和B的反应方程式是。
-
(3) B可与乙醇以物质的量之比1∶2发生取代反应生成一种酯,写出反应方程式。
-
(4) 实验室保存少量物质X的仪器是_______。A . 无色广口瓶 B . 棕色广口瓶 C . 无色细口瓶 D . 棕色细口瓶
-
(5) 请设计一种不同于上述流程的实验方案,检验中相对原子质量最大的元素。
 B . 分离硫酸亚铁溶液和不溶性杂质
B . 分离硫酸亚铁溶液和不溶性杂质  C . 配制1
C . 配制1 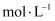 的稀硫酸
的稀硫酸  D . 制备少量氧气
D . 制备少量氧气 

请回答下列问题:
-
(1) 实验时灼烧海带应在(填仪器名称)内进行。
-
(2) 步骤④中反应的离子方程式是。
-
(3) 步骤⑤中选用的溶剂X可以是(填试剂名称)。
-
(4) 上述流程中的实验操作包括下列选项中____(按操作顺序选填代号)。A . 过滤 B . 蒸发 C . 蒸馏 D . 分液
-
(5) 请设计一个简单的实验方案,检验步骤⑤提取碘后的溶液中是否还含有单质碘。
A | B | C | D |
盛装 | 钠在空气中加热 | 准确量取一定体积 | 蒸馏用冷凝管 |
|
|
|
|

-
(1) I.硝酸氧化法
第一步:向三颈烧瓶中依次加入质量分数为40%的乙二醛78.5mL,质量分数为30%的盐酸17.2mL,蒸馏水30mL;
第二步:搅拌并通入氧气5分钟,升温至50℃,加入亚硝酸钠固体2.5g,搅拌下升温至60℃,缓慢分批滴加质量分数为40%的硝酸溶液47mL(23分钟加完),恒温下反应2小时,然后升温至75℃,搅拌30分钟反应结束;
第三步:降温结晶、过滤、洗涤,得到产品。
装置a、b的名称分别为。
-
(2) 在催化剂亚硝酸钠的作用下,可用浓硝酸氧化乙二醛(OHC-CHO)制取乙醛酸,该反应的化学方程式为。
-
(3) 第二步通入氧气的目的是(用化学方程式并结合简单文字说明);硝酸需要缓慢分批加入的原因是。
-
(4) 第三步中洗涤产品所用的最佳试剂为。
-
(5) II.过氧化氢氧化法
乙二醛硝酸氧化法具有原料易得及反应条件温和等优点,但也存在明显不足。因此用过氧化氢代替硝酸制取乙醛酸的理由是。
-
(6) III.电解法
乙醛酸溶液可以由草酸(HOOC-COOH)水溶液经电解获得,请写出电解过程中阴极的电极反应式。
84消毒液 【有效成分】NaClO 【规格】1 000 mL 【质量分数】25% 【密度】1.192 g·cm-3 【使用方法】稀释100倍(体积比)后使用 |
-
(1) 工业上常用氯气与烧碱溶液制取84消毒液,写出该反应的离子方程式。
-
(2) 某同学量取100 mL此84消毒液,按说明要求稀释后用于消毒,则稀释后的溶液中c(NaClO)=mol·L-1。
-
(3) 某化学实验小组欲用NaClO固体配制含25%NaClO的消毒液480mL。
①请计算配制此溶液需称取NaClO固体的质量为g 。
②如图所示的仪器中配制溶液需要使用的是(填字母),还缺少的玻璃仪器是。

-
(4) 若实验遇下列情况,导致所配溶液的物质的量浓度偏高是____(填字母)。A . 定容时俯视刻度线 B . 转移前,容量瓶内有蒸馏水 C . 未冷却至室温就转移定容 D . 定容时水加多了用胶头滴管吸出
 溶液
溶液 标准溶液
标准溶液