实验3-4 酸碱滴定曲线的测绘 知识点题库
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为:1×10﹣3mol•L﹣1 , 则该溶液中溶质的pC=3.下列表达正确的是( )
A . 某温度下任何电解质的水溶液中,pC(H+)+pC(OH﹣)=14
B . 0.01mol/L的CaCl2溶液中逐渐滴加纯碱溶液,滴加过程中pC(Ca2+)逐渐减小
C . 用0.01mol/L的盐酸滴定某浓度的NaOH溶液,滴定过程中pC(H+)逐渐增大
D . 某温度下,AB难溶性离子化合物的Ksp=1.0×10﹣10 , 其饱和溶液中pC(A+)+pC(B﹣)=10
pH的大小,可用来表示溶液的 的强弱.溶液的 性越强,pH越大;溶液的 性越强,pH越小.溶液中H+或OH﹣离子浓度 1mol/L时,一般不用pH表示溶液的酸碱性,而直接用 表示.测定溶液pH通常可用pH试纸,它是用 混合溶液浸制而成.若精确测定溶液pH,则应用 .
常温下,对下列四种溶液的叙述正确的是( )
① | ② | ③ | ④ | |
pH | 10 | 10 | 4 | 4 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
A . 四种溶液分别加水稀释10倍,pH变化最大的是①和④
B . ②、④两溶液相比,两者的kw相同
C . ①、②、③中分别加入少量的醋酸铵固体后,三种溶液的pH均减小
D . ①、④两溶液按一定体积比混合,所得溶液中离子浓度顺序一定为:c(NH4+)>c(Cl﹣)>c(H+)>c(OH﹣)
下列实验,说法正确的是( )
A . 测30%H2O2溶液的pH时,可将双氧水滴在pH试纸上,变色后和标准比色卡比照
B . 用托盘天平称取1.06 g无水碳酸钠,小心转移至250mL容量瓶中,加入蒸馏水至刻度线,配制得到0.04 mol•L﹣1 Na2CO3溶液
C . 用苯萃取溴水中的溴,得到的溴的苯溶液从分液漏斗的上口倒出
D . 在滴有酚酞的Na2CO3溶液中,加入CaCl2溶液,溶液褪色,说明CaCl2溶液有酸性
已知在100℃,水的离子积Kw=1×10﹣12 , 本题涉及的溶液温度均为100℃.下列说法中正确的是( )
A . 0.005 mol/L的H2SO4溶液,pH=2
B . 0.001 mol/L的NaOH溶液,pH=11
C . 0.005 mol/L的H2SO4溶液与0.01 mol/L的NaOH溶液等体积混合,混合溶液的pH为6,溶液显酸性
D . 完全中和pH=3的H2SO4溶液50 mL,需要pH=9的NaOH溶液100 mL
下列各物质的溶液物质的量浓度均为0.1mol/L:①HCl;②NaOH;③Na2CO3;④NH4Cl;⑤CH3COONa;⑥Ba(OH)2;⑦KCl.它们pH按由小到大的排列顺序为( )
A . ⑥②③⑤⑦④①
B . ①④⑦③⑤②⑥
C . ①④⑤③⑦②⑥
D . ①④⑦⑤③②⑥
下列实验操作合理的是( )
①将干燥的pH试纸浸到某溶液中,过一会取出与标准比色卡比较,测得该溶液的pH;
②用铂丝蘸取某溶液在酒精灯外焰上灼烧,直接观察火焰颜色来确认是否含有钾元素;
③通过丁达尔现象来区别硫酸铜溶液和氢氧化铁胶体;
④配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸;
⑤检验红砖中的氧化铁成分时,向红砖粉末中加入盐酸,放置至充分沉淀后,取上层清液于试管中,滴加KSCN溶液即可.
A . ③⑥
B . ②③
C . ③④⑥
D . ①③④
关于溶液的酸碱性说法正确的是()
A . c(H+)很小的溶液一定呈碱性
B . pH=7的溶液一定呈中性
C . c(OH-)= C(H+)的溶液一定呈中性
D . 不能使酚酞试液变红的溶液一定呈酸性
已知某温度下,四种一元弱酸的电离平衡常数为:Ka(HCN)= 6.2×10-10mol/L、Ka(HF)= 6.8×10-4mol/L、Ka(CH3COOH)= 1.8×10-5mol/L、Ka(HNO2)= 6.4×10-6mol/L。物质的量浓度都为0.1 mol/L的下列溶液中,pH最小的是( )
A . HCN
B . CH3COOH
C . HF
D . HNO2
相同物质的量浓度的下列物质的稀溶液中,pH最小的是( )
A . 乙醇
B . 乙酸
C . 碳酸钠
D . 碳酸
用下列装置进行实验,装置正确且能达到相应实验目的是( )
A . 析氢腐蚀  B . 证明二氧化氮生成四氧化二氮为放热反应
B . 证明二氧化氮生成四氧化二氮为放热反应  C . 测定溶液pH
C . 测定溶液pH  D . 测定盐酸浓度
D . 测定盐酸浓度 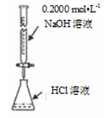
 B . 证明二氧化氮生成四氧化二氮为放热反应
B . 证明二氧化氮生成四氧化二氮为放热反应  C . 测定溶液pH
C . 测定溶液pH  D . 测定盐酸浓度
D . 测定盐酸浓度 
常温下,浓度均为 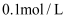 的4种钠盐溶液pH如下:下列说法错误的是( )
的4种钠盐溶液pH如下:下列说法错误的是( )
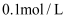 的4种钠盐溶液pH如下:下列说法错误的是( )
的4种钠盐溶液pH如下:下列说法错误的是( ) | 溶质 | | | NaClO | |
| pH | | | | |
A . 四种溶液中,  溶液中水的电离程度最大
B .
溶液中水的电离程度最大
B .  溶液显酸性的原因是:
溶液显酸性的原因是:  C . 向氯水中加入少量
C . 向氯水中加入少量  ,可以增大氯水中次氯酸的浓度
D . 常温下,相同物质的量浓度的
,可以增大氯水中次氯酸的浓度
D . 常温下,相同物质的量浓度的 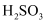 、
、  、HClO,pH最小的是
、HClO,pH最小的是 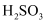
 溶液中水的电离程度最大
B .
溶液中水的电离程度最大
B .  溶液显酸性的原因是:
溶液显酸性的原因是:  C . 向氯水中加入少量
C . 向氯水中加入少量  ,可以增大氯水中次氯酸的浓度
D . 常温下,相同物质的量浓度的
,可以增大氯水中次氯酸的浓度
D . 常温下,相同物质的量浓度的 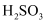 、
、  、HClO,pH最小的是
、HClO,pH最小的是 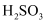
为验证氯水中次氯酸光照分解产物,采用数字化实验,得到的数据图像如图。该图像所代表的意义是( )
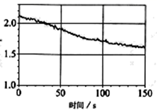
A . 氯离子浓度随时间的变化
B . 氧气体积分数随时间的变化
C . 氯水的pH随时间的变化
D . 氯水导电能力随时间的变化
下列关于实验操作或现象的说法正确的是( )

A . 图1:进行氢氧化铁胶体的电泳实验,通电后,阴极附近颜色逐渐加深
B . 图2:反应一段时间后,试管中固体变为红棕色
C . 图3:测定氯水的pH
D . 图4:接近滴定终点时,滴定管的尖嘴不可以接触锥形瓶内壁
下列实验误差分析错误的是( )
A . 用润湿的pH试纸测稀碱溶液的pH,测定值偏小
B . 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C . 用已知浓度的酸滴定未知浓度的碱,取碱时开始平视后来俯视,测试结果偏小
D . 测定中和反应的反应热时,将碱溶液缓慢倒入酸溶液中,所测温度值偏小
下列数据是某学生实验报告所列,其中合理的是( )
A . 用25mL碱式滴定管量取2.50mL氢氧化钠溶液
B . 用广泛pH试纸测得某溶液的pH为2.3
C . 用10mL量筒量取7.13mL稀盐酸
D . 配制100 mL 1mol/L的  溶液用托盘天平称取5.85g
溶液用托盘天平称取5.85g  固体
固体
 溶液用托盘天平称取5.85g
溶液用托盘天平称取5.85g  固体
固体
在常温条件下,下列说法错误的是( )
A .  的盐酸中
的盐酸中  B . 将
B . 将  溶液从常温加热至
溶液从常温加热至 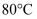 ,溶液的
,溶液的  变小但仍保持中性
C .
变小但仍保持中性
C . 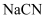 溶液呈碱性,说明
溶液呈碱性,说明 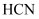 是弱电解质
D .
是弱电解质
D .  为3的醋酸溶液中加入醋酸的固体,溶液
为3的醋酸溶液中加入醋酸的固体,溶液  增大
增大
 的盐酸中
的盐酸中  B . 将
B . 将  溶液从常温加热至
溶液从常温加热至 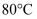 ,溶液的
,溶液的  变小但仍保持中性
C .
变小但仍保持中性
C . 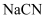 溶液呈碱性,说明
溶液呈碱性,说明 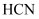 是弱电解质
D .
是弱电解质
D .  为3的醋酸溶液中加入醋酸的固体,溶液
为3的醋酸溶液中加入醋酸的固体,溶液  增大
增大
下列有关仪器的使用方法或实验操作正确的是( )
A . 洗净的容量瓶可放进烘箱中烘干
B . 滴定接近终点时,滴定管尖嘴可接触锥形瓶内壁
C . 测定溶液的  时,需先用蒸馏水润湿
时,需先用蒸馏水润湿  试纸
D . 焰色反应时,需先用
试纸
D . 焰色反应时,需先用  溶液洗涤铂丝并灼烧
溶液洗涤铂丝并灼烧
 时,需先用蒸馏水润湿
时,需先用蒸馏水润湿  试纸
D . 焰色反应时,需先用
试纸
D . 焰色反应时,需先用  溶液洗涤铂丝并灼烧
溶液洗涤铂丝并灼烧
下列由实验现象所得结论正确的是( )
A . 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔,在酒精灯上加热,铝箔熔化但不滴落,证明铝的熔点很高
B . 用pH试纸测得 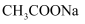 溶液的pH约为9,
溶液的pH约为9, 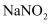 溶液的pH约为8,证明
溶液的pH约为8,证明  酸性大于醋酸
C . 向
酸性大于醋酸
C . 向  溶液中滴入硫酸酸化的
溶液中滴入硫酸酸化的  溶液,溶液由浅绿色变为棕黄色,证明
溶液,溶液由浅绿色变为棕黄色,证明  的氧化性强于
的氧化性强于 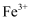 D . 取三支试管各加入等量的己烷、苯、甲苯,再分别加入几滴等量的酸性
D . 取三支试管各加入等量的己烷、苯、甲苯,再分别加入几滴等量的酸性 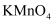 溶液,微热,仅盛有甲苯的试管中溶液褪色,证明苯环能使甲基更易被氧化
溶液,微热,仅盛有甲苯的试管中溶液褪色,证明苯环能使甲基更易被氧化
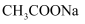 溶液的pH约为9,
溶液的pH约为9, 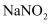 溶液的pH约为8,证明
溶液的pH约为8,证明  酸性大于醋酸
C . 向
酸性大于醋酸
C . 向  溶液中滴入硫酸酸化的
溶液中滴入硫酸酸化的  溶液,溶液由浅绿色变为棕黄色,证明
溶液,溶液由浅绿色变为棕黄色,证明  的氧化性强于
的氧化性强于 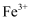 D . 取三支试管各加入等量的己烷、苯、甲苯,再分别加入几滴等量的酸性
D . 取三支试管各加入等量的己烷、苯、甲苯,再分别加入几滴等量的酸性 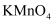 溶液,微热,仅盛有甲苯的试管中溶液褪色,证明苯环能使甲基更易被氧化
溶液,微热,仅盛有甲苯的试管中溶液褪色,证明苯环能使甲基更易被氧化
下列实验目的能实现的是( )
实验目的 | 操作步骤及现象 | |
A | 探究浓度对化学平衡的影响 |
|
B | 测定NaClO溶液的pH | 取一张pH试纸放在表面皿上,用洁净的玻璃棒蘸取NaClO溶液滴于试纸的中部,与标准比色卡对比得出结论 |
C | 证明酸性: | 向 |
D | 将 | 最终得到白色固体,成分为纯净的 |
A . A
B . B
C . C
D . D
最近更新





 溶液与
溶液与 溶液混合后平分到两支试管,一支加入
溶液混合后平分到两支试管,一支加入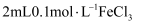 溶液,另一支加入
溶液,另一支加入 , 第一支试管中溶液颜色较深
, 第一支试管中溶液颜色较深
 溶液中滴入过量
溶液中滴入过量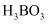 溶液,无气泡冒出
溶液,无气泡冒出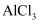 溶液加热蒸干
溶液加热蒸干


