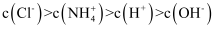е®һйӘҢ3-4 й…ёзўұж»ҙе®ҡжӣІзәҝзҡ„жөӢз»ҳ зҹҘиҜҶзӮ№йўҳеә“
в‘ pH=1зҡ„ејәй…ёжә¶ж¶ІпјҢеҠ ж°ҙзЁҖйҮҠеҗҺпјҢжә¶ж¶ІдёӯжүҖжңүзҰ»еӯҗзҡ„жө“еәҰдёҖе®ҡйҷҚдҪҺ
в‘ЎpH=2зҡ„зӣҗй…ёе’ҢpH=1зҡ„зӣҗй…ёпјҢcпјҲH+пјүд№ӢжҜ”дёә2пјҡ1
в‘ўpHзӣёзӯүзҡ„еӣӣз§Қжә¶ж¶ІпјҡaпјҺCH3COONaгҖҒbпјҺC6H5ONaгҖҒcпјҺNaHCO3гҖҒdпјҺNaOHпјҢжә¶иҙЁзҡ„зү©иҙЁзҡ„йҮҸжө“еәҰз”ұе°ҸеҲ°еӨ§зҡ„йЎәеәҸдёәdпјңbпјңcпјңa
в‘Јеҗ‘NH4HSO4жә¶ж¶Ідёӯж»ҙеҠ NaOHжә¶ж¶ІиҮіpH=7пјҢеҲҷcпјҲNa+пјү=cпјҲSO42п№Јпјү
в‘Өе·ІзҹҘйҶӢй…ёзҡ„з”өзҰ»еёёж•°дёәKa пјҢ йҶӢй…ёж №зҰ»еӯҗзҡ„ж°ҙи§Јеёёж•°дёәKh пјҢ ж°ҙзҡ„зҰ»еӯҗз§Ҝеёёж•°дёәKWпјӣеҲҷдёүиҖ…е…ізі»дёәKaвҖўKh=KW
в‘Ҙз”ІгҖҒд№ҷдёӨжә¶ж¶ІйғҪжҳҜејәз”өи§ЈиҙЁпјҢе·ІзҹҘз”Іжә¶ж¶Ізҡ„pHжҳҜд№ҷжә¶ж¶ІpHзҡ„2еҖҚпјҢеҲҷз”ІгҖҒд№ҷдёӨжә¶ж¶ІзӯүдҪ“з§Ҝж··еҗҲпјҢж··еҗҲжә¶ж¶Ізҡ„pHеҸҜиғҪзӯүдәҺ7
е…¶дёӯеҪ’зәіжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү
в‘ | в‘Ў | в‘ў | в‘Ј | |
жә¶ж¶І | ж°Ёж°ҙ | ж°ўж°§еҢ–й’ | йҶӢй…ё | зӣҗй…ё |
pH | 11 | 11 | 3 | 3 |
дҪңзү© | ж°ҙзЁ» | е°ҸйәҰ | зҺүзұі | еӨ§иұҶ | жІ№иҸң | жЈүиҠұ | 马й“ғи–Ҝ | жҙӢи‘ұ |
pH | 6пҪһ7 | 6.3пҪһ7.5 | 6пҪһ7 | 6пҪһ7 | 6пҪһ7 | 6пҪһ8 | 4.8пҪһ5.5 | 6пҪһ7 |
жҹҗиҜҫеӨ–е°Ҹз»„еҗҢеӯҰз ”з©¶еңҹеЈӨзҡ„й…ёзўұжҖ§пјҢж“ҚдҪңеҰӮдёӢпјҡе°ҶдёҖе®ҡдҪ“з§Ҝзҡ„и’ёйҰҸж°ҙеҠ е…ҘдёҖе®ҡиҙЁйҮҸзҡ„еңҹеЈӨдёӯпјҢе……еҲҶжҗ…жӢҢеҗҺпјҢиҝҮж»Ө并з•ҷеҸ–ж»Өж¶ІпјҢжөӢж»Өж¶Ізҡ„pHеҗҺеҗ‘ж»Өж¶Ідёӯж»ҙеҠ ж°Ёж°ҙпјҢжҜҸеҠ е…Ҙ2mLж°Ёж°ҙе°ұжҗ…жӢҢеқҮеҢҖ并жөӢйҮҸжә¶ж¶Ізҡ„pHпјҢз»ҳеҲ¶еҮәдёӢеӣҫпјҺ
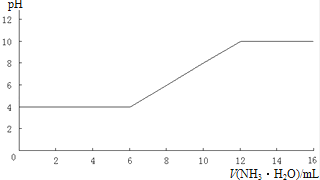
ж №жҚ®дёҠеӣҫеӣһзӯ”пјҡ
пјҲ1пјүеңЁжІЎжңүеҜ№еңҹеЈӨж”№иүҜеүҚпјҢиҜҘеңҹеЈӨжңҖеҸҜиғҪз§ҚжӨҚзҡ„дҪңзү©еҗҚз§°жҳҜ пјҺ
пјҲ2пјүиҜҘеңҹеЈӨж»Өж¶ІдёӯcпјҲH+пјү= пјҺ
пјҲ3пјүд»ҺдёҠеӣҫиҝҳиғҪеҫ—еҲ°зҡ„дҝЎжҒҜжңү пјҲзӯ”еҮәдёҖжқЎеҚіеҸҜпјүпјҺ
 пјҺ еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ
пјҺ еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ-
пјҲ1пјү 25в„ғж—¶пјҢжә¶ж¶Ізҡ„AGдёҺе…¶pHд№Ӣй—ҙзҡ„е…ізі»дёәAG= пјҺ
-
пјҲ2пјү 25в„ғж—¶пјҢдёҖе…ғејұзўұMOHжә¶ж¶Ізҡ„AG=п№Ј8пјҺеҸ–20mLиҜҘMOHжә¶ж¶ІпјҢеҪ“дёҺ16.2mL 0.05molвҖўLп№Ј1зЎ«й…ёж··еҗҲж—¶пјҢдёӨиҖ…жҒ°еҘҪе®Ңе…Ёдёӯе’ҢпјҺжұӮжӯӨжқЎд»¶дёӢиҜҘдёҖе…ғејұзўұзҡ„з”өзҰ»е№іиЎЎеёёж•°пјҺ
еҠ ж°Ёж°ҙдҪ“з§Ҝ/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 |
жә¶ж¶Ізҡ„pH | 4 | 4 | 4 | 4 | 6 | 8 | 10 | 10 | 10 |
еҲ©з”ЁдёҠиҝ°и®°еҪ•зҡ„ж•°жҚ®пјҢд»ҘеҠ е…Ҙзҡ„ж°Ёж°ҙдҪ“з§ҜдёәжЁӘеқҗж ҮгҖҒpHдёәзәөеқҗж Үз»ҳеҲ¶жӣІзәҝеӣҫпјҢе№¶ж №жҚ®жӣІзәҝеӣҫеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ
-
пјҲ1пјү жүҖжөӢеңҹеЈӨзҡ„й…ёзўұжҖ§еҰӮдҪ•пјҹ
-
пјҲ2пјү жүҖз”Ёж°Ёж°ҙзҡ„pHе’ҢcпјҲOHп№ЈпјүеҲҶеҲ«дёәеӨҡе°‘пјҹ
-
пјҲ3пјү дёәдҪҝиҜҘж»Өж¶Іе‘ҲдёӯжҖ§пјҢжүҖеҠ е…Ҙж°Ёж°ҙзҡ„жҒ°еҪ“дҪ“з§ҜжҳҜеӨҡе°‘пјҹ

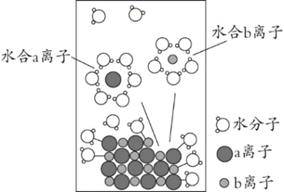

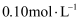 ж°Ёж°ҙ(
ж°Ёж°ҙ( )дёӯйҖҗж»ҙеҠ е…Ҙ
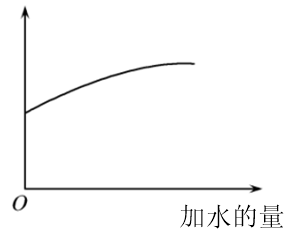
)дёӯйҖҗж»ҙеҠ е…Ҙ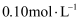 зҡ„зӣҗй…ёпјҢжә¶ж¶ІpHйҡҸжүҖеҠ зӣҗй…ёдҪ“з§ҜеҸҳеҢ–еҰӮеӣҫгҖӮдёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜпјҲ пјү
зҡ„зӣҗй…ёпјҢжә¶ж¶ІpHйҡҸжүҖеҠ зӣҗй…ёдҪ“з§ҜеҸҳеҢ–еҰӮеӣҫгҖӮдёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜпјҲ пјү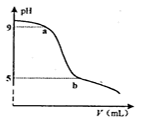
 B . bзӮ№еӨ„еӯҳеңЁ
B . bзӮ№еӨ„еӯҳеңЁ C . з”ұaвҶ’bпјҢжә¶ж¶Ідёӯ
C . з”ұaвҶ’bпјҢжә¶ж¶Ідёӯ жҢҒз»ӯеўһеӨ§
D .
жҢҒз»ӯеўһеӨ§
D . 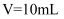 ж—¶пјҢеӯҳеңЁ
ж—¶пјҢеӯҳеңЁ