实验4-1 纯净物与混合物性质的比较 知识点题库
合金是一类用途广泛的金属材料,下列关于合金的描述正确的是( )
A . 合金的硬度比组成它的成分金属小
B . 合金的熔点一般比组成它的成分金属高
C . 在我国,使用最早的合金是青铜
D . 目前用量最大、用途最广泛的合金是铝合金
工业生产中,常将两种或多种金属(或金属与非金属)在同一容器中加热使其熔合,冷凝后得到具有金属特性的熔合物——合金,这是制取合金的常用方法之一。仅根据下表数据判断,不宜用上述方法制取的合金是( )
金属 | Na | K | Al | Cu | Fe |
熔点/℃ | 97.5 | 63.6 | 660 | 1083 | 1535 |
沸点/℃ | 883 | 774 | 2467 | 2567 | 2750 |
A . Fe、Cu合金
B . Cu、Al合金
C . Al、Na合金
D . Cu、Na合金
格林太太镶有两颗假牙:第一个是黄金的,第二颗是不锈钢的.令人百思不解的是,自从镶上假牙后,格林太太经常头疼、夜间失眠、心情烦躁某同学提出以下几种方案来治疗格林太太的“疾病”,理论上可行的是( )
A . 把不锈钢牙都换成铝质假牙
B . 把金质假牙换成铝质假牙
C . 把不锈钢假牙换成金质假牙
D . 在不锈钢假牙表面镀上一层金
浓硝酸、稀硝酸都具有强氧化性,某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行试验(夹持仪器的装置已略去).实验表明浓硝酸能将NO氧化成NO2 , 而稀硝酸不能氧化NO.由此得出的结论是浓硝酸的氧化性强于稀硝酸.
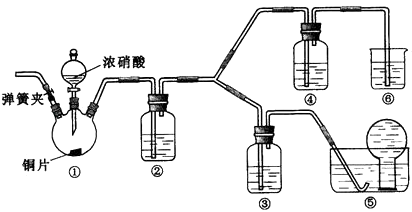
可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应
2NO2+2NaOH═NaNO3+NaNO2+H2O
-
(1) 浓硝酸与NO反应的氧化产物与还原产物的物质的量之比为
-
(2) 实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是
-
(3) 滴加浓硝酸之前的操作依次是检验装置的气密性,加入药品,打开弹簧夹后
-
(4) 装置①中发生反应的化学方程式是,装置②的作用是,发生反应的化学方程式是
-
(5) 该小组得出的结论所依据的实验现象是
-
(6) 试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色.甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体.同学们分别设计了以下4个试验来判断两种看法是否正确.这些方案中可行的是(选填序号字母)
a.加热该绿色溶液,观察颜色变化
b.加水稀释绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化.
下列有关合金的说法错误的是( )
A . 青铜是我国使用最早的合金
B . 钢是用量最大、用途最广的合金
C . 合金的硬度一般高于各成分金属
D . 合金的熔点一般高于各成分金属
下列有关物质的性质与用途不对应的是( )
A . 铝合金的密度小,硬度大,可用作建筑材料
B . 食品工业中用Na2CO3作焙制糕点的膨松剂
C . FeCl3溶液能与Cu反应,可用于腐蚀铜制印刷电路板
D . 明矾能生成Al(OH)3胶体,可用作净水剂
固体化合物X由3种元素组成。某学习小组进行了如下实验:

请回答:
-
(1) 由现象1得出化合物X含有元素(填元素符号)。
-
(2) 固体混合物Y的成分(填化学式)。
-
(3) X的化学式。X与浓盐酸反应产生黄绿色气体,固体完全溶解,得到蓝色溶液,该反应的化学方程式是。
下列实验装置能达到实验目的是(夹持仪器未画出)( )
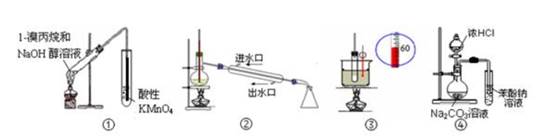
A . ①装置用于检验1-溴丙烷消去产物
B . ②装置用于石油的分馏
C . ③装置用于实验室制硝基苯
D . ④装置可装置证明酸性:盐酸>碳酸>苯酚
钛和钛的合金具有很多优良的性能,如熔点高、密度小、可塑性好、易于加工,尤其是钛合金与人体器官具有很好的“生物相容性”。下列有关钛用途不合适的是( )
A . 用来做保险丝
B . 用于制造航天飞机
C . 用来制造人造骨
D . 用于家庭装修,做钛合金装饰门
2020年11月10日,中国“奋斗者”"号载人潜水器在马里亚纳海沟深度10909米处成功坐底并进行了一系列的深海探测科考活动。下列说法正确的是( )
A . “奋斗者”号使用的锂离子电池工作时Li向负极移动
B . 制造潜水器载人球舱的钛合金比纯金属钛具有更高的强度、韧性和熔点
C . “奋斗者”号返回水面的浮力材料纳米级玻璃微珠可产生了达尔效应
D . 未来对海底“可燃冰”(主要成分为甲烷)的开采将有助于缓解能源危机
某研究学习小组利用下列装置检验浓硫酸与某铁、碳合金丝的反应(其他杂质不参与反应,夹持装置已省略):

请回答:
-
(1) I中不加热时无明显现象是因为。
-
(2) 加热I试管后说明有SO2气体生成的实验现象是。
-
(3) V中出现少量浑浊是因为I中发生了反应(用化学方程式表示)
-
(4) 下列说法正确的是_______A . 反应前,检查装置I的气密性,需在II中加水至浸没导管,微热I中试管,若II中导管口有气泡溢出,就可以说明装置I气密性良好 B . 装置I的优点是可通过抽动铁、碳合金丝控制反应的进行 C . 取下试管III并不断振荡,试管中出现浑浊,是因为生成了BaSO4 D . 试管IV中KMnO4溶液褪色,说明SO2具有氧化性
金属和金属材料与人们的日常生活密不可分,下列认识错误的是( )
A . 一般用铜而不用银作导线,主要是由于考虑价格的因素
B . 铁制品比铝制品容易腐蚀,是由于铁的化学性质比铝活泼
C . 用盐酸可区分假黄金,是由于金不能与盐酸反应,而锌能与盐酸反应
D . 用硫酸铜配制的波尔多液不能用铁制容器盛放,是因为铁能与硫酸铜发生反应
钢铁是现代工业的脊梁我国钢铁产量多年位居世界第一。现有一块铁碳合金(钢铁材料),某化学兴趣小组为了测定合金中铁的质量分数,并探究浓硫酸的某些性质设计了如图所示的实验装置进行实验(夹持仪器已省略),请你参与其中:

-
(1) 仪器A的名称是 。按图示连接好装置,先,再加入药品,称量F的质量。
-
(2) 将mg合金样品放入A中,再加入适量的浓硫酸,未点燃酒精灯前,A、B中均无明显现象,原因是。
-
(3) 点燃酒精灯一段时间后,A、B中可观察到明显的现象。A中发生反应的化学方程式为
 、。B中的现象为。
、。B中的现象为。
-
(4) 装置C的作用是 。
-
(5) D中盛放的试剂是。
-
(6) 反应一段时间待A中不再逸出气体时,停止加热恢复到室温后拆下F称重F增重bg。则铁碳合金中铁的质量分数为 (用含m、b的代数式表示)。
-
(7) 最后对所得测定结果进行评价时,小组内有同学提出本套装置在设计上存在缺陷而导致铁质量分数测定值偏低,可能的原因是 。
下列说法正确的是( )
A .  在空气中加热可得固体
在空气中加热可得固体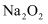 B . 工厂静电除尘是利用胶体带电的性质
C . 司母戊鼎的主要成分是铁
D . 自来水通过蒸馏的方法获得蒸馏水一定需要蒸馏烧瓶和温度计
B . 工厂静电除尘是利用胶体带电的性质
C . 司母戊鼎的主要成分是铁
D . 自来水通过蒸馏的方法获得蒸馏水一定需要蒸馏烧瓶和温度计
 在空气中加热可得固体
在空气中加热可得固体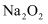 B . 工厂静电除尘是利用胶体带电的性质
C . 司母戊鼎的主要成分是铁
D . 自来水通过蒸馏的方法获得蒸馏水一定需要蒸馏烧瓶和温度计
B . 工厂静电除尘是利用胶体带电的性质
C . 司母戊鼎的主要成分是铁
D . 自来水通过蒸馏的方法获得蒸馏水一定需要蒸馏烧瓶和温度计
探究铜丝与过量浓硫酸的反应,下列装置(部分夹持装置略)或操作错误的是( )
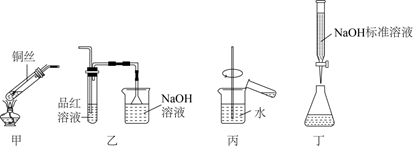
A . 用装置甲进行铜丝和浓硫酸的反应
B . 用装置乙验证有二氧化硫生成并吸收尾气
C . 用装置丙稀释反应后的混合液
D . 用装置丁测定余酸的浓度
科技改变生活。下列说法正确的是( )
A . 丰宁抽水蓄能电站保障了北京冬奧会的电力供应,利用的是电能和化学能的相互转化
B . “雷霆之星”速滑服采用银离子抗菌技术,可有效防护细菌侵入
C . “天问一号”中Ti- Ni形状记忆合金的两种金属都属于主族金属元素
D . “天机芯”是全球首款异构融合类脑计算芯片,其主要成分和光导纤维相同
我国材料的发展充分体现了“中国技术”、“中国制造”和“中国力量”,下列有关说法错误的是( )
A . 三星堆青铜大面具亮相虎年春晚,展示了三星堆青铜文化的独特魅力。青铜属于合金,比纯铜具有更高的熔点
B . 北斗卫星导航专用ASIC硬件结合国产应用处理器打造出一颗真正意义的“中国芯”,该“中国芯”的主要成分为Si
C . 2021年我国科学家首次实现由CO2人工合成淀粉,淀粉是由碳、氢、氧三种元素组成的高分子化合物
D . 2022年2月我国成功举办第24届冬奥会,北京冬奥会使用二氧化碳跨临界制冰机组,与传统制冷剂氟利昂相比更加环保
古文献中常会涉及一些与化学相关的研究成果。下列说法错误的是( )
A . 《抱朴子·黄白》中“以曾青涂铁,铁赤色如铜”主要发生了置换反应
B . 《神农本草经》中“水银…熔化(加热)还复为丹”,其中水银是指金属银
C . 《吕氏春秋》中“金(即铜)柔锡柔,合两柔则刚”体现了合金硬度方面的特性
D . 《己亥杂诗》中“落红不是无情物,化作春泥更护花”蕴含着自然界碳、氮的循环
某兴趣小组用如图所示的装置探究 气体的还原性,下列说法错误的是( )
气体的还原性,下列说法错误的是( )
 气体的还原性,下列说法错误的是( )
气体的还原性,下列说法错误的是( )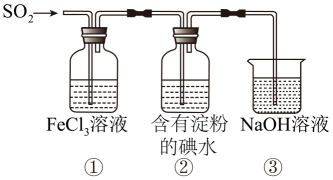
A . ①中发生反应的离子方程式为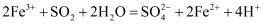 B . ①中加入
B . ①中加入 溶液,紫红色褪去,可说明
溶液,紫红色褪去,可说明 与
与 发生了氧化还原反应
C . ②中蓝色溶液褪色的现象能表明
发生了氧化还原反应
C . ②中蓝色溶液褪色的现象能表明 的还原性强于
的还原性强于 D . 装置③的作用是吸收
D . 装置③的作用是吸收 尾气,防止污染空气
尾气,防止污染空气
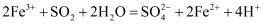 B . ①中加入
B . ①中加入 溶液,紫红色褪去,可说明
溶液,紫红色褪去,可说明 与
与 发生了氧化还原反应
C . ②中蓝色溶液褪色的现象能表明
发生了氧化还原反应
C . ②中蓝色溶液褪色的现象能表明 的还原性强于
的还原性强于 D . 装置③的作用是吸收
D . 装置③的作用是吸收 尾气,防止污染空气
尾气,防止污染空气
已知:25℃, ,
,  为探究
为探究 溶液的性质,进行如下实验。①测量某
溶液的性质,进行如下实验。①测量某 溶液的
溶液的 ,
, 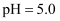 , ②向
, ②向
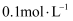
 溶液中滴加
溶液中滴加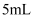
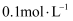
 溶液,无明显现象③向
溶液,无明显现象③向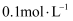
 溶液中滴加少量酸性
溶液中滴加少量酸性 溶液,
溶液, 溶液的紫红色褪去。④向
溶液的紫红色褪去。④向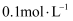
 溶液中滴加过量
溶液中滴加过量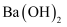 溶液,出现白色沉淀。下列说法正确的是( )
溶液,出现白色沉淀。下列说法正确的是( )
 ,
,  为探究
为探究 溶液的性质,进行如下实验。①测量某
溶液的性质,进行如下实验。①测量某 溶液的
溶液的 ,
, 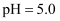 , ②向
, ②向
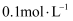
 溶液中滴加
溶液中滴加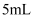
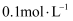
 溶液,无明显现象③向
溶液,无明显现象③向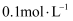
 溶液中滴加少量酸性
溶液中滴加少量酸性 溶液,
溶液, 溶液的紫红色褪去。④向
溶液的紫红色褪去。④向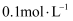
 溶液中滴加过量
溶液中滴加过量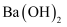 溶液,出现白色沉淀。下列说法正确的是( )
溶液,出现白色沉淀。下列说法正确的是( )
A . 实验①说明该溶液中 B . 实验②所得溶液中
B . 实验②所得溶液中 C . 实验③中发生反应:
C . 实验③中发生反应: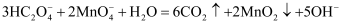 D . 实验④中反应的离子方程式为
D . 实验④中反应的离子方程式为
 B . 实验②所得溶液中
B . 实验②所得溶液中 C . 实验③中发生反应:
C . 实验③中发生反应: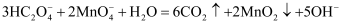 D . 实验④中反应的离子方程式为
D . 实验④中反应的离子方程式为
最近更新



