专题3 从矿物到基础材料 知识点题库
a.质轻 b.延展性好
c.易导热 d.易导电
e.氧化时放热
-
(1) ①太阳能热水器:;②飞机:③焊接铁轨:;④电缆:;⑤铝箔:。
-
(2) 佛山是有色金属之乡,其中铝合金材料的产量约占全国的一半。铝合金材料属于(填“纯净物”、“混合物”或“单质”)。
绿矾是一种重要的化工原料.
【问题1】绿矾晶体(FeSO4•7H2O)由于保存不妥或长久放置,容易被空气中的氧气氧化而变质.为探究绿矾样品的变质情况,化学兴趣小组的同学设计了下列实验方案.可供选择的试剂:KSCN溶液、酸性KMnO4溶液、Cl2水、NaOH溶液、BaCl2溶液请参与完成方案设计.
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液.
方案1:取少量溶液,加入几滴 试剂,如果观察到的现象是 ;实验结论:证明绿矾样品没有被氧化.
方案2:取少量溶液,加入几滴 试剂,如果观察到的现象是 .
实验结论:证明绿矾样品完全被氧化.
使用FeSO4时,如要防止Fe3+的干扰,可以加入适量铁粉进行除杂,写出加入铁粉后发生反应的离子方程式 .
【问题2】以绿矾为原料可以制取聚合硫酸铁(SPFS).聚合硫酸铁是一种重要的无机高分子絮凝剂,极易溶于水,作为工业和生活污水处理等领域具有重要的应用.其组成可表示成Fex(OH)y(SO4)z•nH2O(其中Fe为+3价).工业上常用的一种制备流程为:

取7.507g某固体聚合硫酸铁溶解于水,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得白色沉淀10.485g,向上述滤液中加入NH3•H2O,调节溶液pH=6,经过滤、洗涤、干燥得Fe2O3固体2.800g.通过计算确定该固体聚合硫酸铁样品的化学式为 .(写出计算过程)
 K↑+NaCl)
B . 利用Al2O3制作的坩埚,可用于熔融烧碱
C . 氢氟酸具有强酸性,用氢氟酸蚀刻玻璃
D . 制水泥和玻璃都用石灰石作原料
K↑+NaCl)
B . 利用Al2O3制作的坩埚,可用于熔融烧碱
C . 氢氟酸具有强酸性,用氢氟酸蚀刻玻璃
D . 制水泥和玻璃都用石灰石作原料
-
(1) 中国高铁发展迅速,高铁建设使用的主要材料有钢铁、铝合金和玻璃等.
①高炉炼铁和制造普通玻璃都要用到的原料是.高温下将铁矿石还原为金属铁的主要还原剂是.
②下列关于铝及铝合金的叙述不正确的是(填字母).
a.密度小 b.抗腐蚀能力强 c.不与浓硫酸反应
③钢铁、铝合金、玻璃都属于(填字母).
a.混合物 b.化合物 c.单质
-
(2) 化学实验和科学研究中,经常需要配制一定物质的量浓度的溶液.欲配制0.2mol/LNa2CO3溶液100mL.
①容量瓶在使用前首先应该.需要用托盘天平称量Na2CO3的质量为g.
②配制时,需“将容量瓶塞盖好,反复上下颠倒,摇匀”,摇匀前的一步操作是.
③下列操作,会使最后配成溶液的实际浓度比所要求的浓度偏小的是(填字母).
a.定容时,俯视刻度线,溶液的凹面和刻度线相切,停止加水
b.定容时,如果加水超过了刻度线,立即用胶头滴管吸出多余的部分
c.将称出的Na2CO3在烧杯中溶解,所得溶液恢复至室温再转移到容量瓶中
④准确量取一定体积所配制的Na2CO3溶液加少量水稀释,则稀释前后的溶液分别与盐酸反应时,消耗HCl的物质的量(填“相同”、“不相同”、或“无法确定”).
-
(3) 生活环境的改善,需要对生活和生产中的废弃进行处理.
①燃煤排放的二氧化硫会被雨水吸收形成酸雨,这种酸雨在空气中放置酸性增强的原因是(用化学方程式表示).可以在已酸化的土壤中撒些从而消除酸雨造成的影响.
②氮肥和硝酸的工业生产以及汽车等交通工具的使用,会有大量的氮氧化物排放到空气中,这些氮氧化物对环境造成的影响有(填一种即可).氮氧化物可用氢氧化钠溶液吸收转化为NaNO3、和H2O.汽车安装尾气催化转化装置,可将尾气中的氮氧化物和一氧化碳转化为CO2和.
①加盐酸溶解
②加烧碱溶液溶解
③过滤
④通入过量CO2生成Al(OH)3沉淀
⑤加入盐酸生成盐胜生成Al(OH)3沉淀
⑥加入过量烧碱溶液.

-
(1) 检验“含碘废水”中含有的单质I2 , 常用的试剂是。
-
(2) 进行“过滤1”时,需同时对CuI沉淀进行洗涤。在洗涤过滤滤液中可通过滴加盐溶液来检验其是否已洗涤干净。
-
(3) “滤渣2”的成分为(填化学式)。
-
(4) “制KI”时,发生反应的化学方程式为。
-
(5) 江苏食用加碘盐新标准是每千克食盐中碘元素含量为25毫克(波动范围为18~33mg/kg)。测定食盐试样中碘元素含量的步骤如下:称取4.000g市售食盐加入锥形瓶中,依次加入适量的水、稍过量KI及稀硫酸;充分反应后,再加入12.00mL6.000×10-4mol·L-1Na2S2O3溶液,与生成的碘恰好完全反应。有关反应原理为:
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O; I2+2S2O
 =2I- +S4O
=2I- +S4O 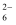 。
。①计算该食盐试样中碘元素的含量(单位mg/kg,写出计算过程)。
②该食盐试样是否符合江苏食用加碘盐新标准,并说明判断依据。
①硫酸钡难溶于水和酸,可做X光透视肠胃的药剂
②神舟10号飞船所用太阳能电池板的材料是单晶硅
③医用酒精是利用了乙醇的氧化性来杀菌消毒的
④玛瑙饰品的主要成分与建筑材料砂子不相同
⑤碳酸钠、氢氧化钠、碳酸氯钠等都可以中和酸,故都可以作为治疗胃酸过多的药物
⑥明矾净水利用了胶体的性质
⑦根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸和多元酸
⑧金属钠具有強的还原性,可利用钠和熔融TiCl4反应制取金属Ti
-
(1) 工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应的化学方程式漂白粉的有效成分是(填化学式)。
-
(2) 实验室制取氨气的化学方程式:
-
(3) 1.2gRSO4中含0.01molR2+ , 则RSO4的摩尔质量是;
-
(4) 实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因现象是: 。反应的化学方程式:
-
(5) 碳酸钠水解反应的离子方程式(第一步): 。
-
(6) 铅蓄电池的负极反应式: 。
-
(7) 硫酸钡的沉淀溶解平衡:。
NaHCO3+H2  HCOONa+H2O下列有关说法正确的是( )
HCOONa+H2O下列有关说法正确的是( )

 +Fe2+═FeCO3↓+CO2↑+H2O
C . 可用稀硫酸和K3[Fe(CN)6]溶液检验铁红中是否含有FeCO3
D . “冷却结晶”后的操作是过滤,“锻烧”操作的主要仪器有酒精灯、蒸发皿、玻璃棒
+Fe2+═FeCO3↓+CO2↑+H2O
C . 可用稀硫酸和K3[Fe(CN)6]溶液检验铁红中是否含有FeCO3
D . “冷却结晶”后的操作是过滤,“锻烧”操作的主要仪器有酒精灯、蒸发皿、玻璃棒
①过量的Fe在Cl2中燃烧;②Fe和过量盐酸反应;③向FeCl2溶液中通入少量Cl2;④将Fe和Fe2O3的混合物溶于盐酸中

 B .
B .  C .
C .  D .
D . 

选项 | 甲 | 乙 | 丙 | 丁 |
A | Na | NaOH | Na2CO3 | NaCl |
B | Ca | CaO | Ca(OH)2 | CaCO3 |
C | Al2O3 | AlCl3 | NaAlO2 | Al(OH)3 |
D | 乙醇 | 乙醛 | 乙酸 | 乙酸乙酯 |
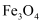 、
、 、
、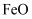 和二氧化硅等。下面是以硫铁矿烧渣制备高效净水剂聚合硫酸铁
和二氧化硅等。下面是以硫铁矿烧渣制备高效净水剂聚合硫酸铁 流程图:
流程图: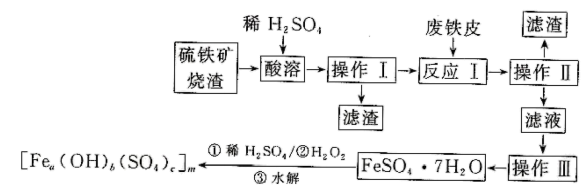
-
(1) 为了加快硫铁矿烧渣“酸溶”速率,常采用的方法是(任写一种)。
-
(2) “操作III”系列操作名称依次为、、过滤和洗涤。
-
(3) “酸溶”过程中
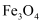 溶解的化学反应方程式为。
溶解的化学反应方程式为。
-
(4) 实验室检验“反应I”已经反应完全的方法是。
-
(5) 加入适量
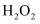 的目的是氧化
的目的是氧化 , 写出
, 写出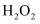 氧化
氧化 的离子方程式。
的离子方程式。
-
(6) 为了测定聚合硫酸铁
 中a、b、c的比例关系,取一定量的聚合硫酸铁,溶于水配成溶液,分成两等份,其中一份与足量
中a、b、c的比例关系,取一定量的聚合硫酸铁,溶于水配成溶液,分成两等份,其中一份与足量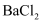 溶液反应,得到沉淀5.825g,另一份用足量铁粉还原,充分反应后过滤,用
溶液反应,得到沉淀5.825g,另一份用足量铁粉还原,充分反应后过滤,用 酸性
酸性 溶液滴定,消耗酸性
溶液滴定,消耗酸性 , 溶液
, 溶液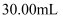 , 请根据数据计算聚合硫酸铁
, 请根据数据计算聚合硫酸铁 中
中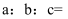 (已知
(已知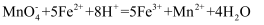 )。
)。




