第三节 化学键 知识点题库
根据氢原子和氟原子的核外电子排布,对F2和HF分子中形成的共价键描述正确的是( )
A . 两者都为s-sσ键
B . 两者都为p-pσ键
C . 前者为p-pσ键,后者为s-pσ键
D . 前者为s-sσ键,后者为s-pσ键
无水CoCl2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水CoCl2 , 故常在实验室中用作吸湿剂和空气湿度指示剂.
CoCl2+H2O⇌CoCl2•xH2O
深蓝色 粉红色
现有65g无水CoCl2 , 吸水后变成CoCl2•xH2O 119g.
(1)水合物中x= .
(2)若该化合物中Co2+配位数为6,而且经定量测定得知内界和外界各占有Cl﹣个数为1:1,则其化学式可表示为
A、B、C、D、E是原子序数依次增大的五种短周期元素.B、E同主族,且满足最高正化合价+最低负化合价=0;A与C、D与C之间都能形成原子个数比分别为2:1和1:1的两种化合物.试解答下列有关问题.
-
(1) 在A2C2分子中含有的化学键是和.
-
(2) C与D形成的化合物的电子式为.
-
(3) 实验室可用由B、C、D组成的化合物为反应物之一制取由A、C、D组成的化合物,反应的化学方程式为.
-
(4) 写出E单质与A、C、D形成的化合物的水溶液反应的离子方程式.
CO2气体在一定条件下可与金属镁反应,干冰在一定条件下也可以形成CO2气体,这两个变化过程中需要克服的作用分别是( )
A . 分子间作用力,离子键
B . 化学键,分子间作用力
C . 化学键,化学键
D . 分子间作用力,分子间作用力
下列各组物质中,只含有共价键的是( )
A . NH3、CO2
B . CaO、HCl
C . Na2S、MgO
D . H2O、Na2O2
下列说法中正确的是( )
A . 在化学键的断裂过程中,肯定发生了化学反应
B . 发生能量变化的一定是化学反应
C . 离子化合物中一定含有离子键,共价化合物中一定不含离子键
D . 在化学键的断裂过程中,肯定放出能量
科学家研究发现普通盐水在无线电波的照射下可以燃烧,其原理是无线电频率可以削弱盐水中所含元素原子之间的“结合力”,释放出氢原子和氧原子,一旦点火,氢原子就会在这种频率下持续燃烧。上述中“结合力”的实质是( )
A . 离子键
B . 离子键与共价键
C . 极性共价键
D . 非极性共价键
科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似。气态时,已知断裂1mol N—N键吸收193kJ热量,断裂1mol N≡N键吸收941kJ热量,则( )
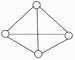
A . N4与N2互称为同位素
B . 1mol N4气体转化为N2时要吸收748kJ能量
C . N4是N2的同系物
D . 1mol N4气体转化为N2时要放出724kJ能量
下列说法正确的是( )
A . HCl的电子式为H:Cl
B . Na2O2只含有离子键
C . 质量数为12的C原子符号为12C
D . 用电子式表示KBr的形成过程: 
既存在离子键又存在共价键的是( )
A . NaOH
B . 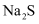 C . Ne
D .
C . Ne
D . 
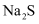 C . Ne
D .
C . Ne
D . 
已知某种锂盐的结构如图,它是一种新型锂离子电池的电解质,其阴离子由W、X、Y、Z四种同周期主族元素构成,Y原子的最外层电子数是X的次外层电子数的3倍(箭头指向表示共用电子对由W提供)。下列说法错误的是( )
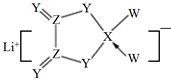
A . 元素非金属性强弱顺序是W>Y>Z>X
B . 阴离子中X与Z的杂化方式相同
C . 原子半径X>Z>Y>W
D . 该物质中含有极性键、非极性键、配位键和离子键
下列五种物质中 ①Ne ②H2O
③NH3 ④KOH ⑤Na2O(填写序号):只存在共价键的是 ,只存在离子键的是 ,既存在共价键又存在离子键的是 ,不存在化学键的是。
下列说法中,正确的是( )
A . HCl气体溶于水形成盐酸,存在H+ , 所以HCl为离子化合物
B . 含金属元素的离子一定是阳离子
C . 含有共价键的化合物一定是共价化合物
D . 稀有气体原子之间不易形成共价键
在乙烯分子中有5个σ键和1个π键,它们分别是( )
A . sp2杂化轨道形成σ键,未杂化的2p轨道形成π键
B . sp2杂化轨道形成π键,未杂化的2p轨道形成σ键
C . C-H之间是sp2杂化轨道形成σ键,C-C之间是未杂化的2p轨道形成π键
D . C-C之间是sp2杂化轨道形成σ键,C-H之间是未杂化的2p轨道形成π键
南开大学科研团队经过多年研究,获得了一种特殊的石墨烯材料,这种三维石墨烯(如图)可在太阳光照射下飞行。下列四种物质中与三维石墨烯属于同一类物质的是( )
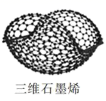
A . 聚合氮 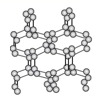 B . 全氮阴离子盐
B . 全氮阴离子盐 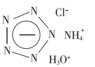 C . 双氢青蒿素
C . 双氢青蒿素 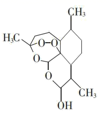 D . 白藜芦醇
D . 白藜芦醇 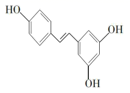
 B . 全氮阴离子盐
B . 全氮阴离子盐  C . 双氢青蒿素
C . 双氢青蒿素  D . 白藜芦醇
D . 白藜芦醇 
下列物质中只含离子键的是( )
A . 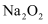 B .
B . 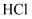 C .
C .  D .
D . 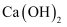
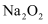 B .
B . 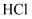 C .
C .  D .
D . 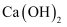
X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中两种或三种元素组成的化合物,己是Z元素形成的单质。已知:甲+乙→丁+己,甲+丙→戊+己;25℃时,0.1 mol·L-1的丁溶液pH=13.下列说法错误的是( )
A . 1 mol甲与足量乙反应转移2 mol电子
B . 离子半径Z>W
C . 甲与丙反应时,既有离子键、共价键的断裂,又有离子键、共价键的形成
D . 四种元素可以组成化合物WXY2Z4
我国科研工作者研发的一种在较低温度下有机物  转化为
转化为 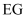 的反应过程如图所示。
的反应过程如图所示。
 转化为
转化为 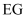 的反应过程如图所示。
的反应过程如图所示。 
下列说法错误的是( )
A . 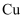 纳米颗粒是一种胶体,能降低氢气解离的活化能
B . 反应过程中断裂的化学键有
纳米颗粒是一种胶体,能降低氢气解离的活化能
B . 反应过程中断裂的化学键有 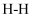 、
、 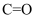 、
、 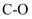 C .
C . 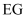 与甘油含有相同官能团但不属于同系物
D . 可用金属钠区别
与甘油含有相同官能团但不属于同系物
D . 可用金属钠区别 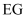 与
与 
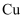 纳米颗粒是一种胶体,能降低氢气解离的活化能
B . 反应过程中断裂的化学键有
纳米颗粒是一种胶体,能降低氢气解离的活化能
B . 反应过程中断裂的化学键有 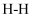 、
、 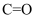 、
、 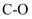 C .
C . 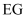 与甘油含有相同官能团但不属于同系物
D . 可用金属钠区别
与甘油含有相同官能团但不属于同系物
D . 可用金属钠区别  与
与 
选择下列物质填空(填写序号):①金刚石 ②干冰 ③氩晶体 ④白磷 ⑤氯化钙 ⑥过氧化钠⑦石英 ⑧石墨 ⑨氯化铵 ⑩铜晶体
-
(1) 固态时能导电的有
-
(2) 熔化时不破坏化学键的有
-
(3) 含有配位键的有
-
(4) 含有非极性共价键的有
下列说法错误的是( )
A . 共价化合物只含共价键,离子化合物不一定只含离子键
B . 离子化合物熔融一定能导电,共价化合物溶于水一定能导电
C . 有化学键的断裂不一定发生了化学反应
D . 离子化合物一定是电解质
最近更新



