第二单元 物质的化学计量 知识点题库
用摩尔(mol)作为单位的基本物理量是( )
A . 长度
B . 质量
C . 数量
D . 物质的量
NA为阿伏加德罗常数的数值,下列说法中正确的是( )
A . 在密闭容器中加入l.5mol H2和0.5molN2 , 充分反应后得到NH3分子数为NA
B . 一定条件下,2.3g的Na完全与O2反应生成3.9g产物时失去的电子数为0.1NA
C . 1.0L的0.1 mol•L﹣1Na2S溶液中含有的S2﹣离子数为0.1NA
D . 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA
某核素AZX可形成HmX型氢化物,则agHmX含有( )
A . 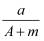 (Z+m)mol 质子
B .
(Z+m)mol 质子
B . 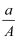 (Z+m)mol 电子
C .
(Z+m)mol 电子
C . 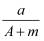 (A﹣Z+m)mol 中子
D .
(A﹣Z+m)mol 中子
D . 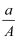 mmolHmX
mmolHmX
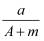 (Z+m)mol 质子
B .
(Z+m)mol 质子
B . 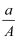 (Z+m)mol 电子
C .
(Z+m)mol 电子
C . 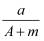 (A﹣Z+m)mol 中子
D .
(A﹣Z+m)mol 中子
D . 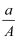 mmolHmX
mmolHmX
实验室里需要480mL0.100mol/LCuSO4溶液,以下配制操作正确的是( )
A . 称取7.68gCuSO4加水配成480mL溶液
B . 称取12.5g 胆矾,加水配成500mL溶液
C . 称取8.0CuSO4 , 加水500mL 溶解配成溶液
D . 称取12.0g胆矾,加水480mL溶解配成溶液
某气体的质量是9.5g,体积是5.6升(标准状况下),该气体的摩尔质量是( )
A . 38
B . 38g•mol﹣1
C . 19
D . 19g•mol﹣1
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 4.6g乙醇含有的C﹣H键数为0.6NA
B . 2gD216O含有的质子数和中子数均为NA
C . 每生成1molO2 , 转移的电子数一定为4NA
D . 标准状况下,22.4L NO与11.2L O2充分反应,产物分子数为NA
比较1.0mol N2和1.0mol CO的下列物理量:①质量 ②分子总数 ③原子总数,其中相同的是( )
A . ①③
B . ①②
C . ①②③
D . ②③
NA表示阿伏加德罗常数。硫与浓硝酸反应的化学方程式为:S+6HNO3(浓)→H2SO4+6NO2↑+2H2O,有关说法正确的是( )
A . 氧化剂与还原剂物质的量之比为1:6
B . 每产生2.24升NO2转移电子0.1NA个
C . 随着反应进行溶液的酸性逐渐增强
D . 氧化性:HNO3(浓)>H2SO4
下列有关阿伏加德罗常数(NA)的说法错误的是( )
A . 22.4L O2所含的原子数目为NA
B . 0.5mol H2O含有的原子数目为1.5NA
C . 1mol H2O含有的H2O分子数目为NA
D . 0.5 NA个氯气分子的物质的量是0.5mol
NA代表阿伏加德罗常数的值。下列说法正确的是( )
A . 常温常压下,124gP4中所含P—P键数目为4NA
B . 100mL1mol·L−1FeCl3溶液中所含Fe3+的数目为0.1NA
C . 标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为2NA
D . 密闭容器中,2molSO2和1molO2催化反应后分子总数为2NA
下列说法正确的是( )
A . 1 mol H2的质量只有在标准状况下才为2 g
B . 标准状况下,1 mol水蒸气的体积大约为22.4 L
C . 273 ℃、1.01×105 Pa状态下,1 mol气体体积大于22.4 L
D . 0.5 mol O2和0.5 mol N2组成的混合气体体积约为22.4 L
同温同压下,相同体积的SO2和O3气体,下列叙述中错误的是( )
A . 质量比4∶3
B . 电子数比1∶1
C . 密度比4∶3
D . 氧原子数比2∶3
设NA代表阿伏加德罗常数,下列说法正确的是( )
A . 室温下,32gO2和O3的混合气体中含有的氧原子数为2NA
B . 浓盐酸与MnO2共热产生22.4L Cl2时,转移电子数为2NA
C . 0.5 mol·L-1MgCl2溶液中,含有Cl-个数为NA
D . 18 g NH4+中所含的质子数为10NA
下列物质中含原子数最多的是( )
A . 6.4g O2
B . 8.8g CO2
C . 0.1mol N2
D . 3.01×1022个H2O
若50g密度为ρ g·cm-3的硝酸钙溶液里含2g Ca2+ , 则NO3-的物质的量浓度 ( )
A . 2ρ mol·L-1
B . 2.5ρ mol·L-1
C . 0.5ρ mol·L-1
D . 0.002ρ mol·L-1
下列实验结果不能作为相应原理、定律或理论的证据之一的是(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)( )
| A | B | C | D | |
| 勒夏特列原理 | 盖斯定律 | 电离理论 | 阿伏加德罗定律 | |
| 实验方案 | | | | |
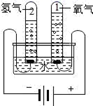
| 结果 | 该平衡体系加压后颜色变深 | 测得: ΔH = ΔH1 + ΔH2 | 产生Na+和Cl- | H2和O2的体积比约为2:1 |
A . A
B . B
C . C
D . D
设NA为阿伏加德罗常数的值,则下列关于C2H2(g)+ 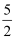 O2(g)=2CO2(g)+H2O(l) ΔH=-1300 kJ·mol-1的说法正确的是( )
O2(g)=2CO2(g)+H2O(l) ΔH=-1300 kJ·mol-1的说法正确的是( )
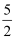 O2(g)=2CO2(g)+H2O(l) ΔH=-1300 kJ·mol-1的说法正确的是( )
O2(g)=2CO2(g)+H2O(l) ΔH=-1300 kJ·mol-1的说法正确的是( )
A . 有10NA个电子转移时,吸收1300 kJ能量
B . 有8NA个碳氧共用电子对生成时,放出1300 kJ能量
C . 有NA个水分子生成且为液体时,吸收1300 kJ能量
D . 有2NA个碳氧双键生成时,放出1300 kJ能量
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 7.8g的苯分子里含有碳碳双键数目为0.3NA
B . 常温下pH=3的FeCl3溶液中由水电离出的H+的数目为0.001NA
C . 标准状况下,2.24LC3H6中含有共用电子对数目为0.9NA
D . 1L0.1mol⋅L-1碳酸钠溶液中含有的阴离子数目为0.1NA
同温、同压下,在3支体积相同的试管中分别充有体积比为1:1的两种气体组成的混合气体,它们是:①NO、NO2;②NO2、O2;③NH3、N2。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积大小关系正确的是( )
A . ①>②>③
B . ①>③>②
C . ②>③>①
D . ③=①>②
用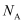 表示阿伏加德罗常数的值,下列叙述错误的是( )
表示阿伏加德罗常数的值,下列叙述错误的是( )
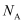 表示阿伏加德罗常数的值,下列叙述错误的是( )
表示阿伏加德罗常数的值,下列叙述错误的是( )
A . 在标准状况下,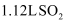 中所含原子总数为
中所含原子总数为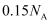 B .
B .  中含有非极性共价键的数目为
中含有非极性共价键的数目为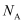 C .
C .  聚乙烯中含有碳碳双键的数目为
聚乙烯中含有碳碳双键的数目为 D .
D .  苯中含有碳碳双键的数目为
苯中含有碳碳双键的数目为
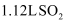 中所含原子总数为
中所含原子总数为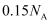 B .
B .  中含有非极性共价键的数目为
中含有非极性共价键的数目为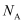 C .
C .  聚乙烯中含有碳碳双键的数目为
聚乙烯中含有碳碳双键的数目为 D .
D .  苯中含有碳碳双键的数目为
苯中含有碳碳双键的数目为
最近更新