物质的相互转化和制备 知识点题库
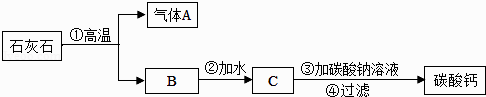
-
(1) 过滤时玻璃棒的作用是.过滤后发现滤液浑浊,应.
-
(2) 写出步骤②的化学方程式.该反应是(填“放热”或“吸热”)反应.
-
(3) 乙同学设计了一种实验方案:
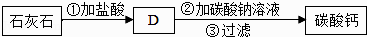
请你写出乙同学实验方案的一个优点:.
![]()
下列说法正确的是( )
流程一:从只含有CuSO4的废液中回收金属铜,并得到工业原料硫酸亚铁,生产流程如图2所示: 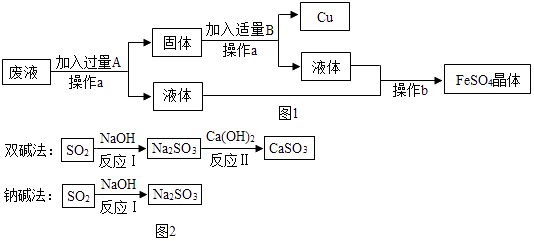
-
(1) 加入过量的A物质,该A物质为.操作a的名称是,操作a所用到的玻璃仪器有烧杯、玻璃棒,操作a中玻璃棒的作用是.
-
(2) 写出流程图中的固体成分的化学式,B的溶液中溶质的化学式
-
(3) 流程二:如图2是两种常用脱硫工艺中含硫物质的转化路径(部分产物已略),请回答下列问题:
①CaSO3中Ca、S、O元素的质量比是.
②已知原料NaOH的价格为2.9元/kg.而Ca(OH)2的价格为0.36元/kg.两种工艺中,处理相同质量的SO2 , 双碱法所需的原料成本更低,其原因是.
①C→CO→CO2 ②Cu→CuO→CuSO4 ③NaOH→Na2CO3→NaCl ④CaCO3→CaO→Ca(OH)2 .
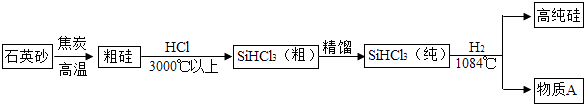
【资料】①石英砂的主要成分是SiO2②生产过程中涉及到的反应均为置换反应
-
(1) SiO2中Si的化合价是.
-
(2) 从SiHCl3(纯)得到高纯硅的化学方程式是.
-
(3) 生产过程中可循环使用的物质是.
-
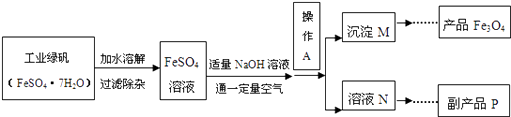
(1) 加水溶解过程中,实验室通常使用的玻璃仪器有烧杯和 ,操作A的名称是。
-
(2) 副产品P的名称是,由溶液N获得该副产品的操作顺序是(用编号填写)b→ 。
a.过滤 b.加热浓缩 c.冷却结晶

已知:BaCl2 + MgSO4 = BaSO4↓+ MgCl2
Ca(OH)2 + MgCl2 = Mg(OH)2↓+ CaCl2
Ca(OH)2 + FeCl3 = Fe(OH)3↓+ CaCl2
-
(1) 氧化铁与盐酸反应的化学方程式为。
-
(2) 滤液1中的溶质有HCl、FeCl3、MgSO4和。
-
(3) 滤液2中加入Ca(OH)2是为了除去 (填序号,下同)。A . MgCl2 B . FeCl3 C . HCl
-
(4) 滤液3呈碱性,为使溶液pH降低,可加入适量的 。A . NaCl B . NaOH C . 盐酸
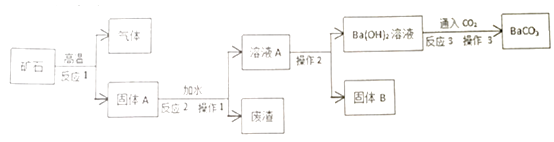
已知,氢氧化钡和氢氧化钙在不同温度下的溶解度是:
温度/℃ | 0 | 40 | 80 |
氢氧化钡溶解度/g | 1.67 | 8.22 | 101.4 |
氢氧化钙溶解度/g | 0.187 | 0.141 | 0.094 |
请回答
-
(1) 碳酸钡与碳酸钙的化学性质相似,高温下能分解成两种氧化物,碳酸钡在高温下分解的化学方程式为。
-
(2) 氧化钡与氧化钙的化学性质相似,能与水反应。溶液A中存在的阳离子是(写离子符号)。
-
(3) 在实验室里完成操作1,需要用到的玻璃仪器除漏斗、玻璃棒外,还有。
-
(4) 操作2采用的操作方法依次为____________(填序号)。A . 过滤 B . 降温 C . 加热 D . 蒸馏 E . 灼烧
-
(5) 反应3的化学方程式为。
-
(6) 废渣要经过洗涤后才能弃渣,原因是。
-
(7) 假设该碳酸盐矿石中含有40%的碳酸钙,那么50kg该矿石理论上可制得氢氧化钙的质量是kg。
-
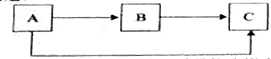
(1) 若A为黑色固体,A、B、C的相对分子质量依次增大,目B与C是组成元素相同的两种气体,则C的化学式为;B→C的反应类型(填“一定”或“不一定”)是化合反应。
-
(2) 若A、B、C均为碱,且C为白色沉淀,写出A→B反应的化学方程式:。
-
(3) 若A、B、C是三种不同类别的物质,都含有同一种元素,且组成元素分别为三种、两种和一种,常温下C为气态,则B的化学式为。
 “
“  ”表示反应一步实现,部分反应物和反应条件略去
”表示反应一步实现,部分反应物和反应条件略去  ,甲为固体单质,丙到乙的反应是吸收热量的。则甲的化学式为,丙到乙的化学方程式为,乙和丙化学性质不同的原因是
,甲为固体单质,丙到乙的反应是吸收热量的。则甲的化学式为,丙到乙的化学方程式为,乙和丙化学性质不同的原因是 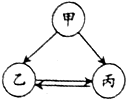
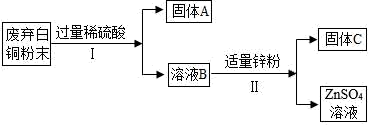
已知:Ni与Fe化学性质相似,常见化合价为+2价。
-
(1) 固体A的化学式是;
-
(2) Ⅱ中反应的化学方程式有:、;
-
(3) Ⅱ中分离出固体C的操作名称是;
-
(4) 由上述流程得出Cu、Ni、Zn的金属活动性由强到弱的顺序是。
-
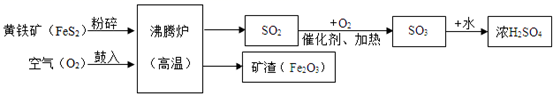
(1) 写出流程图中一种氧化物的名称。
-
(2) 将黄铁矿粉碎,目的是。
-
(3) 请写出黄铁矿在沸腾炉里发生的化学反应方程式。该反应中的(填元素符号)从反应前到反应后化合价升高。
-
(4) 该生产流程的炉渣可以做工业炼铁的原料,请写出工业炼铁反应化学方程式。此外古代记载的湿法冶金技术有“曾青得铁则化为铜”,写出有关化学方程式。
-
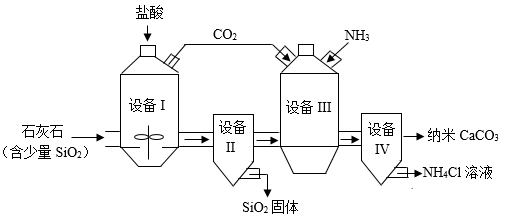
(1) 设备Ⅰ中需不断搅拌,其目的是。设备Ⅰ中发生反应的化学方程式为。
-
(2) 设备Ⅱ和设备Ⅳ均为分离设备,设备Ⅳ中的分离操作是。
-
(3) 设备Ⅲ中参加反应的物质除水外,还有。
-
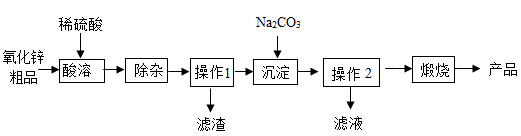
(1) “酸溶”时所用稀硫酸的质量分数为10%。则配制200g 10%的H2SO4溶液需要在80%的H2SO4溶液中加水g。
-
(2) 写出“酸溶”时氧化锌和稀硫酸反应的化学方程式。
-
(3) “酸溶”后溶液含有Zn2+、
 ,另含有Fe2+、Fe3+、Cu2+等杂质。
,另含有Fe2+、Fe3+、Cu2+等杂质。 ①除铁时需加入H2O2 , 将Fe2+转化Fe3+ , 最终生成Fe(OH)3沉淀,离子间的反应关系为:2Fe2++2H++H2O2=2Fe3++2H2O,该反应中化合价降低的是(填元素名称)元素。
②加入足量的锌粉,可以回收金属,所发生化学反应的类型为反应。
-
(4) 操作1、2中均需要用到玻璃仪器有烧杯、玻璃棒和。
-
(5) 进入“煅烧”工艺的物质是ZnCO3·2Zn(OH)2·H2O,该物质经过煅烧后生成了三种氧化物,除了ZnO和H2O以外,还有一种是。
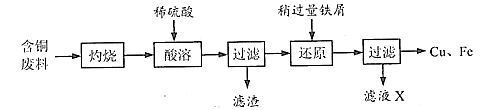
注:灼烧后得到黑色固体和残留物,残留物不溶于水和稀硫酸。
下列关于该流程的说法,错误的是( )
-
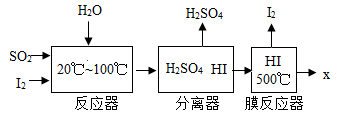
(1) 写出反应器中发生化学反应的方程式。
-
(2) 反应器中S元素的化合价变化为+4→。
-
(3) 膜反应器中发生的是分解反应,则X的化学式是。
①CH4→O2 ②HCl→HNO3 ③CO→Na2CO3 ④Ba(OH)2→NaOH ⑤CO→Fe
-
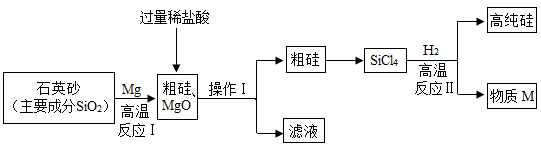
(1) SiO2中硅元素的化合价。
-
(2) 操作I:操作名称是。
-
(3) 反应Ⅱ:发生反应的化学方程式为。该反应要在无氧气的环境中进行,原因是(答出一种即可)。
-
(4) 上述已知生产流程中,可以循环利用的物质是(填化学式)。