合成氨条件的选择 知识点题库
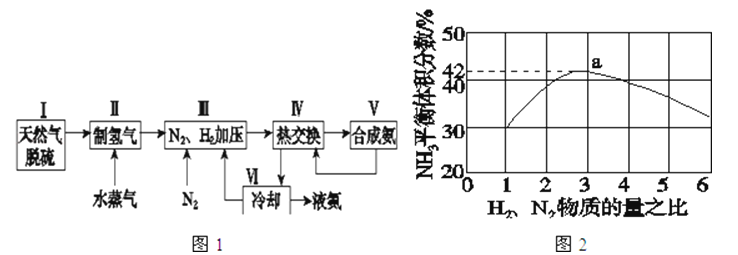
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS.一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式:
(2)步骤Ⅱ中制氢气的原理如下:
①CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.4 kJ•mol﹣1
②CO(g)+H2O(g)═CO2(g)+H2(g)△H=﹣41.2kJ•mol﹣1
对于反应①,一定可以提高平衡体系中H2的百分含量,又能加快反应速率的措施是 (填序号)
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
利用反应②,将CO进一步转化,可提高H2的产量.若1mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18mol CO、CO2和H2的混合气体,则CO的转化率为
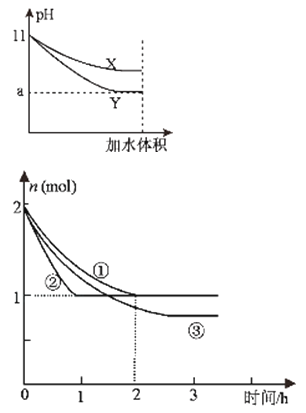
(3)图2表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系.根据图中a点数据计算N2的平衡体积分数:
(4)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号) 简述本流程中提高合成氨原料总转化率的方法
请回答下列问题:
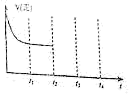
(1)与①比较,②和③分别仅改变一种反应条件.所改变的条件是:② ;③
(2)实验①的平衡常数K= (用最简分数表示),该反应进行到2h时的平均反应速率v(H2)=
(3)氨是工业合成尿素(H2NCONH2)的重要原料,工业上合成尿素的反应分为如下两步:
第1步:2NH3(l)+CO2(g)═H2NCOONH4(氨基甲酸铵)(l)△H1=﹣330.0kJ•mol﹣1
第2步:H2NCOONH4(l)═H2O(l)+H2NCONH2(l)△H2=+226.0kJ•mol﹣1
则2NH3(l)+CO2(g)═H2O(l)+H2NCONH2 (l)△H=
(4)工业上利用反应 3Cl2+2NH3═N2+6HCl检查氯气管道是否漏气.当转移6mol 电子时,生成氮气在标准状况下的体积是 L.
(5)相同pH的氨水和NaOH溶液加水稀释相同的倍数,pH变化曲线如图所示,则x曲线代表的物质是 , 当a=9时,稀释后溶液的体积是稀释前溶液体积的 倍.

(1)步骤Ⅱ中制氢气原理如下:
CH4(g)+H2O(g)⇌CO(g)+3H2(g) CO(g)+H2O(g)⇌CO2(g)+H2(g)
恒容容器中,对于以上两个反应,能加快反应速率的是
a.升高温度 b.充入He c.加入催化剂 d.降低压强
(2)天然气中的H2S杂质常用氨水作吸收液吸收,产物为NH4HS,一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式为 ,该反应的氧化产物为
(3)为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用的研究.
①如将CO2与H2 以1:3的体积比混合. 适当条件下合成某烃和水,该烃是 (填序号).
A.烷烃 B.烯烃 C.苯
②如将CO2与H2 以1:4的体积比混合,在适当的条件下可制得CH4 .
已知:CH4 (g)+2O2(g)═CO2(g)+2H2O(l)△H1=﹣890.3kJ/mol
H2(g)+ O2(g)═H2O(l)△H2=﹣285.8kJ/mol
O2(g)═H2O(l)△H2=﹣285.8kJ/mol
则CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式是
③已知CaCO3和BaCO3均为难溶于水的沉淀,某同学欲用沉淀法测定含有较高浓度CO2的空气中CO2的含量,经查得Ca(OH)2和 Ba(OH)2在20℃时的溶解度(S)数据如下:Ca(OH)2:0.16g; Ba(OH)2:3.89g
则吸收CO2最合适的试剂是 (填“Ca(OH)2”或“Ba(OH)2”)溶液,实验时除需要测定工业废气的体积(折算成标准状况)外,还需要测定 .
(4)已知CO2+2NH3 CO(NH2)2+H2O,若合成尿素CO(NH2)2的流程中转化率为80%时,100吨甲烷为原料能够合成 吨尿素.
CO(NH2)2+H2O,若合成尿素CO(NH2)2的流程中转化率为80%时,100吨甲烷为原料能够合成 吨尿素.
-
(1) 当反应达到平衡时,N2和H2的浓度比是;N2和H2的转化率比是.反应放出的热量(填“大于”“小于”或“等于”)184.8 kJ。
-
(2) 降低平衡体系的温度(保持体积不变),混合气体的平均相对分子质量,密度.平衡常数K(填“增大”“减小”或“不变”).
-
(3) 当达到平衡时,充入氩气,并保持压强不变,平衡将(填“正向”“逆向”或“不”)移动.
-
(4) 若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将(填“向左移动”“向右移动”或“不移动”).达到新平衡后,容器内温度(填“大于”“小于”或“等于”)原来的2倍。
-
(1) 合成氨反应中使用的催化剂是(填名称),该反应温度一般控制在500℃,主要原因是。
-
(2) 下列措施,既能加快合成氨反应的反应速率,又能增大反应物转化率的是(_____)A . 使用催化剂 B . 缩小容积体积 C . 提高反应温度 D . 移走NH3
-
(3) 在t2时刻,将容器的容积迅速扩大到原来的2倍,在其他条件下不变的情况下,t3时刻达到新的平衡状态,之后不再改变条件。请在下图中补充画出从t2到t4时刻正反应速率随时间的变化曲线。
-
(4) 常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是(________)A . 溶液的pH增大 B . 氨水的电离程度减小 C . c(NH4+)减小 D . c(OH-)减小
-
(5) 石蕊(用HZ表示)试液中存在的电离平衡HZ(红色) H+ + Z-(蓝色)。通入氨气后石蕊试液呈蓝色,请用平衡移动原理解释。
 达平衡时,缩小容器体积再达平衡时,气体的颜色比第一次平衡时的深,NO2的体积分数比原平衡大
C . 常温下,
达平衡时,缩小容器体积再达平衡时,气体的颜色比第一次平衡时的深,NO2的体积分数比原平衡大
C . 常温下,  不能自发进行,则其
不能自发进行,则其 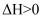 D . 在相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH-)相等
D . 在相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH-)相等
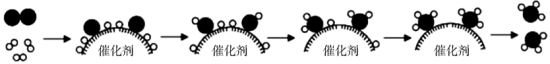
下列说法正确的是( )
 表示氢气分子
B . 过程中有“NH”“NH2”原子团生成
C . 催化剂增大了氢气的平衡转化率
D . 反应结束后催化剂的质量增加
表示氢气分子
B . 过程中有“NH”“NH2”原子团生成
C . 催化剂增大了氢气的平衡转化率
D . 反应结束后催化剂的质量增加

 2NH3(g),673K、30MPa下,n(NH3)和n(H2)随时间的变化关系如图所示。下列说法正确的是( )
2NH3(g),673K、30MPa下,n(NH3)和n(H2)随时间的变化关系如图所示。下列说法正确的是( )
 ]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
-
(1) Shibata曾做过下列实验:①使纯H2缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴(Co),平衡后气体中H2的物质的量分数为0.0250。
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是COH2(填“大于”或“小于”)。
-
(2) 721 ℃时,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H2的物质的量分数为( )A . <0.25 B . 0.25 C . 0.25~0.50 D . 0.50 E . >0.50
-
(3) 我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。

可知水煤气变换的ΔH0(填“大于”“等于”或“小于”),该历程中最大能垒(活化能)E正=eV,写出该步骤的化学方程式。
-
(4) Shoichi研究了467 ℃、489 ℃时水煤气变换中CO和H2分压随时间变化关系(如下图所示),催化剂为氧化铁,实验初始时体系中的
 和
和 相等、
相等、 和
和 相等。
相等。
计算曲线a的反应在30~90 min内的平均速率
 =
= 。467 ℃时
。467 ℃时 和
和 随时间变化关系的曲线分别是、。489℃时
随时间变化关系的曲线分别是、。489℃时 和
和 随时间变化关系的曲线分别是、。
随时间变化关系的曲线分别是、。
-
(1) I.工业上用
 和
和 在一定条件下合成氨,下列措施能使正反应速率增大,且平衡混合物中
在一定条件下合成氨,下列措施能使正反应速率增大,且平衡混合物中 的体积分数—定增大的是( )。
A . 降低反应温度 B . 压缩反应混合物 C . 充入
的体积分数—定增大的是( )。
A . 降低反应温度 B . 压缩反应混合物 C . 充入 D . 液化分离
D . 液化分离
-
(2) 常温下,向100mL0.2mol/L,的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中
 和
和 物质的量分数与加入盐酸的体积的关系如图所示,根据图像回答下列问题。
物质的量分数与加入盐酸的体积的关系如图所示,根据图像回答下列问题。 
①表示
 浓度变化的曲线是(填“A”或“B”)。
浓度变化的曲线是(填“A”或“B”)。②
 的电离常数为(已知lg1.8=0.26)。
的电离常数为(已知lg1.8=0.26)。③当加入盐酸体积为50mL,溶液中
 =mol/L(用数字表示)。
=mol/L(用数字表示)。 -
(3) II.若液氨中也存在类似水的电离(
 ),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。 写出液氨的电离方程式:。
-
(4) 写出碳酸钠溶于液氨后一级氨解的离子方程式:。
-
(5) 写出碳酸钠的液氨溶液中各离子浓度的大小关系:。

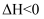 。下列分析错误的是( )
。下列分析错误的是( )
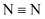 键能大,断开该键需要较多能量
B . 增大合成氨的反应速率与提高平衡混合物中氨的含量所采取的措施均一致
C . 平衡混合物中
键能大,断开该键需要较多能量
B . 增大合成氨的反应速率与提高平衡混合物中氨的含量所采取的措施均一致
C . 平衡混合物中 的沸点最高,液化、分离出
的沸点最高,液化、分离出 能提高其产率
D . 断裂1
能提高其产率
D . 断裂1
 和3
和3
 的共价键所需能量小于断裂2
的共价键所需能量小于断裂2
 的共价键所需能量
的共价键所需能量
-
(1) 工业合成氨反应
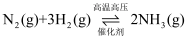 是放热的可逆反应。已知1mol高温高压N2(g)完全反应生成
是放热的可逆反应。已知1mol高温高压N2(g)完全反应生成 (g)可放出92kJ热量。如果将0.5mol
(g)可放出92kJ热量。如果将0.5mol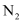 (g)和足量
(g)和足量 (g)混合,使其充分反应,放出的热量(填“大于”“小于”或“等于”)46kJ。
(g)混合,使其充分反应,放出的热量(填“大于”“小于”或“等于”)46kJ。
-
(2) 在容积为5L的密闭容器内模拟工业合成氨,反应经过5min后,生成10mol

①用
 表示的化学反应速率为
表示的化学反应速率为
②一定条件下,能说明该反应进行到最大限度的是。
a.
 的转化率达到最大值
的转化率达到最大值b.
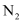 、
、 和
和 的分子数之比为
的分子数之比为
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
-
(3) 某实验小组进行如图甲所示实验。请判断b中的温度(填“升高”或“降低”)。反应过程(填“a”或“b”)的能量变化可用图乙表示。

-
(4) 用
 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图: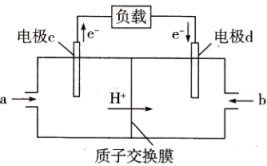
①电极c是(填“正极”或“负极”),电极d的电极反应式为。
②若线路中转移1mol电子,则该燃料电池理论上消耗的
 在标准状况下的体积为L。
在标准状况下的体积为L。
 2NH3 ΔH<0,一定温度下,在恒容的密闭容器中加入 1 mol N2和 3 mol H2合成 NH3。下列有关说法正确的是( )
2NH3 ΔH<0,一定温度下,在恒容的密闭容器中加入 1 mol N2和 3 mol H2合成 NH3。下列有关说法正确的是( )
 的含量
C . 降低
的含量
C . 降低 的沸点
D . 提高
的沸点
D . 提高 和
和 的利用率
的利用率
-
(1) 氨催化氧化法是制硝酸的重要步骤,探究氨催化氧化反应的装置如图所示:

①氨催化氧化时会生成副产物N2O。生成含等物质的量氮元素的NO与N2O时,消耗的O2的物质的量之比为。
②一段时间后,观察到装置M中有白烟生成,该白烟成分是(写化学式)。
③再经过一段时间观察到装置N中溶液变成蓝色,装置N中溶液变成蓝色的原因是。
-
(2) 可用ClO2将氮氧化物转化成NO
 。向1 L含200 mg ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2 , 再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为。
。向1 L含200 mg ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2 , 再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为。
-
(3) 纳米铁粉可去除水中的NO
 。控制其他条件不变,用纳米铁粉还原水体中的NO
。控制其他条件不变,用纳米铁粉还原水体中的NO , 测得溶液中含氮物质(NO
, 测得溶液中含氮物质(NO 、NO
、NO 、NH
、NH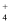 )浓度随时间变化如图所示:
)浓度随时间变化如图所示:
①Fe去除水中的NO
 的机理:NO
的机理:NO 得到纳米铁粉失去的电子转化为NO
得到纳米铁粉失去的电子转化为NO , 极少量NO
, 极少量NO 在纳米铁粉或Cu表面得到电子转化为NH
在纳米铁粉或Cu表面得到电子转化为NH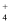 。与不添加少量铜粉相比,添加少量铜粉时去除NO
。与不添加少量铜粉相比,添加少量铜粉时去除NO 效率更高,主要原因是。
效率更高,主要原因是。②与初始溶液中NO
 浓度相比,反应后溶液中所有含氮物质(NO
浓度相比,反应后溶液中所有含氮物质(NO 、NO
、NO 、NH
、NH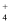 )总浓度减小,原因是。
)总浓度减小,原因是。
 , 其能量变化如图所示,下列说法错误的是( )
, 其能量变化如图所示,下列说法错误的是( )
 的完全转化
C . 增大
的完全转化
C . 增大 的浓度,反应速率增大
D . 断开反应物中的化学键吸收的总能量小于形成生成物中的化学键放出的总能量
的浓度,反应速率增大
D . 断开反应物中的化学键吸收的总能量小于形成生成物中的化学键放出的总能量



