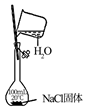气体发生装置的气密性检查 知识点题库
正确的实验操作是实验成功的基本保证。下列实验操作正确的是
SO2是大气污染物之一,为粗略地测定周围环境中SO2的含量,某学生课外活动小组设计了如图所示的实验装置.检验该装置的气密性,先在试管中装入适量的水(保证玻璃导管的下端末在水中),然后(填操作方法) 将会看到(填现象) .则证明该装置气密性良好.
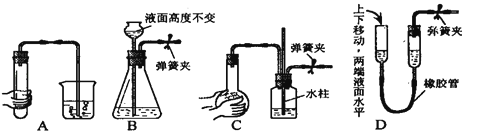
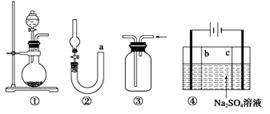
(Ⅰ)气体制备时须先检查装置的气密性,下列各图所示装置,肯定不符合气密性检查要求的是 .
(Ⅱ)下面是中学化学实验中常见的几种仪器:
a.量筒 b.容量瓶 c.分液漏斗 d.托盘天平 e.温度计
(1)其中标示出仪器使用温度的是 (填编号).
(2)称取10.5g固体样品(1g以下使用游码)时,将样品放在了天平的右盘,则所称样品的实际质量为 g.
(3)使用前要检查仪器是否漏液的是 (填编号).
(Ⅲ)实验室需要95mL 1.0mol•L﹣1稀硫酸,现用98%的浓硫酸(其密度为1.84g/mL)来进行配制.若实验仪器有:
A.100mL量筒 B.托盘天平 C.玻璃棒 D.250mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
(1)需量取浓硫酸的体积为 mL.
(2)实验时选用的仪器有(填序号)
(3)配制过程中,下列情况会使配制结果偏高的是(填序号)
A.将稀释的硫酸液转移至容量瓶后,未洗涤烧杯和玻璃棒.
B.将烧杯内的稀硫酸向容量瓶中转移时,因操作不当使部分稀硫酸溅出瓶外.
C.未冷却至室温就定容.
D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切.
E.容量瓶使用时未干燥
F.定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线.
 检查装置气密性
B .
检查装置气密性
B .  实验室制氨气
C .
实验室制氨气
C . 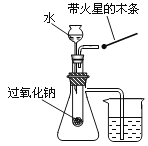 验证过氧化钠与水反应既生成氧气又放热
D .
验证过氧化钠与水反应既生成氧气又放热
D . 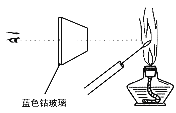 检验K2CO3中的K+
检验K2CO3中的K+

B .
B . 
C .
C . 
D .
D . 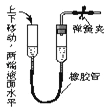

-
(1) 请将下列步骤补充完整并回答下列问题:
①配制浓度均为1mol/L的盐酸和醋酸溶液;
②用量取10.00mL 1mol/L的盐酸和醋酸溶液分别加入两个锥形瓶中;
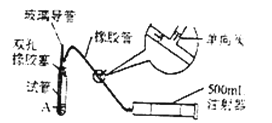
③分别称取除去表面氧化膜的镁带a g,并系于铜丝末端,a的数值至少为;
④在广口瓶中装足量的水,按图连接好装置;检查装置的气密性;
⑤将铜丝向下移动,使足量镁带浸入酸中(铜丝不与酸接触),至反应完全,记录;
⑥反应结束后待温度恢复到室温,若丙中液面高于乙中液面,读取量筒中水的体积前,应,读出量筒中水的体积为V mL.
-
(2) 用文字表述④检查该装置气密性的操作与观察方法:.
-
(3) 本实验中应选用 (填序号)的量筒.A . 100mL B . 200mL C . 500mL
-
(4) 若水蒸气的影响忽略不计,在实验室条件下,气体摩尔体积的计算式为Vm=.
-
(5) 速率不等的原因是,铜丝不与酸接触的原因是.
 倾倒液体
B .
倾倒液体
B .  检查气密性
C .
检查气密性
C . 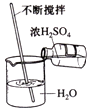 稀释浓硫酸
D .
稀释浓硫酸
D .  取用固体
取用固体
-
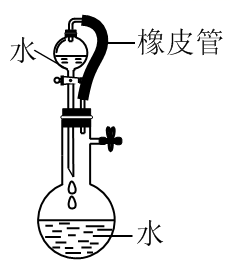
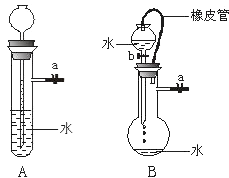
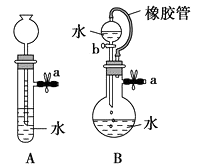
(1) 关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示.试判断:A装置是否漏气?(填“漏气”、“不漏气”或“无法确定”),判断理由:.
-
(2) 关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶.试判断:B装置是否漏气?(填“漏气”、“不漏气”或“无法确定”),判断理由:.

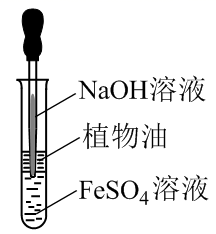
 比较Cl2、Fe3+、I2的氧化性
B .
比较Cl2、Fe3+、I2的氧化性
B . 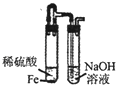 制取Fe(OH)2
C .
制取Fe(OH)2
C . 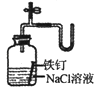 证明铁生锈时空气参加反应
D .
证明铁生锈时空气参加反应
D .  检查装置气密性
检查装置气密性
-
(1) 关闭图A装置中的止水夹a后,从长颈漏斗向试管口注入一定量的水,静置后如图所示。试判断:A装置是否漏气?(填“漏气”、“不漏气”或“无法确定”),判断理由。
-
(2) 关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:B装置是否漏气?(填“漏气”、“不漏气”或“无法确定”),判断理由。

实验步骤:
a.仪器连接后,放入AgNO3固体之前,关闭K,微热硬质玻璃管A;
b.称取 AgNO3 固体1.7g 置于A中,先通一段时间N2 , 再关闭K,用酒精灯加热硬质玻璃管A;
c.待样品完全分解,装置A冷却至室温,称量,测得剩余固体的质量为1.08 g。
请回答下列问题:
-
(1) 使用酒精灯对AgNO3固体加热的操作方法是。
-
(2) 步骤a的操作目的是。
-
(3) 步骤b中先通一段时间的N2的目的是。
-
(4) 装置C瓶中盛装的药品名称为(合理即可),装置D中可观察到的实验现象为。
-
(5) 根据实验现象和称量结果,请写出该装置中AgNO3固体受热分解的化学方程式。
-
(6) 从实验安全角度考虑该装置存在缺陷,应如何改进?。
 TiBr4+CO2制备TiBr4的装置如图所示。回答下列问题:
TiBr4+CO2制备TiBr4的装置如图所示。回答下列问题: 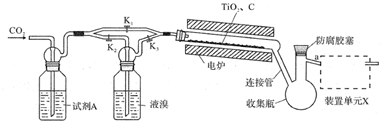
-
(1) 检查装置气密性并加入药品后,加热前应进行的操作是,其目的是,此时活塞K1 , K2 , K3的状态为;一段时间后,打开电炉并加热反应管,此时活塞K1 , K2 , K3的状态为。
-
(2) 试剂A为,装置单元X的作用是;反应过程中需用热源间歇性微热连接管,其目的是。
-
(3) 反应结束后应继续通入一段时间CO2 , 主要目的是。
-
(4) 将连接管切断并熔封,采用蒸馏法提纯。此时应将a端的仪器改装为、承接管和接收瓶,在防腐胶塞上加装的仪器是(填仪器名称)。
-
(1) Ⅰ.某科学探究小组设计以下装置依次完成氯气的制备、氯酸钠的制备、次氯酸钠的制备并探究氯水的性质。
其中:①为氯气发生装置,烧瓶中盛放 MnO2 固体;
②的试管里盛有 15 mL 30% NaOH 溶液,并置于热水浴中;
③的试管里盛有 15 mL 8% NaOH 溶液,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置。
请填写下列空白:

如何检验装置①的气密性。
-
(2) 如果实验室没有 MnO2 , 下列物质可以用来代替 MnO2制 Cl2的是__A . KMnO4 B . Fe2O3 C . 浓硫酸 D . KClO3
-
(3) 制备氯酸钠的化学方程式为 。
-
(4) 比较制取氯酸钠和次氯酸钠的条件,二者的差异是:。
-
(5) ④的试管里紫色石蕊试液现象及原因 。
-
(6) Ⅱ.次氯酸钠溶液可以杀灭新冠病毒,若将其与稀硫酸混合使用可增强消毒能力。现用18mol·L-1 浓硫酸来配制 450 mL 0.2 mol·L-1 的稀硫酸。
①需用量筒量取浓硫酸的体积为mL。
②定容时的操作:当液面离容量瓶颈部的刻度线 1~2cm 时, ,盖好瓶塞,反复上下颠倒,摇匀。
③若所配制的稀硫酸浓度偏高,则下列可能的原因分析中正确的是。
A.配制前,容量瓶用蒸馏水洗涤后再用硫酸润洗
B.量取浓硫酸时,读数时俯视液体的凹液面
C.浓硫酸稀释后立即转移至容量瓶定容
D.颠倒摇匀后,液面低于刻度线,继续滴加蒸馏水
| 选项 | A | B | C | D |
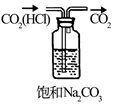
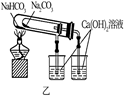
| 实验目的 | 除去CO2中的HCl | 证明下列装置气密性良好 | 比较Na2CO3和NaHCO3的热稳定性 | 配置100mL 0.1mol/LNaCl溶液 |
| 实验内容 | | | | |
选项 | A | B | C | D |
实验操作 |
|
|
|
|
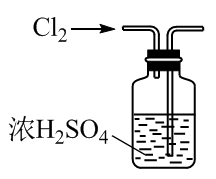
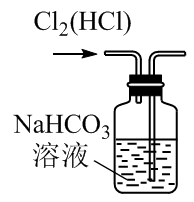
目的 | 证明该装置气密性良好 | 观察Fe(OH)2的生成 | 干燥Cl2 | 除去Cl2中的少量HCl |
 又名“大苏打”“海波”,易溶于水,难溶于乙醇,水溶液呈微弱的碱性,在中性和碱性环境中稳定。某化学实验小组用如图1装置(略去对乙的加热装置)制备
又名“大苏打”“海波”,易溶于水,难溶于乙醇,水溶液呈微弱的碱性,在中性和碱性环境中稳定。某化学实验小组用如图1装置(略去对乙的加热装置)制备 , 已知:
, 已知: 溶解度如图2所示。
溶解度如图2所示。
-
(1) 连接实验装置后,首先进行的实验操作为。
-
(2) 在装置乙中溶解两种固体时,需先将
 溶于水配成溶液,再将
溶于水配成溶液,再将 固体溶于
固体溶于 的溶液中,其目的;装置乙中生成
的溶液中,其目的;装置乙中生成 的总反应方程式为。
的总反应方程式为。
-
(3) 实验过程中,当装置乙中
 接近7.0时,应立即停止通
接近7.0时,应立即停止通 的原因是(用离子方程式表示)。
的原因是(用离子方程式表示)。
-
(4) 装置乙中需向反应后的混合液加入一定量的无水乙醇,其目的是。
-
(5) 设计实验测定
 的纯度:
的纯度:步骤1:准确称取
 样品,溶于水,加入
样品,溶于水,加入 甲醛,配成
甲醛,配成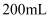 溶液。
溶液。步骤2:准确称取
 于碘量瓶中,加入
于碘量瓶中,加入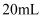 蒸馏水溶解,再加入
蒸馏水溶解,再加入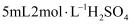 和
和 溶液使铬元素完全转化为
溶液使铬元素完全转化为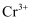 , 加水稀释至
, 加水稀释至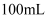 。
。步骤3:向碘量瓶中加入
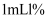 淀粉溶液,用待测
淀粉溶液,用待测 溶液滴定碘量瓶中溶液至终点,消耗
溶液滴定碘量瓶中溶液至终点,消耗 溶液
溶液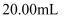 。(已知:
。(已知: )
)试计算
 的纯度为(保留三位有效数字)。
的纯度为(保留三位有效数字)。 -
(6) 利用甲装置中的残渣(
 和
和 的混合物)制备
的混合物)制备 晶体,将下列实验方案补充完整:将固体混合物溶于水配成溶液,,洗涤、干燥得
晶体,将下列实验方案补充完整:将固体混合物溶于水配成溶液,,洗涤、干燥得 晶体。(实验中须使用氧气、
晶体。(实验中须使用氧气、 计)
计)
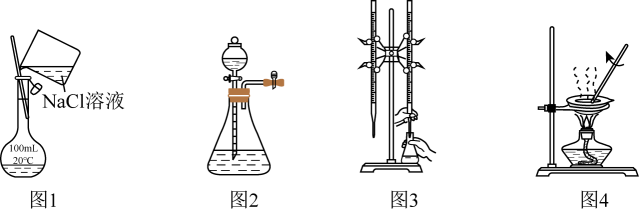
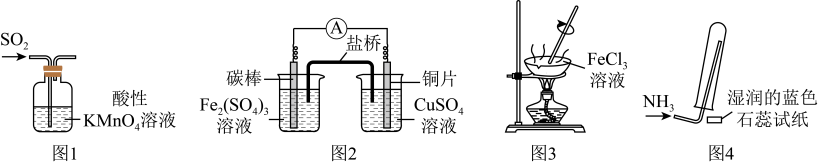
 的漂白性
B . 图2装置可验证氧化性:
的漂白性
B . 图2装置可验证氧化性: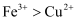 C . 图3装置可制备无水
C . 图3装置可制备无水 D . 图4装置可验证氨水呈碱性
D . 图4装置可验证氨水呈碱性