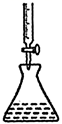气体发生装置的气密性检查 知识点题库
-
(1)
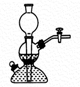
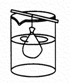
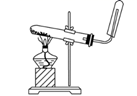
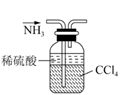
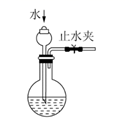
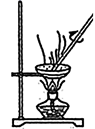
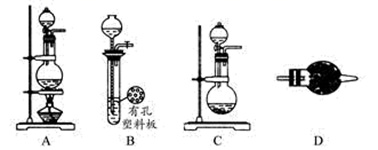
如图所示装置的气密性检查中,漏气的是
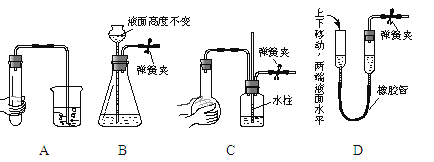
-
(2)
下列对实验仪器名称的标注或实验操作,正确的是

-
(3) 下列说法中,完全正确的一组是 .
①用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部
②给盛有液体的体积超过
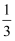 的试管加热至沸腾
的试管加热至沸腾③等体积的浓氨水与蒸馏水混合后的溶液,其中氨水的溶质质量分数一定等于稀释前的一半
④将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管
⑤硝酸、溴水可长期盛放在棕色的滴瓶中
⑥将烧瓶放在桌上,再用力塞进塞子
⑦熔融氢氧化钠要在耐高温的石英坩埚中
⑧将滴管垂直伸进试管内滴加液体
A.①④B.①④⑤⑦C.②③⑤⑥D.①②③④⑤⑥⑦⑧
(1)实验室加热法制氧气:
(2)氢气还原氧化铜实验:
(3)用天平称量固体药品:
(4)用分液漏斗进行分液操作:
如图各图所示装置的气密性检查中,漏气的是

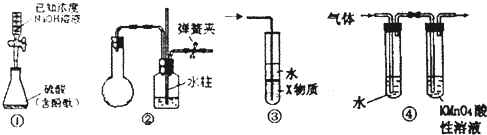
②实验室在用制氢气的简易装置制取氢气前如何检查装置的气密性?简述操作步骤?.
①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为ag。
②装好实验装置。
③检查装置气密性。
④加热,开始反应,直到产生一定量的气体。
⑤停止加热(如图所示,导管出口高于液面)。
⑥测量收集到的气体的体积。
⑦准确称量试管和残留物的质量为b g。
⑧测 量实验室的温度。
⑨把残留物倒入指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净。
⑩处理实验数据,求出氧气的摩尔质量。
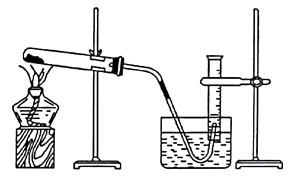
回答下列问题:
-
(1) 如何检查装置的气密性?
-
(2) 以下是测量收集到的气体体积必须包括的几个步骤:
①调整量筒内外液面高度使之相同;②使试管和量筒内的气体都冷却至室温;③读取量筒内气体的体积。这三步操作的正确顺序是(请填写步骤代号)
-
(3) 如果实验中得到的氧气体积是cL(已换算为标准状况),水蒸气的影响忽略不计,氧气的摩尔质量的计算式为(含a、b、c,不必化简)M(O2)=
 橡皮管能使液体顺利留下
B .
橡皮管能使液体顺利留下
B . 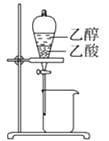 分离乙醇和乙酸
C .
分离乙醇和乙酸
C . 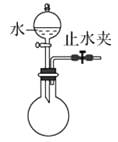 检查装置气密性
D .
检查装置气密性
D . 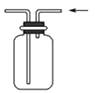 收集氨气
收集氨气
| A | B | C | D |
| | | | |
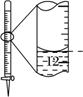
| 向该装置中加入金属Zn和稀硫酸,并关闭活塞,用于检查装置的气密性 | 记录滴定终点读数为12.20mL | 灼烧胆矾晶体使其分解 | 分离含淀粉和葡萄糖的溶液 |
-
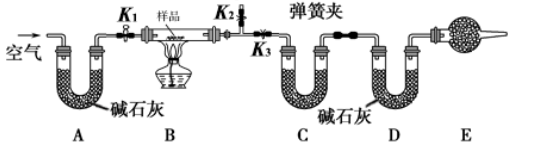
(1) 请将实验步骤补充完整
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是 。
②称取样品,并将其放入硬质玻璃管中;并称量C、D装置的质量。
③打开活塞K1和K2 , 关闭K3 , 缓慢鼓入空气数分钟,其目的是。
④关闭活塞K1和K2 , 打开K3 , 点燃酒精灯加热至不再产生气体。
⑤打开活塞K1 , 缓缓鼓入空气数分钟,然后卸下装置,再次称量C、D装置的质量。
-
(2) 关于该实验方案,请回答下列问题:
①若加热反应后不鼓入空气,对NaCl测定结果的影响是(“偏高”、“偏低”或“无影响”)
②E处干燥管中盛放的药品是,其作用是,如果实验中没有该装置,则会导致测量结果NaHCO3的质量分数(“偏高”、“偏低”或“无影响”)
③若样品质量为wg,反应后C、D装置增加的质量分别为m1g和m2g,由此可知混合物中Na2CO3·10H2O的质量分数为(用含w、m1、m2的代数式表示)。
【操作流程】 安装吸收装置→PH3的产生与吸收→转移KMnO4吸收溶液→亚硫酸标准溶液滴定
【实验装置】

C中盛有200g原粮,D、E、F 各盛装1.00mL浓度为1.00×10-3mol/L的KMnO4 溶液(H2SO4 酸化)。
请回答下列有关问题:
-
(1) 仪器G的名称是。以磷化铝为例,写出磷化铝与水反应的化学方程式 。
-
(2) 检查C装置气密性的方法是:用止水夹夹紧C装置,取下上口活塞,漏斗中加入水,打开下口旋塞,观察到 ,表明装置气密性良好。
-
(3) 实验过程中,用抽气泵反复抽气的目的是 。
-
(4) A中盛装KMnO4溶液是为除去空气中可能含有的 (填“还原”或“氧化”)性气体;B中盛装新制FeSO4溶液的作用是 ;
-
(5) 已知 D、E、F 中发生同一反应,实验中 PH3被氧化成磷酸,写出所发生的化学反应方程式 ;收集装置D、E、F所得吸收液,并洗涤D、E、F,将吸收液、洗涤液一并置于锥形瓶中,加水稀释至25mL,用浓度为5×10-4 mol/LNa2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液11.00mL,则该原粮中磷化物(以PH3计)的含量
为 mg/kg。
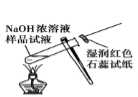 检验样品中是否含有NH4+
B .
检验样品中是否含有NH4+
B . 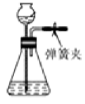 向长颈漏斗中加一定量水,并形成水柱,随后水柱下降至与瓶中液面相平,说明气密性好
C .
向长颈漏斗中加一定量水,并形成水柱,随后水柱下降至与瓶中液面相平,说明气密性好
C . 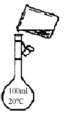 转移溶液
D .
转移溶液
D . 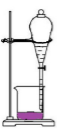 分离汽油和水
分离汽油和水
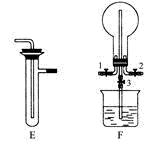
-
(1) Ⅰ.探究氯气与氨气的反应
为制取干燥氨气,可将装置C与(填装置名称)连接;装置C中的烧瓶内固体宜选用。
a.氯化钙 b.碱石灰 c.五氧化二磷 d.生石灰
-
(2) 装置A、E、E连接可制取纯净、干燥的氯气,则两个E装置内的药品依次是。
-
(3) 装置F可用于探究氯气与氨气的反应。实验时打开开关1、3,关闭2,先向烧瓶中通入(填名称),然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体。实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体中的阳离子,F的烧杯中所装液体为,所起的作用是。
-
(4) Ⅱ.探究某些物质的性质
利用装置A、E,可设计实验比较Cl-和Br-的还原性强弱。将装置A中产生的气体通入盛有NaBr溶液的装置E中,充分反应后取下E,加入CCl4 , 静置后观察到的实验现象,则证明Br-的还原性强于Cl-。
-
(5) 将装置B、C分别与F相连后,进行H2S与SO2反应的实验。简述检查装置B气密性的操作,F的烧瓶中发生反应的化学方程式为。
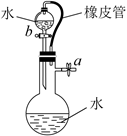 关闭a打开活塞b,通过观察水能否顺利流下来验证装置的气密性
B .
关闭a打开活塞b,通过观察水能否顺利流下来验证装置的气密性
B . 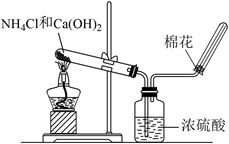 实验室制备并收集氨气
C .
实验室制备并收集氨气
C .  c管先通
c管先通  ,d管再通过量
,d管再通过量  ,可制取少量小苏打
D .
,可制取少量小苏打
D . 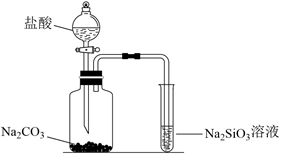 验证酸性强弱:盐酸>碳酸>硅酸
验证酸性强弱:盐酸>碳酸>硅酸
| A | B | C | D |
| | | | |
| 实验室制取并收集氨气 | 吸收氨气 | 检验装置气密性 | 利用排空气法收集氨气 |
| 选项 | A | B | C | D |
| 实验装置 | | | | |
| 实验目的 | 用NaOH标准液滴定盐酸(锥形瓶中) | 除去CO2气体中混有的HCl杂质 | 由CuSO4溶液制取胆矾 | 检查装置气密性 |
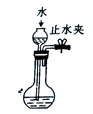 B . 吸收含Cl2的尾气
B . 吸收含Cl2的尾气 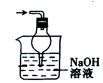 C . 分离出用H2O2制取O2后剩余的MnO2
C . 分离出用H2O2制取O2后剩余的MnO2 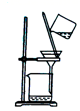 D . 量取15.00mLNaOH溶液
D . 量取15.00mLNaOH溶液 
 )溶液来处理。工业上制备过硫酸钠的原理如下:
)溶液来处理。工业上制备过硫酸钠的原理如下: 主反应: 
副反应: 
(制备  )
)

-
(1) 检查装置a气密性的方法:用止水夹夹住a、b之间的橡皮管,向分液漏斗中加水,,证明装置a气密性良好;装置a中产生的气体需要持续通入装置c中的原因是(答2点)、。
-
(2) 装置c中盛放(NH4)2S2O8溶液的仪器名称是;图中还需补充装置。
(测氰化钠的含量)
已知:①废水中氰化钠的最高排放标准为0.50 mg/L。
②
 ,
, 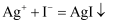 ,AgI呈黄色,
,AgI呈黄色, 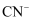 优先与
优先与  发生反应。
发生反应。实验如下:取1 L处理后的NaCN废水,浓缩为10.00 mL置于锥形瓶中,并滴加几滴KI溶液作指示剂,用0.0012 mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为3.75 mL。
-
(3) 滴定终点的现象是。
-
(4) 若用双氧水处理NaCN后,产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,该反应的化学方程式是。
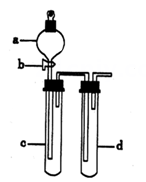
-
(1) a装置的名称为:。
-
(2) 化学实验前均需检查装置气密性,请设计一个实验检查装置甲的气密性:。
-
(3) 实验时c中放一小块铜片,由分液漏斗a向c中加入2mL浓硝酸,c中反应的化学方程式是。在d中加适量NaOH溶液的目的是。
-
(4) 将反应后的溶液倒入烧杯,并向其中加入足量金属钠,观察到的现象是。
-
(5) 如表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是,理由是 (从用量角度和环保角度考虑)。
方案
反应物
甲
Cu、浓HNO3
乙
Cu、稀HNO3
丙
Cu、O2、稀HNO3
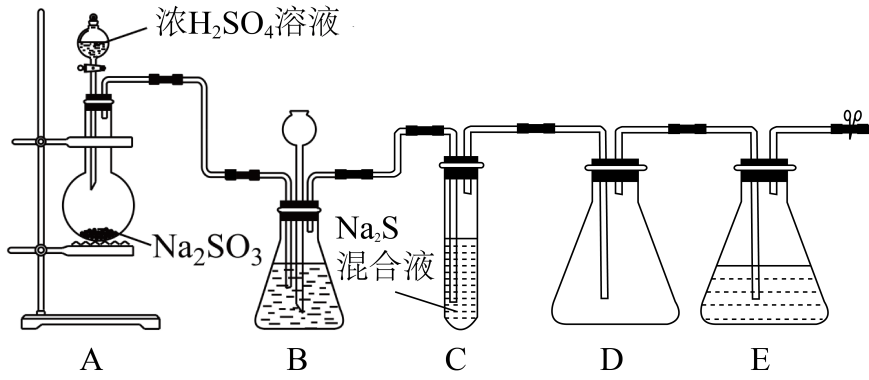
-
(1) 盛装浓H2SO4溶液的仪器名称为。仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若,则整个装置气密性良好。
-
(2) 圆底烧瓶中发生反应的化学方程式为。
-
(3) 装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体能选择(填字母)。
a.蒸馏水 b.饱和NaOH溶液 c.饱和NaHSO3溶液
-
(4) C试管中的试剂可以验证二氧化硫的氧化性,现象为。
为探究10 g固体Na3N的纯度(杂质不与水和HCl反应),某学习小组进行了如下实验。气体体积已经折合成标准状况下的体积。
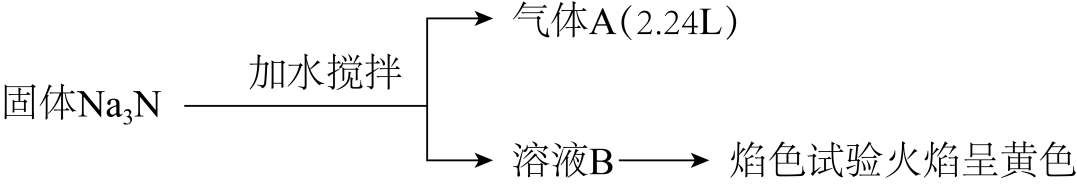
已知:Na3N与水反应会生成一种使湿润红色石蕊试纸变蓝的气体。溶液B与300 mL1.0mol·L-1的盐酸溶液恰好中和。
-
(5) Na3N与水反应的化学方程式为。
-
(6) 加热条件下NH3被CuO氧化,产物含2种单质。写出该反应的化学方程式。
-
(7) 由题中信息可计算出该固体中Na3N的纯度为。